Bài tập hỗn hợp este
Kỳ thi ĐGNL ĐHQG Hà Nội
Thủy phân hoàn toàn hỗn hợp X gồm 2 este mạch hở trong dung dịch NaOH đun nóng, sau phản ứng thu được m gam muối natri axetat và 10,8 gam hỗn hợp Y gồm 2 ancol no, mạch hở có cùng số nguyên tử cacbon. Đốt cháy hoàn toàn 10,8 gam hỗn hợp Y thu được 8,96 lít khí CO2 (đktc) và 10,8 gam H2O. Giá trị của m là
Do thủy phân X thu được muối natri axetat nên 2 este là este của axit axetic.
nCO2 = 0,4 mol; nH2O = 0,6 mol
=> n ancol = nH2O – nCO2 = 0,2 mol
Số C trong mỗi ancol: 0,4/0,2 = 2
Vậy 2 ancol là: CH3CH2OH (x mol) và C2H4(OH)2 (y mol)
x + y = 0,2
46x + 62y = 10,8
=> x = y = 0,1
Este là: CH3COOC2H5 (0,1 mol) và (CH3COO)2C2H4 (0,1 mol)
=> nCH3COONa = 0,3 mol
m = 0,3.82 = 24,6 gam
X là este 3 chức. Xà phòng hóa hoàn toàn 2,904 gam X bằng dung dịch NaOH, thu được chất hữu cơ Y có khối lượng 1,104 gam và hỗn hợp 3 muối của 1 axit cacboxylic thuộc dãy đồng đẳng của axit axetic và 2 axit cacboxylic thuộc dãy đồng đẳng của axit acrylic. Cho toàn bộ lượng Y tác dụng hết với Na, thu được 0,4032 lít H2 (đktc). Hỏi khi đốt cháy hoàn toàn 2,42 gam X thu được tổng khối lượng H2O và CO2 là bao nhiêu gam?
2,904 (g) X + NaOH → 1,104 (g) Y + 3 muối
Y + Na → 0,018 mol H2
=> nOH- ( trong Y) = 2nH2 = 0,036 (mol)
Vì X là este 3 chức => Y là ancol chức => nY = 1/3 nOH- = 0,012 (mol)
=> MY = 1,104/ 0,012 = 92 => Y là glixerol C3H5(OH)3
Gọi CTPT của X: CnH2n-8O6 ( vì X có 5 liên kết pi trong phân tử)
nX = nglixerol = 0,012 (mol) => Mx = 242 (g/mol)
Ta có:14n – 8 + 96 = 242
=> n = 11
Vậy CTPT của X là C11H14O6
Đốt cháy 2,42 (g) C11H14O6 → 11CO2 + 7H2O
0,01 →0,11 → 0,07 (mol)
=> mCO2 + mH2O = 0,11.44 + 0,07.18 = 6,1 (g)
Hỗn hợp X gồm vinyl axetat, metyl axetat và etyl fomat. Đốt cháy hoàn toàn 3,08 gam X, thu được 2,16 gam H2O. Phần trăm số mol của vinyl axetat trong X là:
$\begin{gathered} {n_{H2O}} = 0,12mol \hfill \\ X:\left\{ \begin{gathered}vinylaxetat:C{H_3}COOCH = C{H_2}:{C_4}{H_6}{O_2} \hfill \\ metylaxetat:C{H_3}COOC{H_3}:{C_3}{H_6}{O_2} \hfill \\etylfomiat:HCOO{C_2}{H_5}:{C_3}{H_6}{O_2} \hfill \\ \end{gathered} \right.\xrightarrow{{Qui\,\,doi}}\left\{ \begin{gathered}{C_4}{H_6}{O_2}:a(mol) \hfill \\{C_3}{H_6}{O_2}:b(mol) \hfill \\ \end{gathered}\right.\hfill\\\left\{\begin{gathered}\xrightarrow{{BTNT:H}}6a + 6b = 0,12.2 \hfill \\86a + 74b = 3,08 \hfill \\ \end{gathered} \right. = > \left\{ \begin{gathered}a = 0,01 \hfill \\b = 0,03 \hfill \\ \end{gathered} \right. \hfill \\\% vinylaxetat = 25\% \hfill \\ \end{gathered} $
Hỗn hợp CH3COOC2H5 , HCOOC3H5 và HCOOC3H3. Hỗn hợp X có tỉ khối hơi so với O2 là dX/O2 = 2,7. Đốt cháy hoàn toàn 0,015 mol X ; sau phản ứng thu được hỗn hợp sản phẩm Y. Hấp thụ Y vào dung dịch Ca(OH)2 dư. Kết luận nào dưới đây đúng?
\(\left. \begin{array}{*{35}{l}}{{C}_{4}}{{H}_{8}}{{O}_{2}} \\{{C}_{4}}{{H}_{6}}{{O}_{2}}~~~ \\{{C}_{4}}{{H}_{4}}{{O}_{2}} \\\end{array} \right\}=>~{{C}_{4}}{{H}_{n}}{{O}_{2}}\)
Có : dX/O2= 2,7 => MX = 86,4g
=> n = 6,4 (C4H6,4O2)
\(\begin{array}{*{20}{l}}{ {n_X} = {\rm{ }}0,015{\rm{ }} = > {\rm{ }}{n_{C{O_2}}} = {\rm{ }}0,06mol{\rm{ }} , {\rm{ }}{n_{{H_2}O}} = {\rm{ }}0,048mol}\\{{n_{CaC{O_3}}}{\rm{ }} = {\rm{ }}{n_{C{O_2}}}{\rm{ }} = {\rm{ }}0,06mol{\rm{ }} = > {\rm{ }}{m_{CaC{O_3}{\rm{ }}}} = {\rm{ }}6g}\\{ = > {\rm{ }}{m_{binh{\rm{ }}tang}} = {\rm{ }}{m_{C{O_2}}} + {\rm{ }}{m_{{H_2}O}}}\\{ = {\rm{ }}0,06.44{\rm{ }} + {\rm{ }}0,048.18}\\\begin{array}{l} = {\rm{ }}3,504{\rm{ }}\left( g \right) < {m_{CaC{O_3}}}\\ = > m{\,_{dung\,dich\,giam}} = 6 - 3,504 = 2,496g\end{array}\end{array}\)
X, Y, Z là ba axit cacboxylic đơn chức cùng dãy đồng đẳng (MX<MY<MZ), T là este tạo bởi X, Y, Z với một ancol no, ba chức, mạch hở E. Hỗn hợp M gồm X, Y, Z, T. Chia 79,8 gam hỗn hợp M thành 3 phần bằng nhau.
Phần 1: Đem đốt cháy hết bằng lượng vừa đủ khí O2, thu được 22,4 lít CO2 (đktc) và 16,2 gam H2O.
Phần 2: Cho tác dụng với lượng dư dung dịch AgNO3/NH3 đến khi xảy ra hoàn toàn, thu được 21,6 gam Ag.
Phần 3: Cho phản ứng hết với 400 ml dung dịch NaOH 1M và đun nóng, thu được dung dịch G. Cô cạn dung dịch G thu được m gam chất rắn khan. Giá trị của m gần nhất với
M có phản ứng tráng gương nên X là HCOOH, (X, Y, Z là các axit no đơn chức), Z là este no ba chức
Este T có độ bất bão hòa k = 3 nên:
\({{n}_{T}}=\dfrac{{{n}_{C{{O}_{2}}}}-{{n}_{{{H}_{2}}O}}}{2}=0,05\)
Mỗi mol T cần 3 mol H2O để quay trở lại axit và ancol nên quy đổi M thành:
CnH2nO2: a mol
CmH2m+2O3: b mol
H2O: -0,15 mol
nCO2 = na + mb = 1
nH2O = na + b.(m+1) - 0,15 = 0,9
mM = a.(14n + 32) + b.(14m + 50) - 18.0,15 = 26,6
Giải hệ trên được a = 0,4; b = 0,05
=> 0,4n + 0,05m = 1 => 8n + m = 20
=> m = 3, n = 2,125
Trong 26,6 gam M chứa CnH2nO2 là 0,4 mol; nNaOH = 0,4 mol
=> Chất rắn chứa CnH2n-1O2Na (0,4 mol)
=> m = 0,4.(14n+54) = 33,5 gam
Để thủy phân hết 7,668 gam hỗn hợp X gồm 2 este đơn chức và 2 este đa chức thì cần dùng vừa hết 80 ml dung dịch KOH aM. Sau phản ứng thu được hỗn hợp Y gồm các muối của các axit cacboxylic và các ancol. Đốt cháy hoàn toàn hỗn hợp Y thì thu được muối cacbonat; 4,4352 lít CO2 (đktc) và 3,168 gam H2O. Giá trị của a gần nhất với
Đốt Y: ${{n}_{C{{O}_{2}}~}}=0,198\text{ }mol,\text{ }{{n}_{{{H}_{2}}O}}=0,176\text{ }mol$
${{n}_{COO}}=0,08a\text{ }mol\Rightarrow {{n}_{{{K}_{2}}C{{O}_{3}}~}}=0,04a\text{ }mol,\text{ }{{n}_{O\left( X \right)}}=0,16a$
BTNT O: ${{n}_{O\left( X \right)}}+{{n}_{O\left( KOH \right)}}+{{n}_{O\left( {{O}_{2}} \right)}}=2{{n}_{C{{O}_{2}}}}+{{n}_{{{H}_{2}}O}}+3{{n}_{{{K}_{2}}C{{O}_{3}}}}$
=> 0,16a + 0,08a + ${{n}_{O\left( {{O}_{2}} \right)}}$= 0,198.2 + 0,176 + 0,04a.3
=> ${{n}_{O\left( {{O}_{2}} \right)}}$ = 0,572 - 0,12a
BTKL => ${{m}_{X}}+{{m}_{KOH}}+{{m}_{O\left( {{O}_{2}} \right)}}={{m}_{C{{O}_{2}}}}~+{{m}_{{{H}_{2}}O}}+{{m}_{{{K}_{2}}C{{O}_{3}}}}$
=> 7,668 + 0,08a.56 + 16(0,572 – 0,12a) = 44.0,198 + 18.0,176 + 0,04a.138
=> a = 1,667
Đốt cháy hoàn toàn 2,01 gam hỗn hợp X gồm axit acrylic, vinyl axetat, metyl metacrylat. Toàn bộ sản phẩm cháy cho qua dung dịch Ca(OH)2 dư, sau phản ứng thu được 9 gam kết tủa và dung dịch X. Vậy khối lượng dung dịch X đã thay đổi so với dung dịch Ca(OH)2 ban đầu là:
Các chất trong hỗn hợp đều chứa 2 liên kết pi và 2 nguyên tử oxi.
\(\left. \begin{array}{l}axit{\rm{ }}acrylic:C{H_2} = CH - COOH\\vinyl{\rm{ }}axetat:C{H_3}COOCH = C{H_2}\\metyl{\rm{ }}metacrylat:C{H_2} = C(C{H_3})C{\rm{O}}O - C{H_3}\end{array} \right\rangle = > X:{C_n}{H_{2n - 2}}{O_2}\)
\({{C}_{n}}{{H}_{2n-2}}{{O}_{2}}:\dfrac{2,01}{14n+30}\xrightarrow{+{{O}_{2}}}\left\{ \begin{align}& C{{O}_{2}} \\ & {{H}_{2}}O \\ \end{align} \right.\xrightarrow{+\text{dd}\,\,Ca{{(OH)}_{2}}\,\,}9gam\,\,CaC{{O}_{3}}\)
\(\begin{array}{l}BTNT\,\,C:{n_{CO2}} = {n_{CaCO3}} = {n_{C(X)}} = \dfrac{9}{{100}} = 0,09mol\\ = > {n_{hhX}} = \dfrac{{0,09}}{n}\\ \dfrac{{0,09}}{n}.(14n + 30) = 2,01 < = > n = 3,6\\X:{C_{3,6}}{H_{5,2}}{O_2}:0,025mol\\ = > {n_{{H_2}O}} = 0,065mol\\ {m_{C{O_2}}} + {m_{{H_2}O}} = 0,09.44 + 0,065.18 = 5,13gam\\{\Delta _{mdd{\rm{ }}sau{\rm{ }}pu}} = {\rm{ }}\left( {{m_{C{O_2}}} + {\rm{ }}{m_{{H_2}O}}} \right){\rm{ }}-{\rm{ m}} \downarrow = 5,13 - 9 = - 3,87gam\end{array}\)
∆mdd sau pư < 0 => Khối lượng dung dịch giảm 3,87gam
Hỗn hợp X gồm 1 este đơn chức, không no có một nối đôi C = C mạch hở (A) và 1 este no, đơn chức mạch hở (B). Đốt cháy hoàn toàn 0,15 mol X rồi cho toàn bộ sản phẩm cháy hấp thụ hoàn toàn vào bình đựng dung dịch Ca(OH)2 dư. Sau phản ứng thấy khối lượng bình tăng 23,9 gam và có 40 gam kết tủa. CTPT của 2 este là:
\(\begin{array}{l} X:\underbrace {\left\{ \begin{array}{l}A:{C_n}{H_{2n - 2}}{O_2}(n \ge 3):a\\B:{C_m}{H_{2m}}{O_2}(m \ge 2):b\end{array} \right.}_{0,15mol}\\\left\{ \begin{array}{l}m\,{\,_{binh \uparrow }} = {m_{C{O_2}}} + {m_{{H_2}O}}\\{n_{CO2}} = {n_{CaCO3}} = 0,4\end{array} \right. = > \left\{ \begin{array}{l}{n_{{H_2}O}} = 0,35\\{n_{C{O_2}}} = {n_{CaC{O_3}}} = 0,4\end{array} \right.\\ a = {n_{C{O_2}}} - {n_{{H_2}O}} = 0,05mol = > b = 0,15 - 0,05 = 0,1mol\\ BTNT\,C:\,0,05.n + 0,1.m = 0,4 = > n = 4,m = 2\\\left\{ \begin{array}{l}A:{C_4}{H_6}{O_2}\\B:{C_2}{H_4}{O_2}\end{array} \right.\end{array}\)
Hỗn hợp E gồm bốn chất mạch hở X, Y, Z, T (trong đó: X, Y ( MX < MY) là hai axit kế tiếp thuộc cùng dãy đồng đẳng axit fomic, Z là este hai chức tạo bởi X, Y và ancol T). Đốt cháy 37,56 gam E cần dùng 24,864 lít O2 (đktc), thu được 21,6 gam nước. Mặt khác, để phản ứng vừa đủ với 12,52 gam E cần dùng 380 ml dung dịch NaOH 0,5M. Biết rằng ở điều kiện thường, ancol T không tác dụng được với dung dịch Cu(OH)2. Phần trăm khối lượng của X có trong hỗn hợp E gần nhất với:
12,52 g E cần nNaOH = 0,19 (mol)
Đốt 37,56 g E cần nO2= 1,11 (mol) → nH2O = 1,2 (mol)
=> Đốt 12,52 g E cần 0,37 mol O2 → 0,4 mol H2O
Quy đổi hỗn hợp E thành:
CnH2nO2 : 0,19 mol
CmH2m+2O2 : a mol
H2O: - b mol
mE = 0,19 ( 14n + 32) + a( 14m + 34) – 18b = 12,52
nO2 = 0,19 ( 1,5n – 1) + a ( 1,5n – 0,5) = 0,37
nH2O = 0,19n + a( m + 1) –b = 0,4
=> a = 0,05; b = 0,04 và 0,19n + am = 0,39
=> 0,19n + 0,05m = 0,39
=> 19n + 5m = 39
T không tác dụng với Cu(OH)2 nên m ≥ 3. Vì n ≥ 1 nên m = 3 và n = 24/19 là nghiệm duy nhất.
=> HCOOH ( 0,14) và CH3COOH (0,05)
b = 0,04 => HCOO-C3H6-OOC-CH3: 0,02 mol
=> nHCOOH = 0,14 – 0,02 = 0,12 (mol)
=> %nHCOOH = 44,09%.
Đốt cháy hoàn toàn 5,4 gam hỗn hợp X gồm axit acrylic, axit oleic, vinyl axetat, metyl acrylat cần vừa đủ V lít O2(đktc). Hấp thụ toàn bộ sản phẩm chát vào nước vôi trong dư, sau khi phản ứng hoàn toàn thu được 30 gam kết tủa. Giá trị của V là
CH2=CH-COOH; C17H33COOH; CH3COOCH=CH2; CH2=CH-COOCH3 => tất cả các chất trong X đều có chứa 2 liên kết pi và có 2 oxi trong phân tử
=> Đặt công thức chung của X là: CnH2n-2O2: a (mol)
BTNT “C”: nCO2 = nCaCO3 = 0,3 (mol)
Ta có:
\(\left\{ \matrix{
\sum {{n_{C{O_2}}} = na = 0,3} \hfill \cr
\sum {{m_{hh}} = (14n + 30)a = 5,4} \hfill \cr} \right. \Rightarrow \left\{ \matrix{
a = 0,04 \hfill \cr
n = 7,5 \hfill \cr} \right.\)
Có: nH2O = nCO2 – nX = 0,3 – 0,04 = 0,26 (mol)
BTNT “O”: 2nX + 2nO2 = 2nCO2 + nH2O
=> 2.0,04 + 2.nO2 = 2.0,3 + 0,26
=> nO2 = 0,39 (mol)
=> VO2(đktc) = 0,39.22,4 = 8,736 (l)
Đốt cháy hoàn toàn m gam hỗn hợp A gồm 3 este X, Y, Z (đều mạch hở và chỉ chứa chức este, X có khối lượng nhỏ nhất trong A) thu được số mol CO2 lớn hơn số mol H2O là 0,25 mol. Mặt khác, m gam A phản ứng vừa đủ với dung dịch NaOH thu được 22,2 gam hai ancol hơn kém nhau 1 nguyên tử cacbon và hỗn hợp T gồm hai muối. Đốt cháy hoàn toàn T cần vừa đủ 0,275 mol O2, thu được CO2, 0,35 mol Na2CO3 và 0,2 mol H2O. Phần trăm khối lượng của X trong A là
Sơ đồ bài toán:
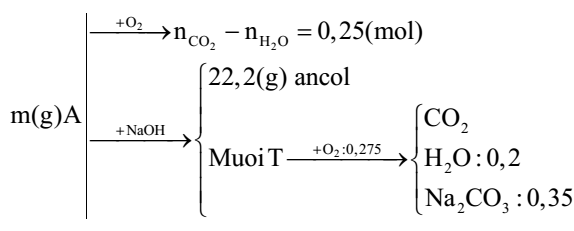
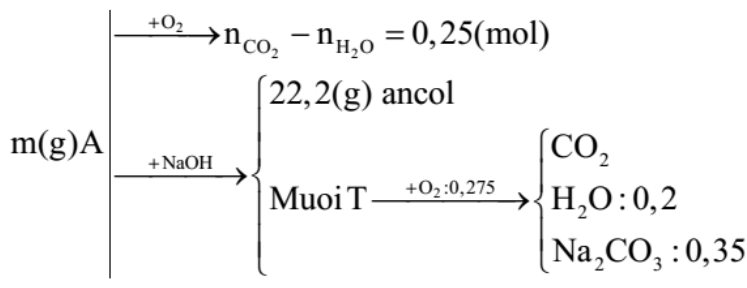
Do các este đều mạch hở và chỉ chứa chức este nên không phải là este của phenol.
- Xét phản ứng đốt muối T:
nCOO = nNaOH = 2nNa2CO3 = 0,7 mol → nO(T) =2nCOO =1,4 mol
BTNT "O": nO(T) + 2nO2(đốt T) = 2nCO2 + nH2O + 3nNa2CO3 → 1,4 + 0,275.2 = 2nCO2 + 0,2 + 0,35.3
→ nCO2 = 0,35 mol
BTKL: m muối =mCO2 + mH2O + mNa2CO3 - mO2(đốt T) =0,35.44 + 0,2.18 + 0,35.106 - 0,275.32 = 47,3 gam
- Xét phản ứng thủy phân A trong NaOH:
BTKL: mA = m muối + m ancol - mNaOH = 47,3 + 22,2 - 0,7.40 = 41,5 gam
- Xét phản ứng đốt A:
Đặt nCO2 = x và nH2O = y (mol)
+ nO(A) = 2nCOO = 1,4 mol. BTKL: mA = mC + mH + mO → 12x + 2y + 1,4.16 = 41,5 (1)
+ nCO2 - nH2O = 0,25 → x - y = 0,25 (2)
Giải hệ (1) và (2) thu được x = 1,4 và y = 1,15
BTNT "O": nO2 (đốt A) = [2nCO2 + nH2O - nO(A)]/2 = (2.1,4 + 1,15 - 1,4)/2 = 1,275 mol
- Xét phản ứng đốt ancol (phản ứng giả sử):
nO2 (đốt ancol) = nO2(đốt A) - nO2(đốt T) = 1,275 - 0,275 = 1 mol
Đặt nCO2 = a; nH2O = b (mol)
BTKL: mCO2 + mH2O = m ancol + mO2(đốt ancol) → 44a + 18b = 22,2 + 32 (3)
BTNT "O": 2nCO2 + nH2O = nO(ancol) + 2nO2 → 2a + b = 0,7 + 2 (4)
Giải (3) và (4) thu được: a = 0,7 và b = 1,3
Nhận thấy: nO(ancol) = nCO2 → Các ancol đều có số C bằng số O → Các ancol chỉ có thể là ancol no
→ n ancol =nH2O - nCO2 = 1,3 - 0,7 = 0,6 mol
→ 1 (CH3OH: u mol) < C tb =0,7: 0,6 = 1,16 < 2 (HO-CH2-CH2-OH: v mol)
nCO2 = u + 2v = 0,7 và u + v = 0,6
Giải được u = 0,5 và v = 0,1
- Phản ứng đốt muối T:
nC(T) = nCO2 + nNa2CO3 = 0,35 + 0,35 = 0,7 mol
nC(T) = nCOO → Số C trong T bằng số nhóm COO
→ 2 muối là HCOONa (n mol) và (COONa)2 (m mol)
m muối =68n + 134m = 47,3; nC(muối) = n + 2m = 0,7
→ n = 0,4 và m = 0,15
Vậy A chứa:
HCOOCH3 (0,2 mol) → mHCOOCH3 = 0,2.60 = 12 gam
(HCOO)2C2H4 (0,1 mol) → m(HCOO)2C2H4 = 0,1.118 = 11,8 gam
(COOCH3)2 (0,15 mol) → m(COOCH3)2 = 0,15.118 = 17,7 gam
Nhận thấy (HCOO)2C2H4 có khối lượng nhỏ nhất → %mX = 11,8/41,5.100% = 28,43%
Cho các hợp chất hữu cơ mạch hở: X, Y là hai axit cacboxylic; Z là ancol no; T là este đa chức tạo bởi X, Y với Z. Đun nóng 33,7 gam hỗn hợp E chứa X, Y, Z, T với 400 ml dung dịch NaOH 1M vừa đủ thu được ancol Z và hỗn hợp F gồm 2 muối. Dẫn toàn bộ Z qua bình đựng Na dư thấy khối lượng bình tăng 15 gam; đồng thời thu được 5,6 lít khí H2 (ở đktc). Đốt cháy hoàn toàn F cần dùng 0,7 mol O2 thu được Na2CO3, H2O và 0,6 mol CO2. Phần trăm khối lượng của T trong E có giá trị gần nhất với giá trị nào sau đây?
X, Y đơn chức
Z, T hai chức
*Z + Na:
R(OH)2 → H2
0,25 ← 0,25
m bình tăng = mZ – mH2 => mZ = 15 + 0,25.2 = 15,5 gam => MZ = 15,5/0,25 = 62 => Z là C2H4(OH)2
*Đốt F:
nNa2CO3 = 0,5nNaOH = 0,2 mol; nO(F) = 2nNaOH = 0,8 mol
BTNT O: nH2O = nO(F) + 2nO2 - 3nNa2CO3 – 2nCO2 = 0,8 + 0,7.2 – 0,6.2 – 0,2.3 = 0,4 mol
BTKL => m muối = mNa2CO3 + mCO2 + mH2O – mO2 = 0,2.106 + 0,6.44 + 0,4.18 – 0,7.32 = 32,4 gam
$\bar RCOONa:0,4mol \to \bar R + 67 = \dfrac{{32,4}}{{0,4}} \to \bar R = 14$ => Có axit là HCOOH
*E + NaOH: T có dạng là ${(\bar RCOO)_2}{C_2}{H_4}$ => MT = (14+44).2+28 = 144
BTKL => mH2O = mE + mNaOH – m muối – mZ = 33,7 + 0,4.40 – 32,4 – 15,5 = 1,8 gam => naxit = nH2O = 0,1 mol
=> neste = (nNaOH-naxit)/2 = 0,15
=> mT = 0,15.144 = 21,6 gam => %mT = 64,1%
Cho X và Y (MX < MY) là hai este đều mạch hở, không phân nhánh và không chứa nhóm chức khác. Đốt cháy X cũng như Y với lượng oxi vừa đủ, luôn thu được CO2 có số mol bằng số mol O2 đã phản ứng. Đun nóng 15,12 gam hỗn hợp E chứa X, Y (số mol của X gấp 1,5 lần số mol Y) cần dùng 200 ml dung dịch KOH 1M, thu được hỗn hợp F chứa 2 ancol và hỗn hợp K chứa 2 muối. Dẫn toàn bộ F qua bình đựng Na dư thấy khối lượng bình tăng 7,6 gam. Đốt cháy hoàn toàn hỗn hợp muối K cần dùng 0,21 mol O2. Phần trăm khối lượng của Y trong hỗn hợp E là
Bảo toàn gốc OH ta có: nOH ancol = nKOH = 0,2 mol
-OH + Na → -ONa + ½ H2
⟹ nH2 = ½ . nOH ancol = 0,1 mol
Bảo toàn khối lượng ta có: mF = 7,6 + 0,1.2 = 7,8 (g)
*Bảo toàn khối lượng ta có: mmuối = 15,12 + 0,2.56 - 7,8 = 18,52 (g)
Bảo toàn nguyên tố kali ta có: nCOOK = nKOH = 0,2 mol; nK2CO3 = 0,1 mol
Đặt nCO2 = x mol; nH2O = y mol
Bảo toàn nguyên tố oxi ta có 0,2 . 2 + 0,21 . 2 = 0,1 . 3 + 2x + y
Bảo toàn khối lượng ta có 18,52 + 0,21 . 32 = 0,1 . 138 + 44x + 18y
Giải hệ có x = 0,26 mol và y = 0 mol ⟹ Muối không chứa H ⟹ Muối phải là của axit 2 chức.
⟹ X và Y là este 2 chức ⟹ nX = 0,06 mol ; nY = 0,04 mol
Đặt số C trong gốc axit của X và Y là a và b
Ta có 0,06a + 0,04b = 0,1 + 0,26
Giải phương trình nghiệm nguyên a = 2 và b = 6
⟹ 2 muối là (COOK)2 và KOOCC≡C-C≡CCOOK
Mặt khác, đốt X hay Y đều cho nCO2 = nO2
⟹ X và Y có dạng Cn(H2O)m.
Lại có X và Y đều là este 2 chức → m = 4 → X và Y đều chứa 8H
Do X và Y mạch hở ⟹ 2 ancol đều đơn chức ⟹ nF = nOH = 0,2 mol ⟹ MF = 39 ⟹ chứa CH3OH
Do đó X là CH3OOCCOOC2H5 và Y là CH3OOCC≡C-C≡CCOOC2H5
→ %mY = 47,62%
Để phản ứng hết với một lượng hỗn hợp gồm 2 chất hữu cơ X và Y (MX < MY) cần vừa đủ 300 ml dung dịch NaOH 1M. Sau khi phản ứng xảy ra hoàn toàn thu được 24,6 gam muối của một axit hữu cơ và m gam một ancol. Đốt cháy hoàn toàn lượng ancol trên thu được 4,48 lít khí CO2 (đktc) và 5,4 gam nước. Công thức của Y là
nCO2 < nH2O → ancol no hở, đơn chức
=> n ancol = nH2O-nCO2 = 0,1
=>C=nCO2 : nancol = 2 => ancol là C2H6O
Vì nNaOH > nC2H6O → X là axit còn Y là este tạo bởi C2H5OH và axit X
nRCOONa = nNaOH = 0,3 → M = 82 → MR=15 → CH3COONa
→ Y là CH3COOC2H5
Đốt cháy hoàn toàn m gam hỗn hợp X gồm hai este đồng phân cần dùng 27,44 lít khí O2, thu được 23,52 lít khí CO2 và 18,9 gam H2O. Nếu cho m gam X tác dụng hết với 400 ml dung dịch NaOH 1M, cô cạn dung dịch sau phản ứng thì thu được 27,9 gam chất rắn khan, trong đó có a mol muối Y và b mol muối Z (MY < MZ). Các thể tích khí đều đo ở điều kiện tiêu chuấn. Tỉ lệ a : b là
${n_{{O_2}}}{\text{ }} = {\text{ }}1,225;{\text{ }}{n_{C{O_2}}}{\text{ }} = {\text{ }}1,05;{\text{ }}{n_{{H_2}O}} = {\text{ }}1,05$
=> X no, đơn chức, mạch hở
- Bảo toàn O: nX = ${{n}_{{{H}_{2}}O}}+2.{{n}_{C{{O}_{2}}}}-2.{{n}_{{{O}_{2}}}}$ => nX = 0,35
Bảo toàn khối lượng: ${{m}_{X}}+{{m}_{{{O}_{2}}}}={{m}_{C{{O}_{2}}}}+{{m}_{{{H}_{2}}O}}$ => mX = 25,9
=> MX = 74 => X có CTPT: C3H6O2
Vì X gồm 2 đồng phân => HCOOC2H5 (a mol) và CH3COOCH3 (b mol)
Ta có: nX = a + b = 0,35
X no, đơn chức, mạch hở => nNaOH phản ứng = nX = 0,35 mol
=> nNaOH dư = 0,4 – 0,35 = 0,05 mol
m rắn = mmuối + mNaOH dư = 68a + 82b + 0,05.40 = 27,9
=> a = 0,2 và b = 0,15
=> a : b = 4 : 3
Chất X (C10H16O4) có mạch cacbon không phân nhánh. Cho a mol X phản ứng hết với dung dịch NaOH, thu được chất Y và 2a mol chất Z. Đun Z với dung dịch H2SO4 đặc, thu được chất T có tỉ khối hơi so với Z là 0,7. Nhận định nào sau đây là sai?
Chất X có độ bất bão hòa là: k = (2C + 2 – H):2 = 3
- Khi đun Z với H2SO4 đặc thu được chất T nhẹ hơn Z nên MT = MZ – 18
${d_{T/Z}} = \dfrac{{{M_T}}}{{{M_Z}}} = \dfrac{{{M_Z} - 18}}{{{M_Z}}} = 0,7 \to {M_Z} = 60({C_3}{H_8}O)$
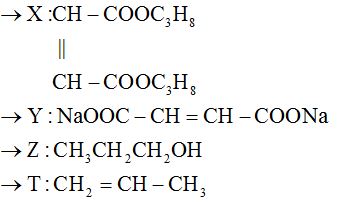
A, B, D, đúng
C sai vì 1 mol Y đốt cháy chỉ thu được 3 mol CO2: C4H2O4Na2 + 3O2 → 3CO2 + H2O + Na2CO3
Đốt cháy hoàn toàn 10,58 gam hỗn hợp X chứa ba este đều đơn chức, mạch hở bằng lượng oxi vừa đủ, thu được 8,96 lít khí CO2 (đktc). Mặt khác, hiđro hóa hoàn toàn 10,58 gam X cần dùng 0,07 mol H2 (xúc tác, to) thu được hỗn hợp Y. Đun nóng toàn bộ Y với 250 ml dung dịch NaOH 1M, cô cạn dung dịch sau phản ứng, thu được một ancol Z duy nhất và m gam rắn khan. Giá trị của m là
\({m_Y} = {\text{ }}{m_X} + {\text{ }}{m_{{H_2}}}{\text{ }} = {\text{ }}10,72\)
Đốt X cũng như đốt Y đều thu được \({n_{C{O_2}}}{\text{ }} = {\text{ }}0,4\)
\({{C_{\overline n }}{H_{2\overline n }}{O_2} + {O_2}\xrightarrow{{{t^o}}}{\text{ }}\overline n C{O_2}{\text{ }} + {\text{ }}\overline n {H_2}O}\)
\({\dfrac{{10,72}}{{14\overline n + 32}}\,\,\,\,\,\,\,\,\,\,\,\,\,\, \to \,\,\,\,\,\,\,\,\,\,\,0,4}\)
\({ = > {\text{ }}\overline n {\text{ }} = {\text{ }}2,5}\)
=> Y chứa HCOOCH3 => ancol Z: CH3OH
nY = 0,16 => \({n_{C{H_3}OH{\text{ }}}} = {\text{ }}0,16\)
- m rắn = mY + mNaOH - mCH3OH = 15,6
Hỗn hợp E gồm ba este X, Y, Z đều đơn chức, mạch hở là đồng phân cấu tạo của nhau ( trong đó X có số mol nhỏ nhất). Cho 5,16 gam E tác dụng với dung dịch NaOH vừa đủ. Sau phản ứng hoàn toàn, thu được 4,36 gam hỗn hợp F gồm hai muối của hai axit cacboxylic kế tiếp nhau trong cùng một dãy đồng đẳng và hỗn hợp hơi M gồm các chất hữu cơ no, đơn chức. Cho F phản ứng với lượng dư dung dịch AgNO3 trong NH3, thu được 8,64 gam Ag. Cho hỗn hợp M phản ứng với lượng dư dung dịch AgNO3 trong NH3, thu được 6,48 gam Ag. Thành phần phần trăm về khối lượng của X trong E là
$\underbrace {X,Y,Z}_{E = 5,16{\kern 1pt} g} + NaOH{\mkern 1mu}dư\xrightarrow{{}}\left\{ \begin{gathered}F\xrightarrow{{ + AgN{O_3}}}Ag:0,08{\mkern 1mu} mol \hfill \\M\xrightarrow{{ + AgN{O_3}}}Ag:0,06{\mkern 1mu} mol \hfill \\ \end{gathered} \right.$
F có phản ứng với AgNO3 => trong F phải có muối HCOONa => muối còn lại là CH3COONa
${n_{HCOONa}} = \dfrac{1}{2}{n_{Ag}} = \dfrac{1}{2}{\mkern 1mu} .0,08 = 0,04(mol)$
$ = > {n_{C{H_3}COONa}} = \dfrac{{4,36 - a.68}}{{82}} = 0,02{\mkern 1mu} (mol)$
${n_{este}} = \sum {{n_{muối}} = 0,04 + 0,02 = 0,06(mol)} $
$= > {{\bar M}_{este}} = \dfrac{{5,16}}{c} = 86(g/mol)$
$= > {\text{ }}CTPT\,của\,E\,:\,{C_4}{H_6}{O_2}$
=> E chứa: CH3COOCH=CH2: 0,02 (mol) ; HCOOR: a (mol) và HCOOR’: b (mol)
=> a + b = 0,06 (1)
M tham gia phản ứng tráng bạc => M chứa anđehit. Có nAg = 0,06 > 2nCH3COOCH=CH2 = 0,04
=> E chứa 1 este có cấu tạo HCOOC=C-CH3: $\dfrac{{0,06 - 0,04}}{2} = 0,01{\mkern 1mu} (mol)$
Este còn lại có cấu tạo HCOOCH=CH-CH3: 0,03 (mol) hoặc HCOOC(CH3)=CH2 : 0,03 (mol)
Vậy X là HCOOCH=CH-CH3
$ = > \% X = \dfrac{{0,01.86}}{{5,16}}.100\% = 16,67\% {\text{ }}$
Đốt cháy hoàn toàn 0,33 mol hỗn hợp X gồm metyl propionat, metyl axetat và 2 hidrocacbon mạch hở cần vừa đủ 1,27 mol O2 tạo ra 14,4g H2O. Nếu cho 0,33 mol X vào dung dịch Br2 dư thì số mol Br2 phản ứng tối đa là:
Gọi k là số liên kết π trong X => nCO2 – nH2O = (k – 1).nX
=> nπ(X) – nX = nCO2 – nH2O
Đặt x là số mol gốc COO có trong X => nO(X) = 2x mol và nπ (COO) = x mol
- Khi đốt cháy X: Bảo toàn Oxi: nO(X) + 2nO2 = 2nCO2 + nH2O
=> 2x + 2.1,27 = 2nCO2 + 0,8
=> nCO2 = (0,87 + x) mol
=> nπ (X) = nCO2 – nH2O + nX = (0,87 + x) – 0,8 + 0,33 = 0,4 + x
Vì chỉ có liên kết π ngoài COO mới phản ứng được với Br2
=> nπ (gốc hidrocacbon) = nπ (X) – nπ (COO) = (0,4 + x) – x = 0,4 mol
=> nBr2 = 0,4 mol
Ba chất hữu cơ A, B, D có cùng CTPT C6H10O4, mạch thẳng, không tác dụng với Na. Biết rằng khi tác dụng với dd NaOH thì A tạo thành 1 muối và 2 ancol kế tiếp nhau trong dãy đồng đẳng, B tạo thành 2 muối và 1 ancol, D tạo thành 1 muối và 1 ancol. Nhận định nào sau đây không đúng?
$ k = \dfrac{{2 + 2x - y}}{2} = \dfrac{{2 + 12 - 10}}{2} = 2$
- A, B, D không phản ứng với Na =>A, B, D không có H linh động
- A + NaOH → 1 muối + 2 ancol kế tiếp nhau trong cùng 1 dãy đồng đẳng. Vậy A là este của axit 2 chức no và 2 ancol no đơn chức đồng đẳng kế tiếp.
→ CTCT của A: CH3OOC-CH2-COO-C2H5
- B + NaOH →2 muối + 1ancol => B là este của ancol 2 chức no và 2 axit đơn chức no
→ CTCT của B: HCOO-CH2-CH2-CH2-OOCCH3 hoặc HCOO-CH2-CH2-OOC-CH2-CH3
- D + NaOH → 1 muối + 1 ancol => D là este của 1 axit no 2 chức và 1 ancol no đơn chức hoặc 1 axit no đơn chức và 1 ancol no hai chức.
→ Vậy D có thể có các CTCT sau:
CH3-OOC-CH2-CH2-COOCH3 ; C2H5-OOC-COO-C2H5 ; CH3-COO-CH2-CH2-OOC-CH3, HCOO-CH2-CH2-CH2-CH2-OOCH

