Bài tập nitric acid
Kỳ thi ĐGNL ĐHQG Hà Nội
Cho 19,2 gam kim loại M tan trong dung dịch HNO3 dư được 4,48 lít NO (đktc, là sản phẩm khử duy nhất). M là
nNO = 0,2 mol
Quá trình cho – nhận e:
$\overset{0}{\mathop{M}}\,\to \overset{+n}{\mathop{M}}\,\,+\,ne~~~~~~\,\,\,\,\,\,\,\,~~~\overset{+5}{\mathop{N}}\,\,\,+\text{ 3}e\to \overset{+2}{\mathop{\,N}}\,O$
$\frac{0,6}{n}$ ← 0,6 0,6 ← 0,2
$=>\,\,\frac{19,2}{M}=\frac{0,6}{n}\,\,=>\,\,M=32n$
Với n = 2 => M = 64 => M là Cu
Hoà tan hết 5,4 gam kim loại M trong HNO3 dư được 8,96 lít khí đktc gồm NO và NO2, dX/H2 = 21. Tìm M biết rằng N+2 và N+4 là sản phẩm khử của N+5
Gọi nNO = x mol; nNO2 = y mol
=> nhỗn hợp khí = x + y = 0,4 mol (1)
$\bar{M}=\frac{30x+46y}{x+y}=21.2$ (2)
Từ (1) và (2) => x = 0,1; y = 0,3
Quá trình cho – nhận e:
$\begin{align}& \overset{0}{\mathop{M}}\,\to \overset{+n}{\mathop{M}}\,\,+\,ne;\,\,\,\,\,\,\,\,\overset{+5}{\mathop{N}}\,\,\,+\text{ 3}e\to \overset{+2}{\mathop{\,N}}\,O \\ & \,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\overset{+5}{\mathop{N}}\,\,\,+\text{ 1}e\to \overset{+4} {\mathop{\,N}}\,{{O}_{2}} \\ \end{align}$
Bảo toàn e: ne cho = ne nhận = 3.nNO + nNO2 = 0,6
$=>\,\,\frac{5,4}{M}.n=0,6\,\,=>\,\,M=9n$
Với n = 3 => M = 27 => M là Al
Cho 11 gam hỗn hợp gồm Al và Fe vào dung dịch HNO3 dư được 6,72 lít NO (đktc, là sản phẩm khử duy nhất). Khối lượng của Al và Fe lần lượt là
Gọi số mol của Al và Fe lần lượt là x và y mol
=> mhỗn hợp = 27x + 56y = 11 (1)
Quá trình cho – nhận e:
\(\begin{align}& Al\to \overset{+3}{\mathop{Al}}\,\,\,\,+\,\,\,3e~~~~~~\,\,\,\,\,\,\,\,~~\overset{+5}{\mathop{N}}\,\,\,+\text{ 3}e\to \overset{+2}{\mathop{\,N}}\,O \\ & Fe\,\to \overset{+3}{\mathop{\,Fe}}\,\,\,+\,\,\,3e \\ \end{align}\)
Bảo toàn e: 3.nAl + 3.nFe = 3.nNO => x + y = 0,3 (2)
Từ (1) và (2) => x = 0,2; y = 0,1
=> mAl = 0,2.27 = 5,4 gam; mFe = 0,1.56 = 5,6 gam
Hoà tan hết m gam Al vào dung dịch HNO3 dư được 0,01 mol NO và 0,015 mol N2O là các sản phẩm khử của N+5. Giá trị của m là
Xét quá trình cho – nhận e:
$\begin{align}& Al\to \overset{+3}{\mathop{Al}}\,\,+\,3e~~~~~~\,\,\,\,\,~~\overset{+5}{\mathop{N}}\,\,\,+\text{ 3}e\to \overset{+2}{\mathop{\,N}}\,O \\ & \,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\overset{+5}{\mathop{2N}}\,\,\,+\text{ 8}e\to \overset{+1}{\mathop{\,{{N}_{2}}}}\,O \\ \end{align}$
Bảo toàn e: 3.nAl = 3.nNO + 8.nN2O => nAl = (3.0,01 + 8.0,015) / 3 = 0,05 mol
=> m = 0,05.27 = 1,35 gam
Cho 6,4 gam Cu tan vừa đủ trong 200ml dung dịch HNO3 thu được khí X gồm NO và NO2, dX/H2 = 18 (không còn sản phẩm khử nào khác của N+5). Nồng độ mol/lít của dung dịch HNO3 đã dùng là
nCu = 0,1 mol
Gọi số mol của NO và NO2 lần lượt là x và y mol
Xét quá trình cho – nhận e:
$\begin{align}& Cu\to \overset{+2}{\mathop{Cu}}\,\,+\,2e~~~~~~\,\,\,\,~~\overset{+5}{\mathop{N}}\,\,\,+\text{ 3}e\to \overset{+2}{\mathop{\,N}}\,O \\ & \,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\overset{+5}{\mathop{N}}\,\,\,+\text{ 1}e\to \overset{+4}{\mathop{\,N}}\,{{O}_{2}} \\ \end{align}$
Bảo toàn e: 2.nCu = 3.nNO + nNO2 => 3x + y = 0,2 (1)
\({\bar M_X} = \dfrac{{30x + 46y}}{{x + y}} = 18.2\,\,\,\,(2)\)
Từ (1) và (2) => x = 1/18 mol; y = 1/30 mol
Bảo toàn nguyên tố N: nHNO3 phản ứng = nNO3 (trong muối) + nNO + nNO2 = 0,1.2 + 1/18 + 1/30 = 13/45 mol
=> CM HNO3 = 13/9 M
Cho 1,35 gam hỗn hợp gồm Cu, Mg, Al tác dụng hết với dung dịch HNO3 thu được hỗn hợp khí gồm 0,01 mol NO và 0,04 mol NO2 (không còn sản phẩm khử nào khác của N+5). Khối lượng muối trong dung dịch là
Bước 1: Tính ne cho
Bảo toàn e: ne cho = ne nhận = 3.nNO + nNO2 = 3.0,01 + 0,04 = 0,07 mol
Bước 2: Tính mmuối
- nNO3 (trong muối) = ne cho = 0,07 mol
⟹ mNO3 = 62.0,07 = 4,34 gam
- mmuối = mkim loại + mNO3 = 1,35 + 4,34 = 5,69 gam
Hòa tan hoàn toàn 8,9 gam hỗn hợp gồm Mg và Zn bằng lượng vừa đủ 500 ml dung dịch HNO3 1M. Sau khi các phản ứng kết thúc, thu được 1,008 lít khí N2O (đktc, khí duy nhất) và dung dịch X chứa m gam muối. Giá trị của m là
nN2O = 0,045 mol
Gọi số mol của Mg và Zn lần lượt là x và y mol => mhỗn hợp = 24x + 65y = 8,9 (1)
Giả sử trong X chứa muối NH4NO3 (a mol)
Xét quá trình cho – nhận e:
$\begin{align}& Mg\to \overset{+2}{\mathop{Mg}}\,\,+\,2e~~~~~~\,\,\,\,\,\,\,\,~~\overset{+5}{\mathop{2N}}\,\,\,+\text{ 8}e\to {{\overset{+1}{\mathop{\,N}}\,}_{2}}O \\ & Zn\to \overset{+2}{\mathop{Zn}}\,\,+\,2e\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\overset{+5}{\mathop{N}}\,\,\,+8e\to \overset{-3}{\mathop{\,N}}\,{{H}_{4}} \\ \end{align}$
Bảo toàn e: 2.nMg + 2.nZn = 8.nN2O + 8.nNH4NO3 => 2x + 2y = 0,36 + 8a (2)
nNO3 (trong muối) = ne cho = 2x + 2y mol
Bảo toàn nguyên tố N: nHNO3 = nNO3 (trong muối) + 2.nN2O + 2.nNH4NO3
=> 0,5 = 2x + 2y + 2.0,045 + 2a (3)
Từ (1), (2) và (3) => x = 0,1; y = 0,1; a = 0,005
=> mmuối = mkim loại + mNO3 (trong muối KL) + mNH4NO3 = 8,9 + 62.(2.0,1 + 2.0,1) + 80.0,005 = 34,1 gam
Hoà tan hết hỗn hợp X gồm Zn và ZnO trong dung dịch HNO3 loãng dư thấy không có khí bay ra và trong dung dịch chứa 113,4 gam Zn(NO3)2 và 8 gam NH4NO3. Phần trăm khối lượng Zn trong X là
nZn(NO3)2 = 0,6 mol; nNH4NO3 = 0,1 mol
ZnO tác dụng với HNO3 không sinh ra sản phẩm khử vì đã đạt số oxi hóa tối đa
Bảo toàn e: 2.nZn = 8.nNH4NO3 => nZn = 4.0,1 = 0,4 mol
Bảo toàn nguyên tố Zn: nZn(NO3)2 = nZn + nZnO => nZnO = 0,6 – 0,4 = 0,2 mol
\( = > \,\,\% {m_{Zn}} = \frac{{0,4.65}}{{0,4.65 + 0,2.81}}.100\% = 61,61\% \)
Cho hỗn hợp gồm 6,72 gam Mg và 0,8 gam MgO tác dụng hết với lượng dư dung dịch HNO3. Sau khi các phản ứng xảy ra hoàn toàn, thu được 0,896 lít một khí X (đktc) và dung dịch Y. Làm bay hơi dung dịch Y thu được 46 gam muối khan. Khí X là
nMg = 0,28 mol; nMgO = 0,02 mol
MgO tác dụng với HNO3 không sinh ra sản phẩm khử vì đã đạt số oxi hóa tối đa
Ta có: nMg(NO3)2 = nMg + nMgO = 0,28 + 0,02 = 0,3 mol => mMg(NO3)2 = 44,4 gam < 46
=> muối khan chứa Mg(NO3)2 và NH4NO3
=> nNH4NO3 = 0,02 mol
Quá trình cho – nhận e:
$\begin{align}& \overset{0}{\mathop{M}}\,g\to \overset{+2}{\mathop{Mg}}\,\,+\,2e~~~~~~\,\,\,~~\overset{+5}{\mathop{N}}\,\,\,+\text{ n}e\to X \\ & \,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\overset{+5}{\mathop{N}}\,\,\,+\text{ 8}e\to \overset{-3}{\mathop{\,N}}\,{{H}_{4}} \\ \end{align}$
Bảo toàn e: 2.nMg = n.nX + 8.nNH4NO3 => 2.0,28 = 0,04.n + 8.0,02 => n = 10
=> X là N2
Cho 20,88 gam FexOy phản ứng với dung dịch HNO3 dư được 0,672 lít khí B (đktc, là sản phẩm khử duy nhất) và dung dịch X. Trong dung dịch X có 65,34 gam muối. Oxit của sắt và khí B là
Muối thu được là Fe(NO3)3 0,27 mol
Coi hỗn hợp ban đầu gồm Fe và O
Bảo toàn nguyên tố Fe: nFe(NO3)3 = nFe = 0,27 mol
=> mO = 20,88 – 0,27.56 = 5,76 gam => nO = 0,36 mol
=> nFe : nO = 0,27 : 0,36 = 3 : 4 => oxit sắt là Fe3O4
Xét quá trình cho – nhận e:
$\begin{align}& Fe\to \overset{+3}{\mathop{Fe}}\,\,+\,3e~~~~~~\,\,\,\,~~\overset{+5}{\mathop{\,\,N}}\,\,\,+\text{ n}e\to X \\ & \,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\overset{0}{\mathop{O}}\,\,\,+\text{ 2}e\to \overset{-2}{\mathop{O}}\, \\ \end{align}$
Bảo toàn e: 3.nFe = n.nX + 2.nO => 3.0,27 = n.0,03 + 2.0,36 => n = 3
=> X là NO
Hoà tan đến phản ứng hoàn toàn 0,1 mol FeS2 vào HNO3 đặc nóng dư. Thể tích NO2 bay ra (ở đktc, biết rằng N+4 là sản phẩm khử duy nhất của N+5) là
Xét quá trình cho – nhận e:
$\begin{align}& Fe{{S}_{2}}\to \,\,F{{e}^{3+}}+\,\,2\overset{+6}{\mathop{S}}\,\,\,+\,\,15e\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\overset{+5}{\mathop{N}}\,\,\,+\,\,1e\,\,\to \,\,\overset{+4}{\mathop{N}}\,{{O}_{2}} \\ & 0,1\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\to \,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,1,5\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,1,5\,\,\,\,\to \,\,\,\,1,5 \\ \end{align}$
=> VNO2 = 1,5.22,4 = 33,6 lít
Cho 19,2 gam Cu phản ứng với 500 ml dung dịch NaNO3 1M và 500 ml HCl 2M. Tính thể tích khí NO thoát ra (đktc) biết NO là sản phẩm khử duy nhất của N+5 :
nCu = 0,3 mol; nNaNO3 = 0,5 mol; nHCl = 1 mol
3Cu + 8H+ + 2NO3- → 3Cu2+ + 2NO + 4H2O
Xét \(\dfrac{{{n_{Cu}}}}{3} = \dfrac{{0,3}}{3} = 0,1;\,\,\,\,\dfrac{{{n_{{H^ + }}}}}{8} = \dfrac{1}{8} = 0,125;\,\,\,\,\dfrac{{{n_{NO_3^ - }}}}{2} = \dfrac{{0,5}}{2} = 0,25\)
=> Cu hết, H+ và NO3- còn dư
=> nNO = 2/3.nCu = 0,2 mol => VNO = 4,48 lít
Cho 4,8 gam S tan hết trong 100 gam HNO3 63% thu được NO2 (sản phẩm khử duy nhất, khí duy nhất) và dung dịch X. Dung dịch X có thể hoà tan hết tối đa bao nhiêu gam Cu (biết sản phẩm khử sinh ra là NO2) ?
- nS = 0,15 mol; nHNO3 = 1 mol
S + 6HNO3 → 6NO2 + H2SO4 + 2H2O
0,15 → 0,9 → 0,15
=> dung dịch sau phản ứng gồm H2SO4 0,15 mol và HNO3 0,1 mol
=> nH+ = 0,4 mol; nNO3- = 0,1 mol
- Cu + 4H+ + 2NO3- → Cu2+ + 2NO2 + 2H2O
0,05 ← 0,2 ← 0,1
=> mCu = 3,2 gam
Cho 2 thí nghiệm sau:
Thí nghiệm 1: Cho 6,4 gam Cu phản ứng với 120 ml dung dịch HNO3 1M được a lít NO.
Thí nghiệm 2: Cho 6,4 gam Cu phản ứng với 120 ml dung dịch HNO3 1M và H2SO4 0,5M được b lít NO.
Biết NO là sản phẩm khử duy nhất của N+5. Mối liên hệ giữa a và b là
3Cu + 8H+ + 2NO3- → 3Cu2+ + 2NO + 4H2O
TN1: nCu = 0,1 mol; nHNO3 = 0,12 mol
Xét \(\frac{{{n_{Cu}}}}{3} = \frac{{0,1}}{3};\,\,\,\,\frac{{{n_{{H^ + }}}}}{8} = \frac{{0,12}}{8} = 0,015;\,\,\,\,\frac{{{n_{NO_3^ - }}}}{2} = \frac{{0,12}}{2} = 0,06\)
=> H+ hết, Cu và NO3- dư => phản ứng tính theo H+
nNO (1) = 1/4.nH+ = 1/4.0,12 = 0,03 mol
TN2: nCu = 0,1 mol; nH+ = 0,24 mol; nNO3- = 0,12 mol
Xét \(\frac{{{n_{Cu}}}}{3} = \frac{{0,1}}{3};\,\,\,\,\frac{{{n_{{H^ + }}}}}{8} = \frac{{0,24}}{8} = 0,03;\,\,\,\,\frac{{{n_{NO_3^ - }}}}{2} = \frac{{0,12}}{2} = 0,06\)
=> H+ hết, Cu và NO3- dư => phản ứng tính theo H+
nNO (2) = 1/4.nH+ = 1/4.0,24 = 0,06 mol
=> nNO (2) = 2.nNO (1) => b = 2a
Cho 29 gam hỗn hợp gồm Al, Cu và Ag tác dụng vừa đủ với 950 ml dung dịch HNO3 1,5M, thu được dung dịch chứa m gam muối và 5,6 lít hỗn hợp khí X (đktc) gồm NO và N2O. Tỉ khối của X so với H2 là 16,4. Giá trị của m là
Gọi nNO = a mol; nN2O = b mol => nX = a + b = 0,25 mol (1)
\({\bar M_X} = \frac{{30a + 44b}}{{a + b}} = 16,4.2\) (2)
Từ (1) và (2) => a = 0,2; b = 0,05
Giả sử phản ứng tạo ra NH4NO3 x mol
Bảo toàn e: ne cho = ne nhận = 3.nNO + 8.nN2O + 8.nNH4NO3 = 3.0,2 + 8.0,05 + 8a
=> nNO3 (trong muối) = ne cho = 1 + 8a
Bảo toàn nguyên tố N: nHNO3 = nNO + 2.nN2O + nNO3 (trong muối) + 2.nNH4NO3
=> 1,425 = 0,2 + 2.0,05 + 1 + 8a + 2a => a = 0,0125 mol
=> mmuối = mkim loại + mNO3 (trong muối) + mNH4NO3 = 29 + (1 + 8.0,0125).62 + 0,0125.80 = 98,2 gam
Hòa tan hoàn toàn m gam Al bằng 620 ml dung dịch HNO3 1M vừa đủ thu được hỗn hợp khí X ( gồm hai khí) và dung dịch Y chứa 8m gam muối. Cho dung dịch NaOH dư vào Y thấy có 25,84 gam NaOH phản ứng. Hai khí trong X là cặp khí nào sau đây
Al + 0,62 mol HNO3 → Al(NO3)3 + khí X
Nếu muối chỉ có mAl(NO3)3 = < 8m → muối có cả NH4NO3
Al(NO3)3 + 4NaOH → NaAlO2 + NaNO3 + 2H2O
NH4NO3 + NaOH → NaNO3 + NH3 + H2O
Ta có nNaOH = 0,646 = \(\dfrac{m}{{27}}.4 + \dfrac{{8m - 7,89m}}{{80}}\) → m =4,32 g → Al: 0,16 mol và NH4NO3: 0,006 mol
Al → Al+3 + 3e N+5 +8e → N-3
N+5 + (5-x) e → N+X
Bảo toàn e có 3.nAl = 8nNH4 + (5-x).nN(+x) → 0,48 = 8.0,006 + (5-x).nN(+x)
Bảo toàn N có nN(+x) + 2nNH4NO3 + 3nAl = nHNO3 → nN(+x) = 0,62 – 2.0,006 – 3.0,16 = 0,128
→ x = 1,625
A sai vì cả 2 khí N đều có số oxh > 1,625
B sai vì tạo khí H2
C đúng
D sai vì cả 2 khí đều có số oxh nhỏ hơn 1,625
Cho 21,6 gam bột Mg tan hết trong dung dịch hỗn hợp gồm NaNO3 và NaHSO4 thu được dung dịch X chỉ chứa m gam hỗn hợp muối trung hòa và 5,6 lít hỗn hợp khí Y gồm N2O và H2( tỉ khối của Y so với H2 là 13,6). Giá trị gần nhất của m là
Xét hỗn hợp khí Y có N2O : x mol và H2 : y mol
Có nY = 0,25 = x + y mol
Và mY = MY . nY = 13,6.2.0,25 = 6,8 g = 44x + 2y
Nên x = 0,15 mol và y = 0,1 mol
Xét phản ứng Mg tác dụng với NaNO3 và NaHSO4 thì
4Mg + 10H+ + 2NO3- → 4Mg+2 + 5H2O + N2O
Mg +2H+ → Mg+2 + H2
Ta có 4nN2O + nH2 = 4.0,15 + 0,1 = 0,7 mol < nMg = 0,9 nên phản ứng có tạo ra NH4+ :
4Mg + 10H+ + NO3- → 4Mg+2 + 3H2O + NH4+
nên nNH4+ = (0,9 – 0,7 ) : 4 =0,05 mol
Bảo toàn nguyên tố N có nNaNO3 = 2nN2O + nNH4 =2.0,15 + 0,05 = 0,35 mol
Bảo toàn nguyên tố H có nNaHSO4 = 10nN2O + 2nH2 + 10nNH4 = 10.0,15 + 0,1.2 + 0,05.10 = 2,2 mol
Sau phản ứng dung dịch X thu được có Mg+2 : 0,9 mol; NH4+ : 0,05 mol; Na+ : 2,55 mol và SO42- : 2,2 mol
=> mmuối = mion = 0,9.24 + 0,05.18 + 2,55.23 + 2,2.96 = 292,35
Hòa tan hết 28,16 gam hỗn hợp rắn X gồm Mg, Fe3O4 và FeCO3 vào dung dịch chứa H2SO4 và NaNO3, thu được 4,48 lít (đktc) hỗn hợp khí Y (gồm CO2, NO, N2, H2) có khối lượng 5,14 gam và dung dịch Z chỉ chứa các muối trung hòa. Dung dịch Z phản ứng tối đa với 1,285 mol NaOH, thu được 43,34 gam kết tủa và 0,56 lít khí (đktc). Mặt khác, cho dung dịch Z tác dụng với lượng dư dung dịch BaCl2 thu được 166,595 gam kết tủa. Biết các phản ứng xảy ra hoàn toàn. Phần trăm khối lượng Mg trong X là
Khi cho dung dịch Z tác dụng với BaCl2 dư thì kết tủa thu được là BaSO4
\( \to {n_{BaS{O_4}}} = \dfrac{{166,595}}{{233}} = 0,715\,\,mol\)
Bảo toàn gốc \(SO_4^{2 - } \to {n_{{H_2}S{O_4}}} = 0,715\,\,mol\)
Khi cho Z tác dụng với NaOH vừa đủ thu được khí là NH3
\({n_{N{H_3}}} = \dfrac{{0,56}}{{22,4}} = 0,025\,\,mol \to {n_{NH_4^ + }} = 0,025\,\,mol\)
Bảo toàn điện tích cho dung dịch Z: \(2{n_{M{g^{2 + }}}} + 2{n_{F{e^{2 + }}}} + 3{n_{F{e^{3 + }}}} + {n_{NH_4^ + }} + {n_{N{a^ + }}} = 2{n_{SO_4^{2 - }}}\)
Mà \({n_{NaOH}} = 2{n_{M{g^{2 + }}}} + 2{n_{F{e^{2 + }}}} + 3{n_{F{e^{3 + }}}} + {n_{NH_4^ + }} = 1,285\,\,mol\)
\( \to 1,285 + {n_{N{a^ + }}} = 2.0,715 \to {n_{N{a^ + }}} = 0,145\,\,mol\)
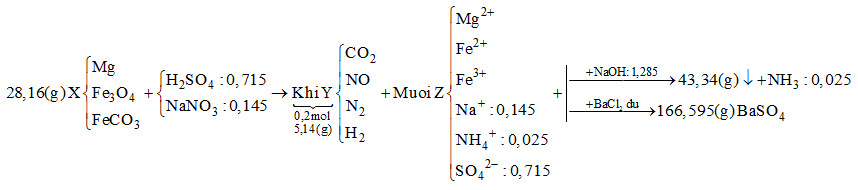
Ta có: \({n_{O{H^ - }\,\,(trong\,\,hidroxit)}} + {n_{NH_4^ + }} = {n_{NaOH}} \to {n_{O{H^ - }\,\,(trong\,\,hidroxit)}} = 1,285 - 0,025 = 1,26\,\,mol\)
Bảo toàn khối lượng: \({m_{Fe}} + {m_{Mg}} + {m_{O{H^ - }\,\,(trong\,\,hidroxit)}} = 43,34 \to {m_{Fe}} + {m_{Mg}} + 1,26.17 = 43,34\)
\( \to {m_{Fe}} + {m_{Mg}} = 21,92g\)
Bảo toàn khối lượng cho dung dịch Z: \({m_{Mg}} + {m_{Fe}} + {m_{Na}} + {m_{NH_4^ + }} + {m_{SO_4^{2 - }}} = 21,92 + 0,145.23 + 0,025.18 + 0,715.96 = 94,345g\)
Bảo toàn khối lượng cho phản ứng: \({m_X} + {m_{{H_2}S{O_4}}} + {m_{NaN{O_3}}} = {m_Z} + {m_Y} + {m_{{H_2}O}}\)
\( \to 28,16 + 0,715.98 + 0,145.85 = 94,345 + 5,14 + {m_{{H_2}O}}\)
\( \to \) \({m_{{H_2}O}} = 14,07g \to {n_{{H_2}O}} = 0,615\,\,mol\)
Bảo toàn nguyên tố H : \(2{n_{{H_2}S{O_4}}} = 2{n_{{H_2}}} + 4{n_{NH_4^ + }} + 2{n_{{H_2}O}}\)
\( \to 2.0,715 = 2{n_{{H_2}}} + 4.0,025 + 2.0,615 \to {n_{{H_2}}} = 0,05\,\,mol\)
Đặt số mol của CO2, NO và N2 lần lượt là x, y, z
\( \to x + y + z + 0,05 = 0,2 \to x + y + z = 0,15\) (*)
Tổng khối lượng Y là 5,14 \( \to 44x + 30y + 28z + 0,05.2 = 5,14\)
\( \to 44x + 30y + 28z = 5,04\) (**)
Bảo toàn nguyên tố N : \({n_{NaN{O_3}}} = {n_{NO}} + 2{n_{{N_2}}} + {n_{NH_4^ + }} \to 0,145 = y + 2z + 0,025\)
\( \to y + 2z = 0,12\) (***)
Từ (*), (**) và (***) \( \to \) x = 0,04; y = 0,01; z = 0,04
\( \to {n_{FeC{O_3}}} = 0,04\,\,mol\)
Gọi số mol của Mg và Fe3O4 lần lượt là a và b
\( \to 24a + 232b + 116.0,04 = 28,16 \to 24a + 232b = 23,52\) (1)
Vì tổng khối lượng của Mg và Fe trong hỗn hợp X là 21,92g
\( \to 24a + 56.(3b + 0,04) = 21,92 \to 24a + 168b = 19,68\) (2)
Từ (1) và (2) \( \to \) a = 0,4; b = 0,06
\( \to \% {m_{Mg}} = \dfrac{{0.4.24}}{{28,16}}.100\% = 34,09\% \)
Dung dịch X chứa 0,2 mol Fe(NO3)3 và 0,24 mol HCl. Dung dịch X có thể hòa tan được tối đa bao nhiêu gam Cu (biết phản ứng tạo khí NO là sản phẩm khử duy nhất)
PT ion rút gọn: 3Cu + 8H+ + 2NO3- → 3Cu2+ + 2NO↑ + 4H2O
ban đầu: 0,24 0,6 (mol)
pư: 0,09←0,24 →0,06 (mol)
sau: 0,09 0,54 (mol)
PT ion rút gọn: Cu + 2Fe3+ → Cu2+ + 2Fe2+
0,1 ← 0,2 (mol)
=> ∑ nCu = 0,09 + 0,1 = 0,19 (mol)
=> mCu = 0,19.64 = 12,16 (g)
Cho hỗn hợp X chứa 18,6 gam gồm Fe, Al, Mg, FeO, Fe3O4 và CuO. Hòa tan hết trong dung dịch HNO3 dư thấy có 0,98 mol HNO3 tham gia phản ứng thu được 68,88 gam muối và 2,24 lít (đktc) khí NO duy nhất. Mặt khác, từ hỗn hợp X ta có thể điều chế được tối đa m gam kim loại. Giá trị của m là
X + HNO3 → Muối + NO + H2O
BTKL: mH2O = mX + mHNO3 - m muối - mNO = 18,6 + 0,98.63 - 68,88 - 0,1.30 = 8,46 gam
=> nH2O = 0,47 mol
BTNT "H": nHNO3 = 4nNH4+ + 2nH2O => 0,98 = 4nNH4+ + 2.0,47 => nNH4+ = 0,01 mol
BTNT "N": nHNO3 = nNO3- + nNH4+ + nNO => 0,98 = nNO3- + 0,01 + 0,1 => nNO3- = 0,87 mol
BTNT "O": nO(X) + 3nHNO3 = 3nNO3- + nNO + nH2O
=> nO(X) + 3.0,98 = 3.0,87 + 0,1 + 0,47 => nO(X) = 0,24 mol
=> m = mKL = mX - mO(X) = 18,6 - 0,24.16 = 14,76 gam

