Đề bài
Hỗn hợp X chứa ba chất hữụ cơ đồng phân. Nếu làm bay hơi 2,10 g X thì thể tích hơi thu được bằng thể tích của 1,54 g khí CO2 ở cùng điều kiện. Để đốt cháy hoàn toàn 1,50 g X cần dùng vừa hết 2,52 lít O2 (đktc). Sản phẩm cháy chỉ có CO2 và H2O theo tỉ lệ 11 : 6 về khối lượng.
1. Xác định công thức phân tử của ba chất trong X.
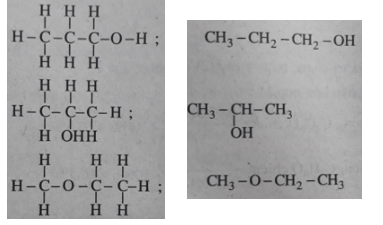
2. Dựa vào thuyết cấu tạo hoá học, hãy viết công thức cấu tạo (triển khai và rút gọn) của từng chất đó.
Phương pháp giải - Xem chi tiết
1. +) Áp dụng định luật bảo toàn khối lượng \({m_{C{O_2}}} + {m_{{H_2}O}} = {m_X} + {m_{{O_2}}}\)
+) Mặt khác, CO2 và H2O theo tỉ lệ 11 : 6 về khối lượng => \({m_{C{O_2}}}\) và \({m_{{H_2}O}}\)
+) Tính khối lượng các nguyên tố trong X (chú ý sự có mặt của O)
+) Tìm CTĐGN của X
+) Tính phân tử khối của X => CTPT
+) Viết các CTCT của các chất trong X
Lời giải chi tiết
Ba chất đồng phân có công thức phân tử giống nhau. Đốt X ta chỉ được CO2 và H2O, vậy các chất trong X có chứa C, H và có thể có chứa O.
Theo định luật bảo toàn khối lượng :
\({m_{C{O_2}}} + {m_{{H_2}O}} = {m_X} + {m_{{O_2}}} = 1,5 + \dfrac{{2,52}}{{22,4}}\times32 = 5,1(g)\)
Mặt khác \({m_{C{O_2}}}:{m_{{H_2}O}}\) =11:6
Từ đó tìm được : \({m_{C{O_2}}}\) = 3,30 g và \({m_{{H_2}O}}\) = 1,80 g
Khối lượng C trong 3,30 g CO2: \(\dfrac{{12\times3,3}}{{44}}\) = 0,9 (g).
Khối lượng H trong 1,80 g H2O : \(\dfrac{{2\times1,8}}{{18}}\) =0,2 (g)
Khối lượng O trong 1,50 g X : 1,50 - 0,9 - 0,2 = 0,4 (g).
Các chất trong X có dạng CxHyOz
x : y : z = \(\dfrac{{0,9}}{{12}}:\dfrac{{0,2}}{1}:\dfrac{{0,4}}{{16}}\) = 0,075 : 0,2 : 0,025 = 3 : 8 : 1.
Công thức đơn giản nhất là \({C_3}{H_8}O\).
\({M_{\rm{x}}} = \dfrac{{2,1\times44}}{{1,54}} = 60(g/mol) \Rightarrow \) CTPT cũng là \({C_3}{H_8}O\).
Các CTCT: