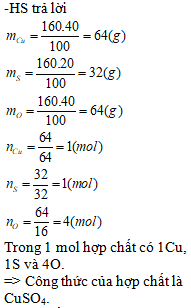Ngày soạn:
Bài 21.TÍNH THEO CÔNG THỨC HOÁ HỌC (T1)
I. MỤC TIÊU:
1. Kiến thức:
- Các bước tính thành phần phần trăm về khối lượng mỗi nguyên tố trong hợp chất khi biết CTHH .
- Ý nghĩa của CTHH cụ thể theo số mol, theo khối lương hoặc theo thể tích. .
2. Kĩ năng:
- Tính được tỉ lệ số mol, tỉ lệ khối lượng các nguyên tố, giữa các nguyên tố và hợp chất.
- Tính theo thành phần phần trăm về khối lượng của các nguyên tố khi biết CTHH của một số hợp chất và ngược lại.
- Xác định được CTHH của hợp chất khi biết thành phần phần trăm về khối lượng các nguyên tố tạo ra chất.
3. Thái độ:Gây hứng thú học tập bộ môn , tính cẩn thận , khoa học , chính xác
II. CHUẨN BỊ CỦA GIÁO VIÊN VÀ HỌC SINH
1. Chuẩn bị của GV:Bảng phụ, Phiếu học tập
2. Chuẩn bị của HS: Ôn tập các phần kiến thức : CTHH, NTK , PTK , Mol …
III. Phương pháp: Hoạt động nhóm, vấn đáp, làm bài tập , tư duy logic...
IV. TIẾN TRÌNH BÀIDẠY
1. Kiểm tra bài cũ:


3. Củng cố, luyện tập
- Các bước tính thành phần phần trăm về khối lượng mỗi nguyên tố trong hợp chất.
4. Hướng dẫn học sinh tự học ở nhà:
- Về nhà học bài.
- Làm bài tập 1 SGK/71.
5. Phần bổ sung của đồng nghiệp hoặc cá nhân
Ngày soạn:
Bài 21.TÍNH THEO CÔNG THỨC HOÁ HỌC (T2)
I. MỤC TIÊU:
1. Kiến thức:
- Các bước lập CTHH khi biết thành phần phần trăm về khối lượng của các nguyên tố trong hợp chất .
- Ý nghĩa của CTHH cụ thể theo số mol, theo khối lương hoặc theo thể tích. .
2. Kĩ năng:
- Tính được tỉ lệ số mol, tỉ lệ khối lượng các nguyên tố, giữa các nguyên tố và hợp chất.
- Tính theo thành phần phần trăm về khối lượng của các nguyên tố khi biết CTHH của một số hợp chất và ngược lại.
- Xác định được CTHH của hợp chất khi biết thành phần phần trăm về khối lượng các nguyên tố tạo ra chất.
3. Thái độ: Hình thành được tính cẩn thận , chính xác và ham thích bộ môn hoá học .
II. CHUẨN BỊ CỦA GIÁO VIÊN VÀ HỌC SINH
1. Chuẩn bị của GV: Bảng phụ,Phiếu học tập.
2. Chuẩn bị của HS:Học lại kiến thức cũ.
III. Phương pháp: Hoạt động nhóm, vấn đáp, làm bài tập, tư duy logic...
IV. TIẾN TRÌNHBÀI DẠY
1. Kiểm tra bài cũ: HS1, 2: Làm bài tập 1.a.
2. Bài mới: Giới thiệu bài: Từ CTHH ta có thể xác định được % về khối lượng của các nguyên tố trong hợp chất. Vậy, từ thành phần phần trăm các nguyên tố trong hợp chất làm sao có thể lập CTHH?
|
Hoạt động của GV |
Hoạt động của HS |
Nội dung ghi bảng |
|
Hoạt động 1. Lập CTHH của hợp chất khi biết % nguyên tố trong hợp chất(10’) |
||
|
-GV: Một hợp chất có thành phần các nguyên tố là 40% Cu ; 20% S và 40% O . Hãy xác định công thức hoá học của hợp chất ( biết khối lượng mol là 160g ). -GV: Hướng dẫn: +B1: Tìm khối lượng của Cu , S , O trong 1 mol hợp chất. +B2: Tìm số mol nguyên tửcủa Cu , S , Otrong hợp chất. - Dựa vào công thức nào để tính số mol nguyên tử của các nguyên tố ? +B3: Viết công thức hoá học của hợp chất ? -GV: Cho HS nhắc lại các bước xác định công thức hoá học của hợp chất ? |
- HS: Theo dõi, suy nghĩ cách thực hiện bài tập. -HS trả lời
Trong 1 mol hợp chất có 1Cu, 1S và 4O. => Công thức của hợp chất là CuSO4. -HS: Nhắc lại các bước lập CTHH khi biết % các nguyên tố trong hợp chất. |
II. Biết thanøh phần các nguyên tố, hãy xác định công thức hoá học của hợp chất: - Tìm khối lượng của mỗi nguyên tố trong 1 mol hợp chất. - Tìm số mol nguyên tử của mỗi nguyên tố có trong 1 mol hợp chất . - Lập công thức hoá học của hợp chất. |
|
Hoạt động 2.Luyện tập. |
||
|
Bài 1: Hợp chất A có thành phần các nguyên tố là : 28,57% Mg , 14,2 % C , còn lại là oxi . Biết khối lượng mol của hợp chất A là 84 . Hãy xác định công thức hoá học của hợp chất. -GV: Hướng dẫn và gọi HS làm từng bước: + Tính %O. + Tính khối lượng Mg, C và O. + Tinh n của Mg, C, O. + Từ số mol lập CTHH. Bài 2: Hợp chất A ở thể khí có thành phần các nguyên tố là : 80% C , 20% H . Biết tỉ khối của khí A so vớihiđro là 15 . Xác định công thức hoá học của khí A. -GV: Hướng dẫn các bước tiến hành bài tập |
-HS: Suy nghĩ cách làm bài tập:
|
|
3. Củng cố, luyện tập :
GV yêu cầu HS làm bài tập 2.a SGK/71.
4. Hướng dẫn học sinh tự học ở nhà
GV yêu cầu HS về nhà làm bài tập 2. b, 3, 4, 5 SGK/71.
Chuẩn bị bài: “Tình theo phương trình hoá học”.
5. Phần bổ sung của đồng nghiệp hoặc cá nhân.