Ngày soạn:
BÀI 10. HOÁ TRỊ(T1)
I. MỤC TIÊU:Sau bài này HS phải:
1. Kiến thức :
- Hoá trị biểu thị khả năng liên kết của nguyên tử nguyên tố này với nguyên tử nguyên tố khác hay với nhóm nguyên tử khác.
- Quy ước: Hóa trị của H là I, hóa trị của O là II; Hóa trị của một nguyên tố trong hợp chất cụ thể được xác định theo hóa trị của H và O.
2. Kỹ năng :Tính hoá trị của một nguyên tố hoặc nhóm nguyên tử theo CTHH cụ thể
3. Thái độ :Giúp HS yêu thích môn học để học tập tốt hơn .
II. CHUẨN BỊ CỦA GIÁO VIÊN VÀ HỌC SINH CỦA GIÁO VIÊN VÀ HỌC SINH :
1. Chuẩn bị của GV:Bảng 1,2 trang 42 ,43 SGK
2. Chuẩn bị của HS:Thuộc KHHH của một số nguyên tố ở bảng 1 trang 42 . Xem lại cấu tạo nguyên tử .
III. PHƯƠNG PHÁP: Đàm thoại gợi mở, vấn đáp, quan sát, giải thích, làm bài tập..
IV. TIẾN TRÌNH DẠY HỌC :
1. Kiểm tra bài cũ:
Câu 1: Cho các công thức hoá học sau:
a. Clo Cl2;
b. Axit sunfuric H2SO4.
Hãy nêu những gì biết được về các CTHH trên.
Câu 2: Viết CTHH của hợp chất sau:
a. Amoniac, tạo bởi 1N và 3H.
b. Đồng sunfat, tạo bởi 1Cu, 1S và 4O.
Đáp án:
|
Câu |
Đáp án chi tiết |
Thang điểm |
|
Câu 1 Câu 2 |
a.Cl2: - Có 1 nguyên tố: Cl. - Có 2Cl. - PTK = 2.35,5 = 71đvC b. H2SO4: - Có 3 nguyên tố: H, S, O. - Có 2H, 1S và 4O. -PTK = 2.1 + 1.32 + 4.16 =98đvC. a. NH3. b. CuSO4. |
3 ý đúng * 1đ = 3đ. 3 ý đúng * 1đ = 3đ. 2đ 2đ |
2. Bài mới :
a. Giới thiệu bài:Nguyên tử có khả năng liên kết với nhau. Hoá trị là con số biểu thị khả năng đó. Vậy, hoá trị là gì? Cách xác định hoá trị ra sao?Chúng ta cùng tìm hiểu bài học hôm nay.
b. Các hoạt động
Hoạt động của GV |
Hoạt động của HS |
Nội dung ghi bảng |
|
Hoạt động 1: Tìm hiểu cách xác định hoá trị một nguyên tố như thế nào? |
||
|
- GV: Quy ước H hoá trị I. - GV: Lấy ví dụ chứng minh H có hoá trị I. - GV khẳng định : Căn cứ vào số nguyên tử H liên kết với 1 nguyên tử của nguyên tố khác -> Hoá trị của nguyên tố đó . - GV: Dựa vào khả năng liên kết của O => O hoá trị II. -GV: Hướng dẫn HS lấy ví dụ. -GV: Hướng dẫn cách xác định hoá trị của nhóm nguyên tử dựa vào khả năng liên kết của chúng |
-HS: Ghi vở. -HS: Lấy ví dụ theo hướng dẫn của GV. -HS: Lắng nghe và ghinhớ. -HS :Theo dõi và ghi vở. -HS: Lấy ví dụ. -HS: Theo dõi, lấy ví dụ cùng GV và ghi vở. |
I- Hóa trị của một nguyên tố đượcxác định bằng cách nào? - H có hoá trị I-> nguyên tử của nguyên tố khác liên kết được với bao nhiêu H thì nguyên tố đó có hoá trị bấy nhiêu. + HCl (Axitclohiđric)-> Cl(I). + NH3 (Amoniăc) -> N(III). - O có hoá trịII. +Na2O -> Na hoá trị I. + CaO -> Cahoá trị II. - Xác định hoá trị của nhóm nguyên tử cũng tương tự. |
|
Hoạt động 2: Kết luận |
||
|
-GV hỏi:Cl(I), O(II), S(II), SO4(II)… => Hoá trị là gì? -GV hỏi: Hoá trịđược xác định bằng cách nào ? Cách ghi hoá trị? -GV: Hướng dẫn cách tra cứu bảng 1,2 SGK/42 , 43. |
-HS: Trả lời. -HS: Xác định theo hoá trị của H vàO. Hoá trị được ghi bắng số La Mã. -HS: Tra bảng hoá trị theo hướng dẫn của GV. |
2- Kết luận : - Hoá trịlà con số biểu thị khả năng liên kết của nguyên tử nguyên tố này với nguyên tử nguyên tố khác . - Hoá của H là I và O là II. - Hoá trị đượcghi bằng số La Mã. |
|
Hoạt động 3: Tìm hiểu quy tắc hoá trị |
||
|
- GV: Gọia, b là hóa trị của A, B - GV: Đưa ra công thức hoá trị. - GV: YC HS rút ra quy tắc. - GV: Cho HS làm BT BT: Ap dụng quy tắc hoá trị hãy xác định đối với các chất sau: Ca(OH)2, Ca(OH)2CO2. - GV: NX và bổ sung (nếu có ) - GV: Quy tắc chỉ vận dụng chủ yếu cho các hợp chất vô cơ. |
- HS: Lắng nghe - HS: Lắng nghe. - HS: Trả lời . - HS: Làm BT. - HS: Lắng nghe. - HS: Lắng nghe. |
II- QUY TẮC HOÁ TRỊ : 1- Qui tắc : A,B : là kí hiệu hoá học của nguyên tố. x.a = y.b Tích của chỉ số và hoá trị của nguyên tố này bằng tích của chỉ số và hoá trị của nguyên tố kia . +Ca(OH)2 1 xII= 2 x I +CO21 xIV = 2xII +FeO1xII= 1x II |
3. Củng cố, luyện tập :
Hãy xác định hoá trị của (P, Ca) trog hợp chất sau: P2O5, CaCO3.
Áp dụng quy tắc hoá trị cho 2 công thức hoá học trên.
4. Hướng dẫn học sinh tự học ở nhà :
- Học thuộc hoá trị của một số nguyên tố , nhóm nguyên tử trong bảng 1,2 trang 42, 43.
- Làm BT 1, 2, 3a, 4a SGK/ 37, 38.
- Chuẩn bị bài : Hoá trị (T2).
5. Phần bổ sung của đồng nghiệp hoặc cá nhân
Ngày soạn :
BÀI 10: HOÁ TRỊ (T2 )
I. MỤC TIÊU:Sau bài này HS phải:
1. Kiến thức: Quy tắc hóa trị: Trong hợp chất 2 nguyên tố AxBy thì a.x=b.y (a, b là hóa trị tương ứng của A,B ( Quy tắc hóa trị đúng với cả khi A hay B là nhóm nguyên tử)
2.Kỹ năng :
- Tính hoá trị của một nguyên tố hoặc nhóm nguyên tử theo CTHH cụ thể
- Lập được CTHH của hợp chất khi biết hóa trị của hai nguyên tố hóa học hoặc nguyên tố và nhóm nguyên tử tạo nên chất.
3. Thái độ: Cẩn thận, chính xác, có ý thức học tập nghiêm túc.
II. CHUẨN BỊ CỦA GIÁO VIÊN VÀ HỌC SINH CỦA GIÁO VIÊN VÀ HỌC SINH :
1. Chuẩn bị của GV :Bảng 1,2 trang 42 ,43 SGK .
2. Chuẩn bị của HS : Thuộc hoá trị của một số nguyên tố ở bảng /SGK 42 ,43.
III. PHƯƠNG PHÁP: Đàm thoại gợi mở, vấn đáp, quan sát, giải thích, làm bài tập..
IV. TIẾN TRÌNH DẠY HỌC:
1. Kiểm tra bài cũ:
Hoá trị là gì? Hãy nêu quy tắc hoá trị?
2. Bài mới:
a. Giới thiệu bài : Nguyên tử có khả năng liên kết với nhau. Hoá tri là con số biểu thị khả năng đó. Biết được hoá trị ta sẽ hiểu và viết đúng cũng như lập đượccông thức hoá học của hợp chất.
b. Các hoạt động
Hoạt động của GV |
Hoạt động của HS |
Nội dung ghi bảng |
|
Hoạt động 1. Tìm hiểu cách tính hoá trị của một nguyên tố |
||
|
- GV: Hướng dẫn HS cách tính hoá trị của Fe trong hợp chất FeCl3 . - GV: Yêu cầu HS xác định hoá trị của C trong hợp chất CO2. - GV: Hướng dẫn các bước tương tự như tính hoá trị của Fe - GV: Nhận xét và bổ sung |
- HS: Thực hiện các bước theo hướng dẫn của GV. - HS: Ghi đề bài tập. - HS: Làm BT
HS: Làm bài tập vào vở. |
II- QUY TẮC HOÁ TRỊ : 2. Vận dụng : a. Tính hoá trị của một nguyên tố: Ví dụ: Tính hoá trị của Fe trong hợp chất FeCl3, Cl(I) Bg: Gọi hoá trị của Fe là a 1.a = 3. I
-> Fe là hoá trị III |
|
Hoạt động 2. Lập công thức hoá học của hợp chất theo hoá trị |
||
|
- GV: Hướng dẫn HS lập công thức hoá học của hợp chất tạo bởi nitơ IV và oxi. 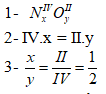 =>x, y => công thức đúng. -GV : Dựa vào VD hãy nêucác bước giải - GV: Nhận xét - GV: Lập công thức hoá học của hợp chất gồm : *Nhôm (III) và nhóm SO4(II) - GV:Cho HS lên bảng sữa. - GV: Nhận xét - GV: Lưu ý một số vấn đề + Nếu a=b thì x=y=1 + Nếu a khác b và tỉ lệ a: b ( tối giản) thì x=b, y=a + Nếu a: b chưa tối giản thì giản ước để có a’: b’và lấy x=b’ , y=a’. |
- HS: Theo dõi và thực hiện theo các bước GV hướng dẫn: +Gọi CTTQ: +Ap dụng quy tắc hoá trị: a.x = b.y -> IV. x= II . y. => =>Công thức đúng : NO2 - HS: Nêu các bước giải. -HS: Ghi vở. - HS: Làm BT vào vở. - HS: Sữa BT 1Gọi CTTQ: 2.Ap dụng QTHT: III.x = II.y 3. 4.Vậy công thức : Al2(SO4)3 - HS:Sữa bài vào vở. - HS : Lắng nghe và ghi vở. |
b.Lập công thức hoa học của hợp chất theo hoá trị : Ví dụ : Lập công thức hoá học của hợp chất tạo bởi nitơ IV và oxi 1- Gọi CTTQ: 2- Áp dụng QTHT:a.x = b.y => IV. x= II . y => =>Công thức cần lập : NO2. * Các bước lập công thức hoá học 1- Gọi CTTQ: 2-Ap dụng QTHT: a.x = b.y 3- Lập tỷ lệ: =>x, y => CT đúng cần tìm. |
3. Củng cố, luyện tập:
Lập CTHH của hợp chất tạo bởi:
a. Canxi(II) và oxi(II).
b. Canxi (II) và PO4(III).
c. Lưu huỳnh(IV) và oxi(II).
4. Hướng dẫn học sinh tự học ở nhà:
Làm bài tập 5,6,7,8 SGK/ 38.
Dặn các em ôn tập lại kiến thức chuẩn bị luyện tập.
5. Phần bổ sung của đồng nghiệp hoặc cá nhân

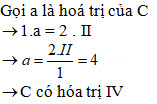
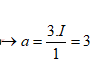
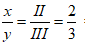 =>x = 2 , y = 3
=>x = 2 , y = 3