I. NGUYÊN TẮC ĐIỀU CHẾ KIM LOẠI
Khử ion kim loại thành nguyên tử.
Mn+ + ne → M
I CÁC PHƯƠNG PHÁP ĐIỀU CHẾ KIM LOẠI
1. Phương pháp nhiệt luyện
- Đối tượng KL: KL có mức độ hoạt động trung bình
- Phương thức điều chế: khử ion kim loại trong hợp chất ở nhiệt độ cao bằng các chất khử thông thường như C, CO, H2, Al.
VD:
Fe2O3 + 3 CO to→to→ 2Fe + 3CO2
2. Phương pháp thủy luyện
- Đối tượng KL: KL có mức độ hoạt động trung bình và yếu
- Phương thức điều chế: Khử những in kim loại cần điều chế bằng những kim loại có tính khử mạnh như Fe, Zn,....
VD:
Fe + CuSO4 → FeSO4 + Cu
3. Phương pháp điện phân
a) Điện phân nóng chảy:
- Đối tượng KL: KL có mức độ hoạt động mạnh
- Phương thức điều chế: Dùng dòng điện một chiều khử ion kim loại trong chất điện li nóng chảy (muối halogenua, oxit, hidroxit).
Ví dụ: Điện phân MgCl2 nóng chảy để điều chế Mg.
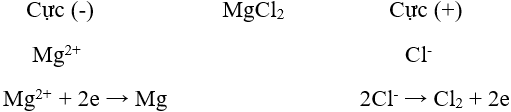
Phương trình điện phân
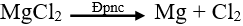
b) Điện phân dung dịch:
- Đối tượng KL: Dùng điều chế các kim loại yếu.
- Phương thức điều chế: Dùng dòng điện một chiều khử ion kim loại yếu trong dung dịch muối của nó.
Ví dụ: Điện phân dung dịch CuCl2 để điều chế kim loại Cu.
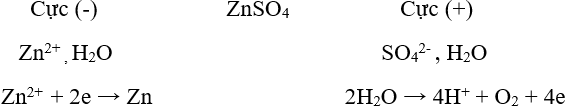
Phương trình điện phân
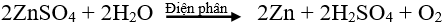
Video mô phỏng - Quá trình điện phân muối ăn NaCl
c) Tính lượng chất thu được ở các điện cực
- Dựa vào công thức Farađây:
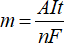
- Trong đó:
m: Khối lượng chất thu được ở điện cực (g).
A: Khối lượng mol nguyên tử của chất thu được ở điện cực.
n: Số electron mà nguyên tử hoặc ion đã cho hoặc nhận.
I: Cường độ dòng điện (ampe).
t: Thời gian điện phân (giây).
F: Hằng số Farađây (F = 96500).
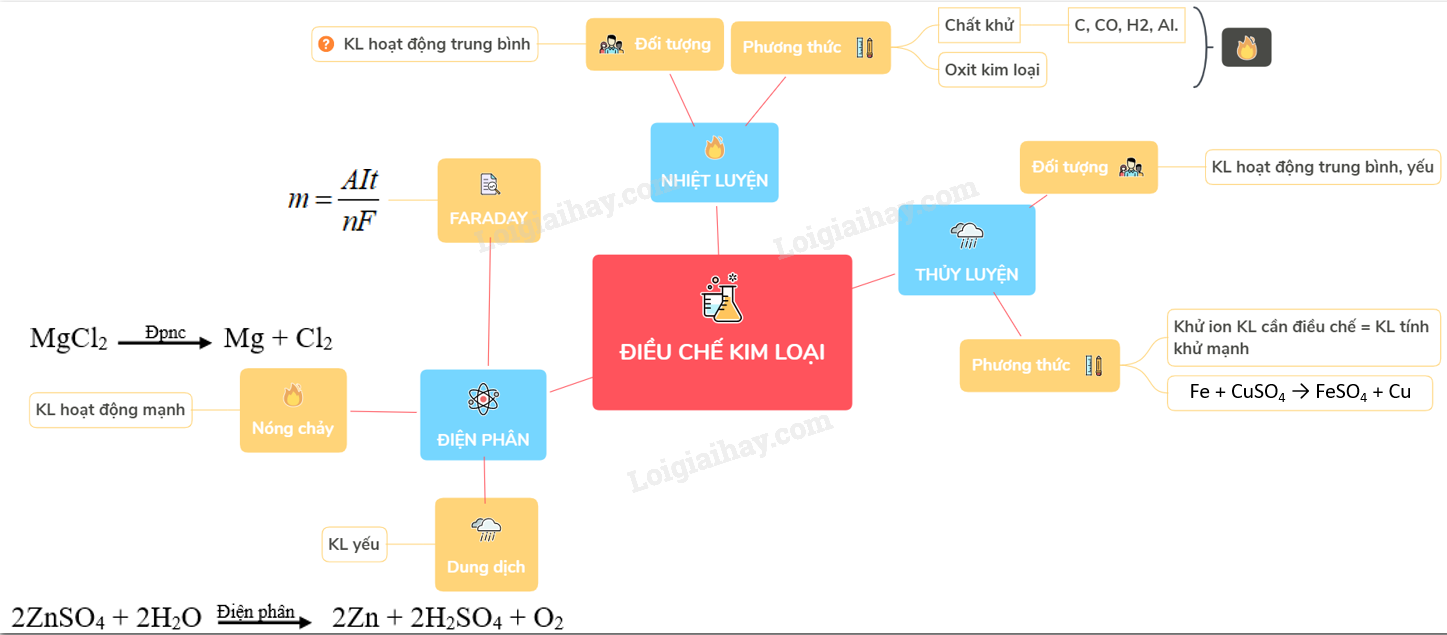
Sơ đồ tư duy: Điều chế kim loại