I. ĐỊNH NGHĨA, ĐỒNG PHÂN, DANH PHÁP
1. Định nghĩa
VD: CH3COOH + C2H5OH ⇆ CH3COOC2H5 + H2O
=>ĐN: Khi ta thay thế nhóm (-OH) trong phân tử axit bằng gốc (-OR') thì thu được este
RCOOH → R - COOR' (R' ≠ H)
Chú ý:Cách viết khác của este
R - COO - R' hoặc R' - OOC - R hoặc R' - OCO - R (R'≠ H)
R là gốc xuất phát từ axit, còn R' là gốc xuất phát từ ancol
* Công thức của este đa chức
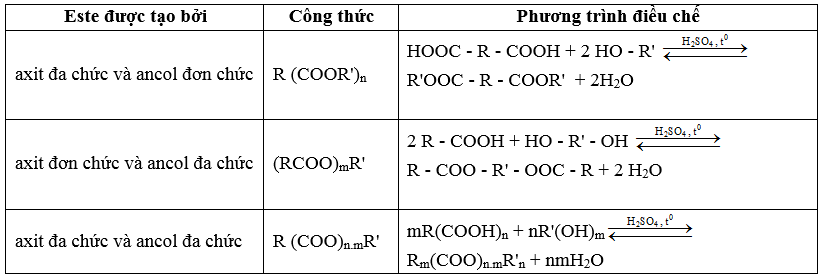
2. Đồng phân
- Đồng phân của este no, đơn chức, mạch hở: RCOOR’ hoặc CnH2nO2 (n≥ 2)
- Cách viết đồng phân este:
Bước 1: Tính k (tổng số liên kết π và vòng trong phân tử), tìm số liên kết π trong gốc hidrocacbon.
Bước 2: Viết các đồng phân của este fomat HCOOR’ (R’ mạch không nhánh, có nhánh).
Bước 3: Thực hiện chuyển lần lượt 1 cacbon từ gốc R’ sang gốc R cho đến khi R’ chỉ còn 1 cacbon thì dừng lại.
VD:Viết đồng phân của este có CTPT sau: C4H8O2
Bước 1: k =\frac{{2 + 2.4 - 8}}{2} = 1. Vì este đơn chức có 1 liên kết π trong nhóm COO nên gốc R và R’ đều là gốc hidrocacbon no.
Bước 2: Viết đồng phân este trên theo thứ tự như sau:
1. H - COO - CH2 - CH2 - CH3
2. H - COO - CH (CH3) - CH3
3. CH3 - COO - CH2 - CH3
4. CH3 - CH2 - COO - CH3
Bước 3: Ta thấy ở đồng phân thứ 4: R’ chỉ còn 1C nên đã là đồng phân cuối cùng, nếu tiếp tục chuyển 1C qua R thì R’ trùng H (axit cacboxylic)
Chú ý:
-Công thức tính nhanh số đồng phân este no, đơn chức CnH2nO2 : 2n-2(2< n< 5)
- Phân biệt đồng phân (tính cả đồng phân hình học) ≠ đồng phân cấu tạo (không tính đồng phân hình học)
- Ứng với công thức CnH2nO2 có các loại đồng phân mạch hở sau:
+) Axit no, đơn chức: C2H5COOH
+) Este no, đơn chức: CH3COOCH3
+) Anđehit – rượu: HO – CH2 – CH2 – CHO
+) Xeton – rượu: CH3 – CO – CH2OH
+) Anđehit – ete: CH3 – O – CH2 – CHO
+) Xeton – ete: CH3 – O – CH2 – CO – CH3
3. Danh pháp: R - COO - R'
a. Nếu ancol đơn chức R’OH:
Tên este = tên gốc hidrocacbon R’+ tên gốc axit ("ic" → "at")
VD:
CH3COOC2H5: etyl axetat
CH2=CH-COO-CH3: metyl acrylat
H-COO-CH(CH3)-CH3 iso propyl fomat
b. Nếu ancol đa chức:
Tên este = tên ancol + tên gốc axit ("ic" → "at")
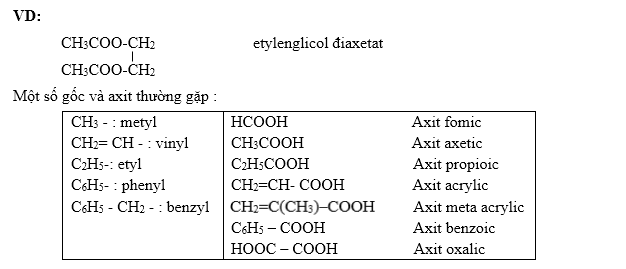
II. TÍNH CHẤT VẬT LÝ
1. Trạng thái: Đa số ở trạng thái lỏng. Những este có KLPT rất lớn có thể ở trạng thái rắn ( như mỡ động vật, sáp ong …)
2.Nhiệt độ sôi: Thấp, dễ bay hơi do không tạo liên kết hidro giữa các phân tử.
3.Tính tan: Ít tan hoặc không tan trong nước do không tạo liên kết hidro giữa các phân tử với nước.
4. Đa số các este có mùi thơm đặc trưng:
- Isoamyl axetat: CH3COOCH2CH2CH(CH3)2: mùi chuối
- Etyl butirat: CH3CH2CH2COOC2H5: mùi dứa
- Geranyl axetat: CH3COOC10H17: mùi hoa hồng…

