1. Nếu sục CO2 dư vào dung dịch [Al(OH)4]- chỉ xảy ra phản ứng:
[Al(OH)4]- + CO2 → Al(OH)3 + HCO3-
Nếu ${{n}_{{{\left[ Al{{\left( OH \right)}_{4}} \right]}^{-}}}}=\text{ }a$ thì ${{n}_{C{{O}_{2}}}}$phản ứng $=~{{n}_{Al{{\left( OH \right)}_{3}}}}=\text{ }a$
* Kết tủa không bị hòa tan khi sục CO2 dư
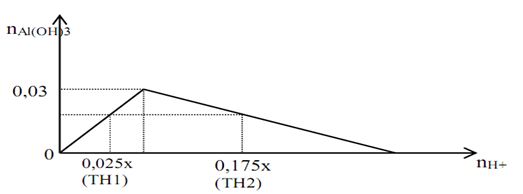
2. Nếu cho H+ tác dụng với dung dịch [Al(OH)4]- thì xảy ra 1 hoặc 2 phản ứng sau:
[Al(OH)4]- + H+ → Al(OH)3 + H2O (1)
Al(OH)3 + 3H+ → Al3+ + 3H2O (2)
*Phương pháp: Nếu đặt: n[Al(OH)4]- = a mol; nH+ = b mol thì:
+ Nếu b $\le $ a thì ${{n}_{Al{{\left( OH \right)}_{3}}}}=\text{ }b$
+ Nếu a < b < 4a thì kết tủa bị hoà tan 1 phần và ${{n}_{Al{{\left( OH \right)}_{3}}}}=\text{ }\frac{4a-b}{3}$
+ Nếu b$\ge $ 4a thì không có kết tủa
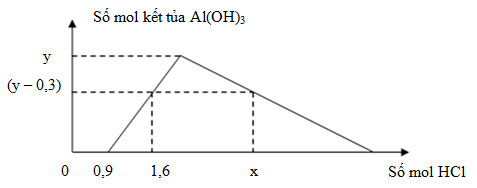
3. Nếu biết ${{\mathbf{n}}_{\mathbf{Al}{{\left( \mathbf{OH} \right)}_{\mathbf{3}}}}}=\text{ }\mathbf{b}\text{ }<\text{ }{{\mathbf{n}}_{{{\left[ \mathbf{Al}{{\left( \mathbf{OH} \right)}_{\mathbf{4}}} \right]}^{-}}}}=\text{ }\mathbf{a}.$ Tính số mol H+
* Phương pháp: Có 2 khả năng xảy ra:
+ Khả năng thứ 1: Nếu [Al(OH)4]- dư chỉ xảy ra phản ứng:
[Al(OH)4]- + H+ → Al(OH)3 + H2O (1)
b b
$=>{{\mathbf{n}}_{{{\mathbf{H}}^{+}}\text{ }\mathbf{min}}}=\text{ }\mathbf{b}$
+ Khả năng thứ 2: Nếu [Al(OH)4]- hết xảy ra 2 phản ứng
[Al(OH)4]- + H+ → Al(OH)3 + H2O (1)
a a a
Al(OH)3 + 3H+ → Al3+ + 3H2O (2)
a – b 3(a – b)
$=>{{n}_{{{H}^{+}}}}=\text{ }4a-3b$
+ Nếu đề bài yêu cầu tính nH+ min thì nH+ = b
+ Nếu đề bài yêu cầu tính nH+ max thì nH+ = 4a – 3b
+ Nếu đề bài chỉ yêu cầu tính nH+ thì phải lấy nghiệm cả 2 trường hợp trên