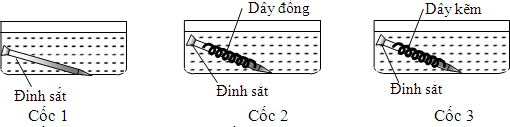
1. Khái niệm
- Ăn mòn kim loại là sự phá hủy kim loại hoặc hợp kim do tác dụng của các chất trong môi trường
- Kim loại bị ăn mòn là kim loại bị oxi hóa thành ion dương (M → Mn+ + ne), làm mất đi tính chất vật lí và hóa học của nó.
- Căn cứ vào môi trường và cơ chế cảu sự ăn mòn, người ta chia thành 2 loại: ăn mòn điện hóa và ăn mòn hóa học
2. Các dạng ăn mòn kim loại
|
Sự ăn mòn hóa học |
Sự ăn mòn điện hóa học |
|
|
Điều kiện xảy ra ăn mòn |
+ Kim loại tinh khiết + Khô |
- Có 2 điện cực khác nhau về bản chất + Cặp kim loại A – kim loại B (Trong đó kim loại có thế điện cực chuẩn nhỏ hơn sẽ là cực âm.) + Cặp kim loại – Cacbon - 2 điện cực tiếp xúc (trực tiếp hoặc gián tiếp qua dây dẫn) - 2 điện cực nhúng vào cùng 1 dd chất điện li |
|
Cơ chế của sự ăn mòn |
Thiết bị bằng Fe tiếp xúc với hơi nước, khí oxi thường xảy ra phản ứng: |
- Sự ăn mòn điện hóa một vật bằng gang (hợp kim Fe – C hoặc thép) trong môi trường không khí ẩm có hòa tan khí CO2, SO2, O2... sẽ tạo ra một lớp dung dịch điện li phủ bên ngoài kim loại. O2 + 2H2O + 4e → 4OH- |
|
Bản chất của sự ăn mòn |
Là quá trình oxi hóa - khử mà kim loại nhường trực tiếp e cho chất ăn mòn (môi trường) => không có dòng điện, ăn mòn xảy ra chậm |
Quá trình oxi hóa khử mà kim loại bị ăn mòn bởi dd chất điện li => Xuất hiện dòng điện |
3. Chống ăn mòn kim loại
a. Phương pháp bảo vệ bề mặt (cách li)
- Phủ lên bề mặt kim loại một lớp sơn, dầu mỡ, chất dẻo hoặc tráng, mạ bằng một kim loại khác che kín toàn bộ bề mặt kim loại
Ví dụ: các đồ vật làm bằng sắt thường được phủ 1 lớp sơn chống gỉ.
b. Phương pháp điện hóa
- Phương pháp bảo vệ điện hóa là dùng một kim loại có tính khử mạnh hơn làm vật hi sinh để bảo vệ vật liệu kim loại. Vật hi sinh và kim loại cần bảo vệ hình thành một pin điện, trong đó vật hi sinh đóng vai trò cực âm và bị ăn mòn
Ví dụ: Để bảo vệ vỏ tàu biển bằng thép, người ta gắn chặt những tấm kẽm vào phần vỏ tàu ngâm trong nước biển. Vì khi gắn miếng Zn lên vỏ tàu bằng thép sẽ hình thành một pin điện, phần vỏ tàu bằng thép là cực dương, các lá Zn là cực âm và bị ăn mòn theo cơ chế:
- Ở anot (cực âm): Zn → Zn2+ + 2e
- Ở catot (cực dương): 2H2O + O2 + 4e → 4OH-
Kết quả là vỏ tàu được bảo vệ, Zn là vật hi sinh, nó bị ăn mòn