- Dạng toán về kim loại tác dụng với dung dịch muối rất hay gặp trong bài thi đại học. Đây là 1 dạng toán không khó nếu nắm chắc phần đại cương và dãy điện hóa kim loại.
- Khi giải bài tập về phần này cần xác định bài đó thuộc dạng nào trong 4 dạng sau:
+ Dạng 1: Một kim loại tác dụng với 1 muối
+ Dạng 2: Một kim loại tác dụng với hỗn hợp muối
+ Dạng 3: Hỗn hợp kim loại tác dụng với 1 muối
+ Dạng 4: Hỗn hợp kim loại tác dụng với hỗn hợp muối
Nguyên tắc chung: Kim loại có tính khử mạnh hơn sẽ tác dụng với muối có gốc cation kim loại có tính oxi hóa mạnh hơn theo quy tắc α.
- Cần xác định kim loại nào phản ứng với muối nào trước.
- Với Na, K, Ca và Ba phản ứng với nước trước sau đó dung dịch kiềm tạo thành sẽ phản ứng với muối.
- Cần ghi nhớ 1 số phản ứng hay gặp
2Fe3+ + Fe → 3Fe2+
Cu + 2Fe3+ → Cu2+ + 2Fe2+
Fe2+ + Ag+ → Ag + Fe3+
I. BÀI TOÁN 1 KIM LOẠI TÁC DỤNG VỚI 1 MUỐI
|
Thứ tự cặp oxi hóa- khử: Am+ABn+B |
Kim loại + muối → muối mới + kim loại mới nA + mBn+ → nAm+ + mB |
- Điều kiện của phản ứng:
- A phải đứng trước B trong dãy điện hóa.
- Muối B phải tan:
Ví dụ: Fe + Cu2+ → Fe2+ + Cu
Nhưng: Fe + Al3+ không xảy ra do tính khử của Fe yếu hơn Al3+
Hay Cu + AgCl không xảy ra do AgCl không tan
- Phương pháp giải:
+) Sử dụng tăng giảm khối lượng
- Nếu mB↓> mA tan thì khối lượng thanh kim loại A tăng: Độ tăng khối lượng = mB↓- mA tan
- Nếu mB↓< mA tan thì khối lượng thanh kim loại A giảm: Độ giảm khối lượng = mA tan- mB↓
+) sử dụng bảo toàn e: ne kim loại cho = ne cation nhận
II. BÀI TOÁN 1 KIM LOẠI TÁC DỤNG VỚI 2 MUỐI
|
Thứ tự cặp oxi hóa – khử: Ap+ABn+BCm+C |
mA + pCm+ → mAp+ + pC 1. nA + pBn+ → nAp+ + pB 2. |
- Điều kiện của phản ứng:
- A phải đứng trước B và C trong dãy điện hóa.
- Muối Bn+, Cm+ phải tan.
- Phương pháp giải
- Nếu biết số mol ban đầu của A, Bn+, Cm+ta chú ý đến thứ tự phản ứng và sử dụng bảo toàn e
- Nếu biết số mol ban đầu của Bn+, Cm+nhưng không biết số mol ban đầu của A ta có thể dùng phương pháp mốc so sánh nếu biết khối lượng của chất rắn sau phản ứng (m):
- Mốc 1 (vừa đủ phản ứng 1.): mrắn = mC = m1
- Mốc 2 (vừa đủ phản ứng 2.): mrắn = mC + mB = m2
So sánh m với m1 và m2 :
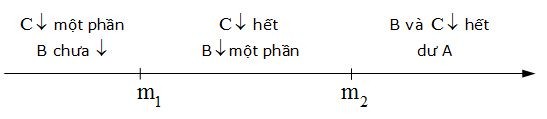
Như vậy có 3 trường hợp có thể xảy ra:
+ Trường hợp 1: Nếu m < m1 dư Cm+ chỉ có phản ứng 1. Dung dịch sau phản ứng có Ap+ ,Bn+ chưa phản ứng và Cm+ dư. Chất rắn sau phản ứng chỉ có C.
+ Trường hợp 2: Nếu m1 < m < m2 xong phản ứng 1, phản ứng 2 xảy ra một phần dư Bn+. Dung dịch sau phản ứng có Ap+ ,Bn+ dư. Chất rắn sau phản ứng có C và B.
+ Trường hợp 3: Nếu m > m2 xong phản ứng 1, xong phản ứng 2 dư A. Dung dịch sau phản ứng có Ap+. Chất rắn sau phản ứng có C, B và A dư.

