Cặp chất nào sau đây phản ứng với nhau thu được sản phẩm là NaCl
A,C,D không có phản ứng hóa học xảy ra
B. PTHH: NaOH + HCl → NaCl + H2O
Điện phân nóng chảy NaCl thu được sản phẩm gồm:
PTHH: \(2NaCl\xrightarrow{{dpnc}}2Na + C{l_2}\)
Dung dịch muối nào sau đây làm quỳ tím chuyển sang màu đỏ
NaHSO4 là muối axit, có tính chất như một axit mạnh nên làm quỳ tím chuyển sang màu đỏ
Cho dung dịch Na2SO4 vào dung dịch BaCl2 thấy
Phản ứng sinh ra kết tủa trắng BaSO4. PTHH: Na2SO4 + BaCl2 → BaSO4↓ + 2HCl
Hiện tượng khi thêm vài giọt dung dịch H2SO4 vào dung dịch BaCl2 là:
Hiện tượng: xuất hiện kết tủa trắng
H2SO4 + BaCl2 → BaSO4↓ trắng + 2HCl
Dãy hợp chất nào sau đây gồm các muối?
A. Loại HCl là axit
B. Thỏa mãn tất cả đều là muối
C. Loại H2SO4 là axit còn NaOH là bazo
D. Loại CaO là oxit bazo, Ba(OH)2 là bazo
CaCO3 có thể tham gia phản ứng với
CaCO3 có thể phản ứng với HCl
CaCO3 + 2HCl → CaCl2 + H2O + CO2↑
Để phân biệt hai dung dịch Na2CO3 và NaCl ta có thể dùng chất có công thức
Để phân biệt hai dung dịch Na2CO3 và NaCl ta có thể dùng chất HCl vì
Na2CO3 + 2HCl → 2NaCl + H2O + CO2 còn NaCl không tác dụng nên không có hiện tượng
Để phân biệt các chất đựng trong lọ riêng biệt sau: NaNO3, Cu(NO3)2, Fe(NO3)3, Ba(NO3)2 người ta cần sử dụng hóa chất nào?
Trích mẫu thử của từng chất vào các ống nghiệm riêng biệt và đánh dấu tương ứng
- Cho dung dịch NaOH dư vào 4 ống nghiệm trên
+ống nghiệm nào xuất hiện kết tủa màu xanh thì ống nghiệm đó chứ Cu(NO3)2
3NaOH + Cu(NO3)2 → Cu(OH)2↓ + 2NaNO3
+ ống nghiệm nào xuất hiện kết tủa màu nâu đỏ thì ống nghiệm đó chứa Fe(NO3)3
3NaOH + Fe(NO3)3 → Fe(OH)3↓ + 3NaNO3
+ ống nghiệm nào không có hiện tượng hig chứa NaNO3 và Ba(NO3)2
- Cho H2SO4 dư vào 2 dung dịch chưa phân biệt được NaNO3 và Ba(NO3)2
+ ống nghiệm xuất hiện kết tủa màu trắng là Ba(NO3)2
H2SO4 + Ba(NO3)2 → BaSO4↓ + 2HNO3
Dung dịch muối FeCl2 tác dụng được với tất cả các chất nào trong dãy chất sau:
FeCl2 + Mg → MgCl2 + Fe↓
FeCl2 + KOH → Fe(OH)2↓ + 2KCl
FeCl2 + NaOH → Fe(OH)2↓ + 2NaCl
FeCl2 + 2AgNO3 → 2AgCl↓ + Fe(NO3)2
Nung sắt(II)nitorat (Fe(NO3)2) ở nhiệt độ cao, ta thu được sản phẩm là:
Đây là trường hợp đặc biệt: 4Fe(NO3)2 → 2Fe2O3 + 4NO2 + 5O2
Để nhận biết 3 dung dịch bị mất nhãn : Na2SO4 , HCl , H2SO4 loãng , người ta dùng :
Lấy mẫu thử của 3 dung dịch
Dùng quì tím
+ Na2SO4 không làm quì đổi màu
+ HCl và H2SO4 làm quì hóa đỏ
Dùng BaCl2 nhận biết HCl và H2SO4
+ không có hiện tượng là HCl
+ Xuất hiện kết tủa trắng là H2SO4
BaCl2 + H2SO4 → BaSO4+ 2HCl
Cho 200ml dung dịch KOH 1M tác dụng vừa đủ dung dịch MgSO4 2M. Tính thể tích dung dịch MgSO4 2M cần dùng
Đổi 200 ml = 0,2 (lít)
nKOH = VKOH. CM KOH = 0,2.1 = 0,2 (mol)
PTHH: 2KOH + MgSO4→ Mg(OH)2↓ + K2SO4
Theo PTHH: nMgSO4 = 1/2 nKOH = 1/2. 0,2 = 0,1 (mol)
→ VMgSO4 = 0,1 : 2 = 0,05 lít
Cho V (lít) CO2 (đktc) hấp thụ hết vào 200 ml dung dịch Ca(OH)2 1M thu được 15 gam kết tủa. Giá trị của V là
200 ml = 0,2 (lít)
nCa(OH)2 = V. CM = 0,2.1 = 0,2 (mol)
nCaCO3 = mCaCO3 : MCaCO3 = 15 : 100 = 0,15 (mol)
Ta thấy nCaCO3 < nCa(OH)2 nên có 2 trường hợp xảy ra
TH1: Phản ứng chỉ tạo ra muối CaCO3. Khi đó CO2 pư hết, dd Ca(OH)2 dư. Mọi tính toán theo số mol CO2 và CaCO3
PTHH: CO2 + Ca(OH)2 → CaCO3↓ + H2O (1)
(mol) 0,15 ← 0,15
Theo PTHH (1): nCO2 = nCaCO3 = 0,15 (mol) ⟹ VCO2(đktc) = 0,15.22,4 = 3,36 (lít)
TH2: Phản ứng tạo cả muối CaCO3 và Ca(HCO3)2. Khi đó cả CO2 và Ca(OH)2 cùng phản ứng hết. Mọi tính toán theo số mol của Ca(OH)2, CO2 và CaCO3.
PTHH: CO2 + Ca(OH)2 → CaCO3↓ + H2O (2)
(mol) 0,15 0,15 ← 0,15
2CO2 + 2Ca(OH)2 → Ca(HCO3)2 (3)
Theo PTHH (2): nCa(OH)2(2) = nCaCO3 =0,15 (mol)
⟹ nCa(OH)2(3) = nCa(OH)2 ban đầu - nCa(OH)2(2) = 0,2 - 0,15 = 0,05 (mol)
Theo PTHH (3): nCO2 = 2nCa(OH)2(3) = 2.0,05 = 0,1 (mol)
Theo PTHH (2): nCO2(2) = nCaCO3 = 0,15 (mol)
⟹ ∑nCO2 (2)+(3) = 0,15 + 0,1 = 0,25 (mol) ⟹ VCO2(đktc) = 0,25.22,4 = 5,6 (lít)
Nung nóng muối A (công thức tổng quát nCaX2.H2O) trong điều kiện không có không khí ở 5000C thu được CaCO3 và hỗn hợp hơi B. Khối lượng CaCO3 thu được chỉ bằng 59,9% so với khối lượng muối A đem nung ban đầu. Tỷ khối hơi của B so với CO2 là 1,015. Toàn bộ B được cho vào CaO(rắn, dư) và làm lạnh để ngưng tụ toàn bộ hệ, thu được hỗn hợp C. Phân tích C cho thấy ngoài CaO dư còn có một chất vô cơ D và một chất hữu cơ E có tỷ lệ mol D:E là 1:2. Đốt cháy hoàn toàn 5,8 g E, cho toàn bộ sản phẩm vào dung dịch nước vôi trong dư, thu được 30 gam kết tủa. Xác định n và X trong công thức của A.
Nhiệt phân A tạo ra chất hữu cơ E => A là muối ngậm nước của axit hữu cơ
Khi nhiệt phân muối canxi của axit hữu cơ ta thu được anđehit/xeton (E) và CaCO3
Như vậy B gồm: H2O và anđehit/xeton (E)
Khi cho hỗn hợp B qua CaO thì chỉ có H2O bị hấp thụ: CaO + H2O → Ca(OH)2 (D)
Giả sử nCa(OH)2 = 1 mol; nE = 2 mol => nH2O = nCa(OH)2 = 1 mol
- Xét hỗn hợp B: MB = 1,015.44 = 44,66
Áp dụng phương pháp đường chéo ta có:
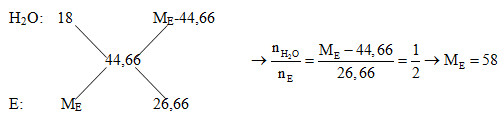
- Xét phản ứng đốt cháy 5,8 gam E: nE = 5,8 : 58 = 0,1 mol; nCO2 = nCaCO3 = 30 : 100 = 0,3 mol
=> Số C trong E = nCO2 : nE = 0,3 : 0,1 = 3
Vậy suy ra E có CTPT là C3H6O
- Xét phản ứng nhiệt phân 1mol muối A: nCaX2.H2O \(\xrightarrow{{{t^o}}}\) nCaCO3 + 2C3H6O + H2O
BTKL: mA = m sản phẩm = 100n + 2.58 + 18 = 100n + 134 (g)
Mà CaCO3 bằng 59,9% khối lượng của A nên ta có phương trình: \(\frac{{100n}}{{100n + 134}}.100\% = 59,9\% \) => n = 2
=> A có dạng là 2CaX2.H2O
Ta thấy 1 mol muối A nặng 100.2 + 134 = 334 gam => MA = 334 (g/mol) => 2(40 + 2MX) + 18 = 334 => MX = 59
=> X là CH3COO-
Vậy suy ra A là 2(CH3COO)2Ca.H2O; E là CH3-CO-CH3 (axeton)
Nhiệt phân hoàn toàn 25 g hỗn hợp MgCO3, CaCO3 , BaCO3 thu được khí B. Cho khí B hấp thụ hết vào nước vôi trong thu được 15 gam kết tủa và dung dịch C. Đun nóng dung dịch C tới phản ứng hoàn toàn thấy tạo thành thêm 6 gam kết tủa. Hỏi % khối lượng của MgCO3 nằm trong khoảng nào?
\(\begin{array}{l}\overline M C{O_3} \to MO + C{O_2}\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,(1)\\C{O_2} + Ca{(OH)_2} \to CaC{O_3} \downarrow + {H_2}O\,\,\,(2)\\0,15\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\, \leftarrow 0,15\\2CO2 + Ca{(OH)_2} \to Ca{(HC{O_3})_2} + {H_2}O\,(3)\end{array}\)
Ca(HCO3)2 \(\xrightarrow{{{t^0}}}\) CaCO3↓ + CO2↑ + H2O (4)
0,06 ← 0,06
\({n_{CaC{O_3}(2)}} = \frac{{15}}{{100}} = 0,15\,(mol);\,{n_{CaC{O_3}\,(4)}} = \frac{6}{{100}} = 0,06\,(mol)\)
Ta có: \(\sum {{n_{C{O_2}(1)}} = {n_{C{O_2}(2)}} + {n_{C{O_2}(3)}} = {n_{C{O_2}(2)}} + 2{n_{CaC{O_3}(4)}} = 0,15 + 2.0,06 = 0,27\,(mol)} \)
\( \Rightarrow {n_{MC{O_3}}} = {n_{C{O_2}(1)}} = 0,27\,(mol)\)
Gọi x, y, z lần lượt là số mol của MgCO3; CaCO3; BaCO3 trong 100 g hỗn hợp
\( \Rightarrow x + y + z = \frac{{100.0,27}}{{25}} = 1,08 \Rightarrow y + z = 108 - x\,\,(*)\)
Có: 84x + 100x + 197z = 100 → 100y + 197z = 100 – 84x (**)
\({M_{CaC{O_3}}} < {\overline M _{CaC{O_3},BaC{O_3}}} < {M_{BaC{O_3}}}\)
\( \Rightarrow 100 < \frac{{100y + 197z}}{{y + z}} < 197\)
Thế (*) và (**) vào ta có: \( \Rightarrow 100 < \frac{{100 - 84x}}{{1,08 - x}} < 197\)
\( \Rightarrow \left\{ \begin{array}{l}100.(1,08 - x) < 100 - 84x\\100 - 84x < 197.(1,08 - x)\end{array} \right. \Rightarrow \left\{ \begin{array}{l}108 - 100x < 100 - 84x\\100 - 84x < 212,76 - 197x\end{array} \right. \Rightarrow \left\{ \begin{array}{l}8 < 16x\\113x < 112,76\end{array} \right. \Rightarrow \left\{ \begin{array}{l}0,5 < x\\x < 0,9979\end{array} \right.\)
→ 0,5 < x < 0,9979
Nhân cả các vế với 84
→ 42 < 84x < 83,82
Phần trăm khối lượng của MgCO3 trong hh là: \(\% {m_{MgC{O_3}}} = \frac{{{m_{MgC{O_3}}}}}{{{m_{hh}}}}.100\% \Rightarrow \frac{{42}}{{100}}.100\% < \frac{{84x}}{{100}}.100\% < \frac{{83,82}}{{100}}.100\% \)
\( \Rightarrow 42\% < \% {m_{MgC{O_3}}} < 82,83\% \)
Hoà tan hoàn toàn 25,2 g một muối cacbonat của kim loại hóa trị II bằng dung dịch HCl 7,3% (D = 1,038 g/ml). Cho toàn bộ khí CO2 thu được vào 500 ml dung dịch NaOH 2M, sau phản ứng đem cô cạn thì thu được 47,8 gam chất rắn. Biết các phản ứng xảy ra hoàn toàn. a/ Xác định CTHH của muối cacbonat
Đặt công thức của muối cacbonat là MCO3.
Các PTHH:
MCO3 + 2 HCl →MCl2 + CO2↑ + H2O (1)
NaOH + CO2 → NaHCO3. (2)
a a a
2NaOH + CO2 → Na2CO3 + H2O. (3)
2b b b
Số mol NaOH: nNaOH = 0,5. 2 = 1 mol
Cho CO2 vào dung dịch NaOH có thể xảy ra các trường hợp sau:
TH1: chỉ xảy ra pư (2). NaOHPƯ hết, CO2 có thể hết hoặc dư. Mọi tính toán theo NaOH
Theo(3): nNaHCO3 = nNaOH = 1(mol) => mNaHCO3 = 1 . 84 = 84(g) ≠ 47,8(g)=> loại
TH2: xảy ra cả (2) và (3). CO2 và NaOH đều hết. rắn thu được là 2 muối
Gọi a, b lần lượt là số mol CO2 tham gia ở phản ứng (2) và (3).
Theo phương trình và bài ta có:
\(\left\{ \begin{array}{l}{n_{NaOH}} = a + 2b = 1\\{m_{muoi}} = 84a + 106b = 47,8\end{array} \right.\) => vô nghiệm => loại
TH3: xảy ra (3). CO2 hết, rắn sau pư là NaOHdư và Na2CO3
Gọi nCO2(3)= x(mol); nNaOHdư = y(mol)
Theo (3) nNaOHpư = 2nCO2(4)=2x(mol) ; nNa2CO3 = nCO2(4) = x(mol)
\(\left\{ \begin{array}{l}{n_{NaOH}} = 2x + y = 1\\\sum {m{\,_{ran}}\, = m{\,_{N{a_2}C{O_3}}} + {m_{NaO{H_{\,du}}}} = 106x + 40y = 47,8} \end{array} \right. \Rightarrow \left\{ \begin{array}{l}x = 0,3\\y = 0,4\end{array} \right.\)
→ nMCO3 = nCO2(3) = 0,3 (mol)
\({M_{MC{O_3}}} = \frac{{{m_{MC{O_3}}}}}{{{n_{MC{O_3}}}}} = \frac{{25,2}}{{0,3}} = 84 \Rightarrow {m_M} = 84 - 60 = 24\,(Mg)\)
→ Công thức muối: MgCO3
Trộn 30ml dd có chứa 1,04 g BaCl2 với 170ml dd có chứa 3,4g AgNO3. Tính CM của chất còn lại trong dd sau phản ứng. Biết thể tích dd thay đổi không đáng kể.
n BaCl2 = mBaCl2 : MBaCl2 = 1,04 : (137 + 35,5 . 2) = 0,005 mol
nAgNO3 = mAgNO3 : MAgNO3 = 3,4 : (108 + 14 + 3 . 16) = 0,02 mol
PTHH: BaCl2 + 2AgNO3 → 2AgCl↓ + Ba(NO3)2
Tỉ lệ: 1 2 2 1
Pứ: 0,005 0,02 ?mol ?mol
Ta có
=> BaCl2 phản ứng hết, AgNO3 dư
nAgNO3phản ứng = 2nBaCl2 = 0,01 mol
=> nAgNO3 dư = nAgNO3 – nAgNO3 phản ứng = 0,02 – 0,01 = 0,01 mol
nBa(NO3)2 = nBaCl2 = 0,005 mol
Vdd sau phản ứng = VBaCl2 + VAgNO3 = 30 + 170 = 200ml = 0,2 lít
=> CM AgNO3 = nAgNO3 : Vdd = 0,01 : 0,2 = 0,05M
CM Ba(NO3)2 = n Ba(NO3)2 : Vdd = 0,005 : 0,2 = 0,025M
Hòa tan 10 gam hỗn hợp muối XCO3 và Y2(CO3)3 bằng dd HCl dư thư được dd A và 0,672 lít khí ở đktc.Khối lượng muối khan thu được sau phản ứng là

=> m Muối = 10,33 gam
Cho dung dịch AgNO3 dư tác dụng với hỗn hợp có hòa tan 12,5 gam hai muối KCl và KBr thu được 20,78 gam hỗn hợp AgCl và AgBr. Thành phần % của muối AgCl trong hỗn hợp thu được sau phản ứng là.




