Nung nóng muối A (công thức tổng quát nCaX2.H2O) trong điều kiện không có không khí ở 5000C thu được CaCO3 và hỗn hợp hơi B. Khối lượng CaCO3 thu được chỉ bằng 59,9% so với khối lượng muối A đem nung ban đầu. Tỷ khối hơi của B so với CO2 là 1,015. Toàn bộ B được cho vào CaO(rắn, dư) và làm lạnh để ngưng tụ toàn bộ hệ, thu được hỗn hợp C. Phân tích C cho thấy ngoài CaO dư còn có một chất vô cơ D và một chất hữu cơ E có tỷ lệ mol D:E là 1:2. Đốt cháy hoàn toàn 5,8 g E, cho toàn bộ sản phẩm vào dung dịch nước vôi trong dư, thu được 30 gam kết tủa. Xác định n và X trong công thức của A.
Trả lời bởi giáo viên
Nhiệt phân A tạo ra chất hữu cơ E => A là muối ngậm nước của axit hữu cơ
Khi nhiệt phân muối canxi của axit hữu cơ ta thu được anđehit/xeton (E) và CaCO3
Như vậy B gồm: H2O và anđehit/xeton (E)
Khi cho hỗn hợp B qua CaO thì chỉ có H2O bị hấp thụ: CaO + H2O → Ca(OH)2 (D)
Giả sử nCa(OH)2 = 1 mol; nE = 2 mol => nH2O = nCa(OH)2 = 1 mol
- Xét hỗn hợp B: MB = 1,015.44 = 44,66
Áp dụng phương pháp đường chéo ta có:
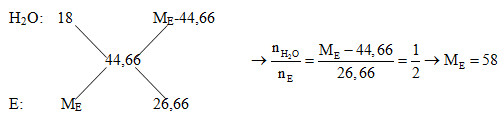
- Xét phản ứng đốt cháy 5,8 gam E: nE = 5,8 : 58 = 0,1 mol; nCO2 = nCaCO3 = 30 : 100 = 0,3 mol
=> Số C trong E = nCO2 : nE = 0,3 : 0,1 = 3
Vậy suy ra E có CTPT là C3H6O
- Xét phản ứng nhiệt phân 1mol muối A: nCaX2.H2O \(\xrightarrow{{{t^o}}}\) nCaCO3 + 2C3H6O + H2O
BTKL: mA = m sản phẩm = 100n + 2.58 + 18 = 100n + 134 (g)
Mà CaCO3 bằng 59,9% khối lượng của A nên ta có phương trình: \(\frac{{100n}}{{100n + 134}}.100\% = 59,9\% \) => n = 2
=> A có dạng là 2CaX2.H2O
Ta thấy 1 mol muối A nặng 100.2 + 134 = 334 gam => MA = 334 (g/mol) => 2(40 + 2MX) + 18 = 334 => MX = 59
=> X là CH3COO-
Vậy suy ra A là 2(CH3COO)2Ca.H2O; E là CH3-CO-CH3 (axeton)

