Kim loại nào sau đây không tác dụng được với dung dịch axit H2SO4 loãng?
Fe, Al, Na tác dụng với dung dịch axit H2SO4 loãng
Cu không tác dụng với dd axit H2SO4 loãng
Dãy các chất có thể tác dụng với dung dịch HCl là:
Dãy các chất có thể tác dụng với dung dịch HCl là Na, FeO, CuO
B, C, D sai do có CO2 không tác dụng với HCl
Dãy gồm các oxit tác dụng được với nước tạo thành dung dịch axit là:
A sai do CO không tác dụng với nước
B sai do NO không tác dụng với nước
C đúng
D sai do NO và CO không tác dụng với nước
Hiện tượng quan sát được khi cho mẩu magie vào ống nghiệm chứa axit HCl dư là:
Khi cho mẩu magie vào ống nghiệm chứa axit HCl dư mẩu Mg tan dần, có bọt khí thoát ra, dung dịch thu được không màu : Mg + 2HCl → MgCl2 + H2
Dung dịch MgCl2 thu được không có màu
Axit HCl tác dụng được với oxit nào trong các oxit sau: Na2O; BaO; CuO; MgO; SO2; P2O5
Na2O; BaO; CuO; MgO là các oxit bazo nên pư với axit=> muối và nước
Hòa tan 2,4 gam oxit của một kim loại hóa trị II vào 21,9 gam dung dịch HCl 10% thì vừa đủ . Oxit đó là:
Đặt công thức của oxit là RO
C% = m chất tan : m dung dịch
=> mHCl = mdung dịch . C% = 21,9 . 10% = 2,19g
=> nHCl = 2,19 : 36,5 = 0,06 mol
PTHH: RO + 2HCl → RCl2 + H2O
1 2
x ← 0,06
Theo phương trình phản ứng ta tính được
nRO = 0,06 : 2 = 0,03 mol
=> MRO = mRO : nRO = 2,4 : 0,03 = 80
=> MR = 64 (Cu)
Hòa tan 1,68 gam oxit của 1 kim loại hóa trị II vào 21,9 gam dung dịch HCl 10% thì phản ứng xảy ra vừa đủ. Công thức của oxit là:
![]() → nXO = 0,03 mol
→ nXO = 0,03 mol
→ MXO = 1,68 :0,06 =56 → MX = 40(Ca)
Chất tác dụng với dung dịch HCl tạo thành chất khí nhẹ hơn không khí là:
A. Thỏa mãn vì sinh ra khí H2 (M = 2 g/mol) nhẹ hơn không khí.
PTHH: Mg + 2HCl → MgCl2 + H2↑
B, C. Loại vì sinh ra khí CO2 (M = 44 g/mol) nặng hơn không khí
PTHH: CaCO3 + 2HCl → CaCl2 + CO2↑ + H2O
MgCO3 + 2HCl → MgCl2 + CO2↑ + H2O
D. Loại vì sinh ra khí SO2 (M = 64 g/mol) nặng hơn không khí
PTHH: Na2SO3 + 2HCl → 2NaCl + SO2↑ + H2O
Hòa tan 10 gam hỗn hợp chất rắn gồm Fe, FeO và Cu vào dung dịch HCl loãng dư. Kết thúc phản ứng thấy có 2,24 lít khí H2 (đktc) thoát ra và thu được dung dịch B và 0,8 gam chất rắn C. Cô cạn dung dịch B thu được m gam muối. Gía trị của m là:
Theo PTHH nFe =nH2 = 0,1 mol
mCu =mC =0,8g
→ mFeO = 10 – 0,1.56 -0,8 =3,6 (g) → nFeO =0,05 mol
→nFeCl2 = nFe + nFeO = 0,15 mol → mmuối =19,05g
Cặp chất tác dụng với nhau tạo thành sản phẩm có chất khí:
PTHH: BaCO3 + H2SO4 → BaSO4↓ + H2O + CO2↑
Nhóm chất tác dụng với dung dịch H2SO4 loãng sinh ra chất kết tủa màu trắng:
* ZnO, CuO tan không có kết tủa
* BaCl2, Ba(NO3)2 , Ba(OH)2 tan tạo kết tủa BaSO4 màu trắng
Do đề bài hỏi nhóm chất tan tạo kết tủa trắng => Chỉ có nhóm BaCl2, Ba(NO3)2 thoả mãn điều kiện
Cho 4,8 gam kim loại magie tác dụng vừa đủ với dung dịch axit clohidric. Thể tích khí Hiđro thu được ở đktc là:
nMg = mMg : MMg = 4,8 : 24 = 0,2mol
PTHH: Mg + 2HCl → MgCl2 + H2
1mol 2mol 1mol
0,2mol ? mol
VH2 = nH2 . 22,4 = 0,2 . 22,4 = 4,48l
Hòa tan vừa hết 20 gam hỗn hợp CuO và Fe2O3 trong 200 ml dung dịch HCl 3,5M . Khối lượng mỗi oxit trong hỗn hợp là:
gọi x, y lần lượt là số mol của CuO và Fe2O3
CuO + 2HCl → CuCl2 + H2O (1)
x → 2x
Fe2O3 + 6HCl → 2FeCl3 + 3H2O (2)
y → 6y
ta có mhh = mCuO + mFe2O3 = 80x + 160y = 20 (I)
nHCl = VHCl . CM HCl = 0,2 . 3,5 = 0,7 mol
nHCl = nHCl (1) + nHCl(2) = 2x + 6y = 0,7 (II)
Giải hệ (I) và (II) ta có x = 0,05 và y = 0,1
=> mCuO = 0,05 . 80 = 4g
mFe2O3 = 0,1 . 160 = 16g
Hãy cho biết muối nào có thể điều chế bằng phản ứng của kim loại với dung dịch Axit H2SO4 loãng ?
A. Thỏa mãn: Zn + H2SO4 → ZnSO4 + H2↑
B,D loại vì không phải muối sunfat
C. Loại vì Cu không phản ứng với dd H2SO4
Cho 0,52 gam hỗn hợp hai kim loại Mg và Fe tan hoàn toàn trong dd HCl, dư thấy thoát ra 0,336 lít khí (đktc). Tính tổng khối lượng muối clorua thu được sau phản ứng là :
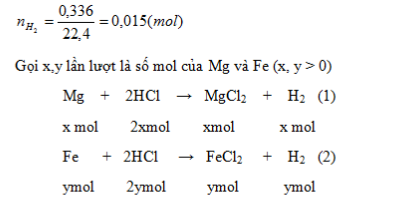

Hỗn hợp X gồm Fe và Al (với tỉ lệ mol 1 : 1). Hòa tan hoàn toàn m gam X bằng dung dịch HCl dư, sau phản ứng thu được 5,6 lít H2 (đktc). Giá trị của m là:
\({n_{{H_2}}} = \dfrac{{5,6}}{{22,4}} = 0,25\,\,mol\)
Đặt số mol Al = số mol Fe = x (mol)
PTHH:
2Al + 6HCl → 2AlCl3 + 3H2↑
x → 1,5x (mol)
Fe + 2HCl → FeCl2 + H2↑
x → x (mol)
Tổng số mol H2 là: 1,5x + x = 0,25 \( \to\) x = 0,1 (mol)
\( \to\) mhh = mAl + mFe = 0,1.27 + 0,1.56 = 8,3
Để trung hòa hoàn toàn 100ml dung dịch NaOH 1M cần vừa đủ V ml dung dịch H2SO4 2M. Giá trị của V là:
nNaOH = 0,1.1 = 0,1 (mol)
PTPƯ: 2NaOH + H2SO4 → Na2SO4 + H2O
0,1 → 0,05 (mol)
=> VH2SO4 = nH2SO4 : CM = 0,05 : 2 = 0,025 (lít) = 25 (ml)
Phản ứng giữa natri hiđroxit và axit sunfuric loãng được gọi là phản ứng
Phản ứng giữa dd axit và dd bazo được gọi là phản ứng trung hòa.
Cho a gam sắt vào dung dịch HCl dư. Sau phản ứng thu được 6,72 lít khí hidro ở đktc.Giá trị của a là
nH2(ĐKTC) = 6,72: 22,4 = 0,3 (mol)
PTHH: Fe + 2HCl → FeCl2 + H2↑
0,3 ← 0,3 (mol)
=> mFe = 0,3. 56 = 16,8 (g)
Hòa tan hoàn toàn 5,6 gam Fe cần dùng V(ml) dung dịch HCl 2M. Giá trị của V cần tìm là:
nFe = 5,6: 56 = 0,1 (mol)
PTHH: Fe + 2HCl → FeCl2 + H2↑
Theo PTHH: nHCl = 2nFe = 2. 0,1 = 0,2 (mol)
=> VHCl = n: CM = 0,2: 2 = 0,1 (lít) = 100 (ml)

