Để phân biệt hai dung dịch Na2CO3 và NaCl ta có thể dùng chất có công thức
Để phân biệt hai dung dịch Na2CO3 và NaCl ta có thể dùng chất HCl vì
Na2CO3 + 2HCl → 2NaCl + H2O + CO2 còn NaCl không tác dụng nên không có hiện tượng
Cho sơ đồ sau:![]() . Các chất X1 và X2 trong sơ đồ trên là:
. Các chất X1 và X2 trong sơ đồ trên là:
![]()
Cho PTHH: NaOH + X → Fe(OH)3 + Y. Chất X và Y trong PTHH trên là:
Ta có 3NaOH + FeCl3→ Fe(OH)3 + 3NaCl
A sai do FeCl2 + NaOH → Fe(OH)2 + NaCl
B sai do FeSO4 +NaOH → Fe(OH)2 + Na2SO4
D sai do sản phẩm không tạo ra Na2SO4
![]()
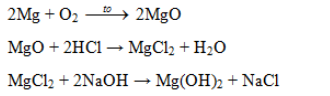

C nhiệt phân sinh ra ZnO và H2O => C là Zn(OH)2
B tác dụng với KOH tạo thành Zn(OH)2 + KCl => B là ZnCl2
A tác dụng với HCl => ZnCl2 + H2 => A là Zn
Sản phẩm của phản ứng nhiệt phân hoàn toàn Fe(OH)3 là:
Nhiệt phân bazo không tan thu được oxit tương ứng và nước
Dung dịch nào sau đây không phản ứng với dung dịch BaCl2?
Dung dịch không phản ứng với dung dịch BaCl2 là HNO3
Trong các dung dịch dưới đây có mấy dung dịch có thể sử dụng để nhận biết 2 dung dịch Na2SO4 và Na2CO3?
Dung dịch HCl, dung dịch BaCl2, dung dịch NaOH, dung dịch Ba(OH)2,
Dung dịch có thể sử dụng để nhận biết 2 dung dịch Na2SO4 và Na2CO3 là : Dung dịch HCl
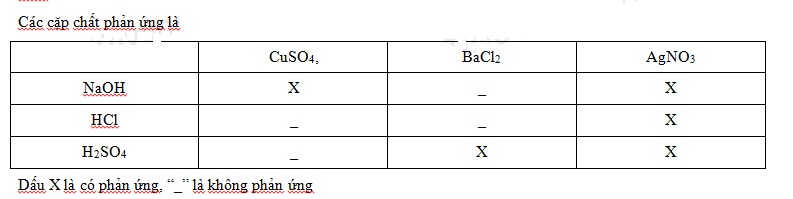
Dãy A gồm các dung dịch : NaOH, HCl, H2SO4; Dãy B gồm các dung dịch: CuSO4, BaCl2, AgNO3.
Cho lần lượt các chất ở dãy A phản ứng đôi một với các chất ở dãy B. Số phản ứng thu xảy ra thu được kết tủa là:
Cho các chất có công thức: Ba(OH)2, MgSO4, Na2CO3, CaCO3, H2SO4. Số chất tác dụng được với dung dịch K2CO3 là:
Chất tác dụng được với dung dịch K2CO3 là: Ba(OH)2, MgSO4, H2SO4
Cho dung dịch KOH vào ống nghiệm đựng dung dịch FeCl3, hiện tượng quan sát được là:
3KOH + FeCl3 → Fe(OH)3↓+ 3KCl
Fe(OH)3 kết tủa màu nâu đỏ
Nếu chỉ dùng dung dịch NaOH thì có thể phân biệt được 2 dung dịch muối trong mỗi cặp chất sau:
Khi cho NaOH vào 2 dd chỉ Fe2(SO4)3 xuất hiện kết tủa nâu đỏ, Na2SO4 không có hiện tượng
6NaOH + Fe2(SO4)3 → 3Na2SO4 + 2Fe(OH)3↓
=> NaOH phân biệt được 2 dd Fe2(SO4)3 và Na2SO4
Cho 20 gam CaCO3 vào 200 ml dung dịch HCl 3M. Số mol chất còn dư sau phản ứng là:
n CaCO3 = m CaCO3 : M CaCO3 = 20 : 100 = 0,2 mol
nHCl = VHCl . CM HCl = 0,2 . 3 = 0,6 mol
PTHH: CaCO3 + 2HCl→ CaCl2 + H2O + CO2↑
Tỉ lệ: 1 2
Pứ: 0,2 mol 0,6 mol
Ta có \({{{n_{CaC{O_3}}}} \over 1} < {{{n_{HCl}}} \over 2}(0,2 < 0,3)\)
=> CaCO3 phản ứng hết và HCl còn dư
nHCl phản ứng = 2nCaCO3 = 0,4 mol
=> nHCl dư = nHCl – nHCl phản ứng = 0,6 – 0,4 = 0,2 mol
Hòa tan 10 gam hỗn hợp muối XCO3 và Y2(CO3)3 bằng dd HCl dư thư được dd A và 0,672 lít khí ở đktc.Khối lượng muối khan thu được sau phản ứng là

Cho 0,1 mol Ba(OH)2 vào dung dịch NH4NO3 dư thì thể tích thoát ra ở đktc là :
PTHH: Ba(OH)2 + 2NH4NO3 → Ba(NO3)2 + 2NH3 + 2H2O
Tỉ lê: 1 2
Pứ: 0,1 ? mol
Từ PTHH ta có n NH3 = 2 n Ba(OH)2 = 0,2 mol
=> V NH3 = n NH3 . 22,4 = 0,2 . 22,4 = 44,8 lít
Để nhận biết 3 dung dịch bị mất nhãn : Na2SO4 , HCl , H2SO4 loãng , người ta dùng :
Lấy mẫu thử của 3 dung dịch
Dùng quì tím
+ Na2SO4 không làm quì đổi màu
+ HCl và H2SO4 làm quì hóa đỏ
Dùng BaCl2 nhận biết HCl và H2SO4
+ không có hiện tượng là HCl
+ Xuất hiện kết tủa trắng là H2SO4
BaCl2 + H2SO4 → BaSO4+ 2HCl
Cho dung dịch AgNO3 dư tác dụng với hỗn hợp có hòa tan 12,5 gam hai muối KCl và KBr thu được 20,78 gam hỗn hợp AgCl và AgBr. Thành phần % của muối AgCl trong hỗn hợp thu được sau phản ứng là.
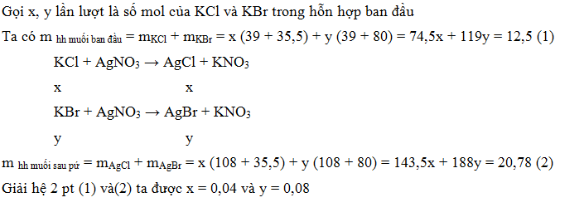
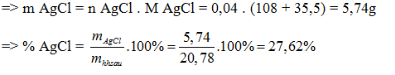
Dung dịch ZnSO4 bị lẫn tạp chất CuSO4 Kim loại nào sau đây làm sạch dung dịch
Ta dùng kim loại sao cho đẩy được Cu ra khỏi muối đồng thời muối mới bắt buộc phải là ZnSO4 để tránh thêm tạp chất khác
=> kim loại là Zn
Zn + CuSO4 → ZnSO4 + Cu
Lọc loại bỏ kết tủa thu được ZnSO4 tinh khiết
Cho 175 ml dung dịch Ba(OH)2 1M vào 100 ml dung dịch Mg(HCO3)2 1M. Sau phản ứng hoàn toàn, thu được m gam kết tủa. Tìm giá trị của m.
Ba(OH)2 + Mg(HCO3)2 → BaCO3↓ + MgCO3↓ + 2H2O
0,1 ← 0,1
Dư: 0,075
Vậy, m(kết tủa) = mBaCO3 + mMgCO3 =197.0,1 + 84.0,1 = 28,1 (g)
Cho 500 ml dung dịch NaCl 2M tác dụng với 600 ml dung dịch AgNO3 2M. Khối lượng kết tủa thu được là:
nNaCl = VNaCl . CM NaCl = 0,5 . 2 = 1 mol
n AgNO3 = VAgNO3 . CM AgNO3 = 0,6 . 2 = 1,2 mol
PTHH: NaCl + AgNO3 → NaNO3 + AgCl↓
Tỉ lệ: 1 1 1
Pứ: 1mol 1,2 mol ? mol
Ta có \({{{n_{NaCl}}} \over 1} < {{{n_{AgN{O_3}}}} \over 1}(1 < 1,2)\)
=> AgNO3 dư
=> nAgCl = nNaCl = 1 mol
=> mAgCl = nAgCl . MAgCl = 1 . (108 + 35,5) = 143,5g

