A. KIM LOẠI KIỀM THỔ
I. VỊ TRÍ VÀ CẤU TẠO
1. Vị trí
- Kim loại kiềm thổ là những nguyên tố s (ns2) thuộc nhóm IIA, gồm các kim loại:
Beri Magie Canxi Stronti Bari
=> Trong mỗi chu kì, các kim loại kiềm thổ đứng sau kim loại kiềm.
2. Cấu tạo.

II. TÍNH CHẤT VẬT LÍ
- Nhiệt độ nóng chảy và nhiệt độ sôi tương đối thấp
- Do cấu tạo mạng tinh thể của các nguyên tố khác nhau nên nhiệt độ nóng chảy, nhiệt độ sôi không thay đổi dựa theo điện tích hạt nhân
- Là những chất rắn màu trắng bạc hoặc xám nhạt, có ánh bạc, dẫn điện, dẫn nhiệt tốt.
- Độ cứng: kim loại kiềm thổ cứng hơn kim loại kiềm, nhưng nhìn chung kim loại kiềm thổ có độ cứng thấp; độ cứng giảm dần từ Be → Ba (Be cứng nhất có thể vạch được thủy tinh; Ba chỉ hơi cứng hơn chì).
- Khối lượng riêng tương đối nhỏ, độ cứng tuy cao hơn kim loại kiềm nhưng vẫn nhỏ hơn nhôm.
III. TÍNH CHẤT HÓA HỌC
- Kim loại kiềm thổ có 2e lớp ngoài cùng trong cấu hình e
=> có xu hướng nhường 2 e khi tham gia phản ứng hóa học
M – 2e → M2+
=> Kim loại kiềm thổ có tính khử mạnh.
1. Tác dụng với phi kim
- Ở to thường, Be và Mg bị oxi hóa chậm tạo thành lớp màng oxit bảo vệ, các kim loại còn lại tác dụng với mạnh hơn.
- Khi đốt nóng tất cả các kim loại nhóm IIA đều cháy thành oxit.
2Mg + O2 → 2MgO
- Với halogen: phản ứng dễ dàng ở nhiệt độ thường: M + X2 → MX2
Ví dụ:
Ca + Cl2 → CaCl2
- Với phi kim kém hoạt động phải đun nóng:
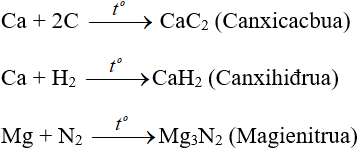
2. Tác dụng với axit
a) Tác dụng với HCl, H2SO4 loãng
Ca + 2HCl → CaCl2 + H2
b) Tác dụng với HNO3, H2SO4 đặc
- Khử N+5, S+6 thành các hợp chất mức oxi hoá thấp hơn.
4Ca + 10HNO3 (l) → 4Ca(NO3)2 + NH4NO3 + 3H2O
Mg + 4HNO3 đ → Mg(NO3)2 + 2NO2 + 2H2O
3. Tác dụng với nước
- Ca, Sr, Ba tác dụng với nước ở nhiệt độ thường tạo dung dịch bazơ:
Ca + 2H2O → Ca(OH)2 + H2
- Mg không tan trong nước lạnh, tan chậm trong nước nóng tạo thành MgO.
Mg + H2O \(\xrightarrow{{{t}^{o}}}\) MgO + H2
IV. ỨNG DỤNG
- Kim loại Be được dùng làm chất phụ gia để chế tạo những hợp kim có tính đàn hồi cao, bền chắc, không bị ăn mòn.
- Kim loại Mg dùng để chế tạo những hợp kim có đặc tính cứng, nhẹ, bền. Những hợp kim này được dùng để chế tạo máy bay, tên lửa, ôtô,... Kim loại Mg còn được dùng để tổng hợp nhiều hợp chất hữu cơ. Bột Mg trộn với chất oxi hoá dùng để chế tạo chất chiếu sáng ban đêm.
- Kim loại Ca dùng làm chất khử để tách oxi, lưu huỳnh ra khỏi thép. Canxi còn được dùng để làm khô một số hợp chất hữu cơ.
V. ĐIỀU CHẾ
Điện phân nóng chảy muối kim loại kiềm thổ
CaCl2 \(\xrightarrow{\text{pnc}}\) Ca + Cl2
B. MỘT SỐ HỢP CHẤT CỦA CANXI
I. CANXI HIDROXIT: Ca(OH)2
- Tính chất vật lý: là chất rắn màu trắng, ít tan trong nước
- Tính chất hóa học: Mang đầy đủ tính chất của một dung dịch kiềm (tác dụng với axit, oxit axit, muối)
II. CANXI CACBONAT CaCO3
- Tính chất vật lý: chất rắn màu trắng, không tan trong nước
- Tính chất hóa học : đây là muối của axit yếu, không bền nên tác dụng được với nhiều axit vô cơ, giải phóng khí cacbonic :
CaCO3 + 2HCl → CaCl2 + H2O + CO2
CaCO3 + 2CH3COOH → Ca(CH3COO)2 + H2O + CO2
+ Canxi cacbonat tan dần trong nước có chứa khí cacbon dioxit, tạo ra muối tan là canxi hidrocacbonat (Ca(HCO3)2):
CaCO3 + H2O + CO2 \(\rightleftarrows \) Ca(HCO3)2
=> Phản ứng thuận: Giải thích sự xâm thực của nước mưa đối với đá vôi
+ Phản ứng nghịch: Giải thích sự hình thành thạch nhũ có trong hang động.
III. CANXI SUNFAT: CaSO4
Tính chất:
- Canxi sunfat là chất rắn, màu trắng, tan ít trong nước (độ tan ở 25oC là 0,15 g/100 gam H2O).
- Tuỳ theo lượng nước kết tinh trong muối canxi sunfat, ta có 3 loại :
+ CaSO4.2H2O có trong tự nhiên là thạch cao sống, bền ở nhiệt độ thường.
+ CaSO4.H2O hoặc CaSO4.0,5H2O là thạch cao nung
+ CaSO4 có tên là thạch cao khan: không tan và không tác dụng với nước.
IV. NƯỚC CỨNG
- Định nghĩa: Nước cứng là nước có chứa nhiều cation Ca2+, Mg2+. Nước chứa ít hoặc không chứa các ion trên được gọi là nước mềm.
- Phân loại:
+ Nước cứng tạm thời: là nước có chứa các ion: Ca2+, Mg2+, HCO3-
+ Nước cứng vĩnh cửu: là nước có chứa các ion: Ca2+, Mg2+, SO42-, Cl-
+ Nước cứng toàn phần: là nước có cả tính cứng tạm thời và tính cứng vĩnh cửu
=> Nước tự nhiên thường là nước cứng toàn phần.
- Tác hại của nước cứng:
+ Làm giảm bọt, giảm khả năng tẩy rửa của xà phòng, khiến thức ăn lâu chín và giảm mùi vị.
+ Nước cứng cũng gây tác hại cho các ngành sản xuất, làm hỏng nhiều dung dịch cần pha chế.
- Biện pháp làm mềm nước cứng
+ Nguyên tắc : Làm giảm nồng độ các cation Ca2+, Mg2+ trong nước cứng.
- Phương pháp kết tủa
+ Nước cứng tạm thời : Đun sôi
Ca(HCO3)2 \(\xrightarrow{{{t}^{o}}}\) CaCO3¯ + CO2 + H2O
Mg(HCO3)2 \(\xrightarrow{{{t}^{o}}}\) MgCO3¯ + CO2 + H2O
+ Nước cứng vĩnh cửu : Dùng dung dịch Na2CO3, Na3PO4.
Ca2+ + \(C{{O}_{3}}^{2-}\) → CaCO3 ¯
3Ca2+ + \(P{{O}_{4}}^{3-}\) → Ca3(PO4)2 ¯
- Phương pháp trao đổi ion
V. NHẬN BIẾT ION Ca2+, Mg2+ TRONG DUNG DỊCH
Để chứng minh sự có mặt của ion Ca2+, Mg2+ ta dùng dung dịch chứa muối cacbonat để tạo ra kết tủa CaCO3 hoặc MgCO3. Sau đó sục khí CO2 dư vào dung dịch, nếu kết tủa tan chứng tỏ có mặt của Ca2+ hoặc Mg2+ trong dung dịch ban đầu
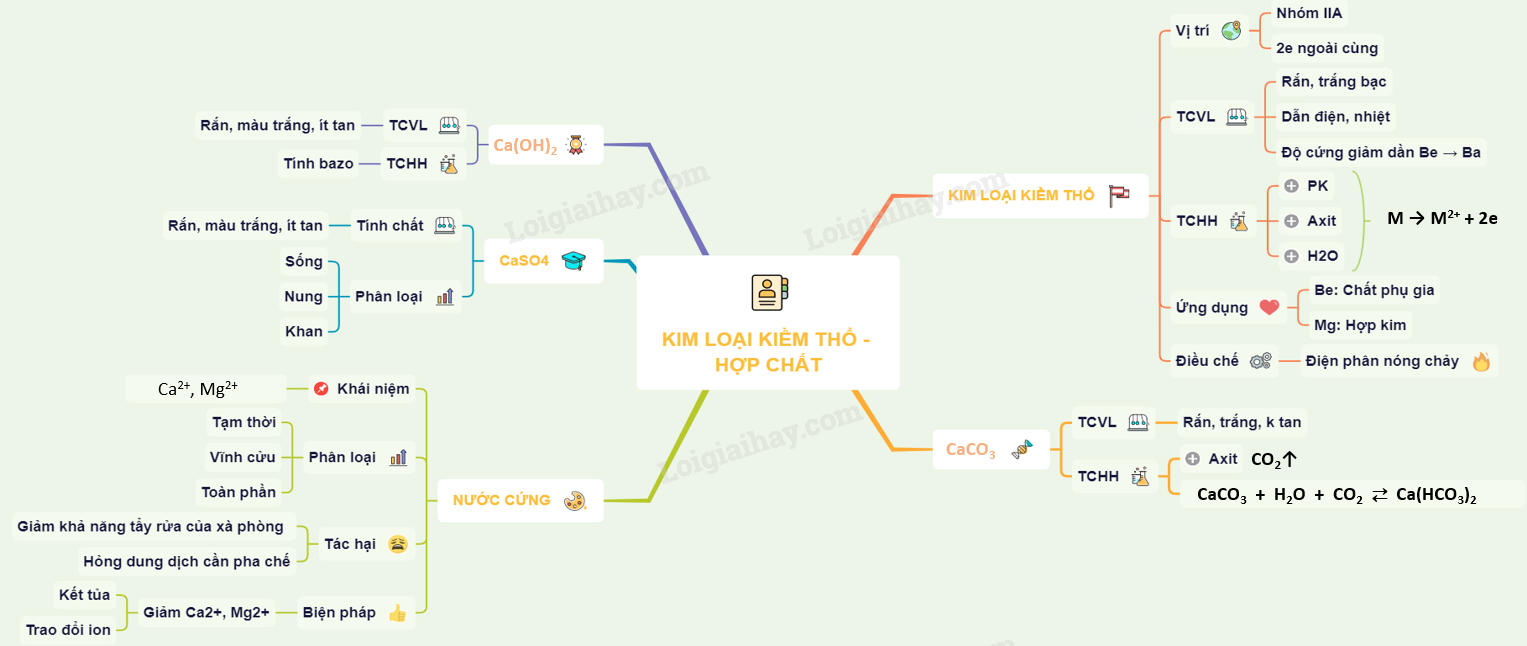
Sơ đồ tư duy: Kim loại kiềm thổ và hợp chất quan trọng của kim loại kiềm thổ