Đề bài
Câu 1. Phát biểu nào sau đây không đúng về nhôm?
A. Nhôm dẫn điện tốt nên dùng làm dây dẫn.
B. Nhôm khó nóng chảy nên dùng làm dụng cụ đun nấu.
C. Nhôm dễ dát mỏng, không độc nên dùng làm giấy gói kẹo, thuốc lá.
D. Nhôm có khối lượng riêng nhỏ nên dùng để chế tạo.
Câu 2. Phản ứng nào sau đây chứng minh Al là kim loại có tính khử mạnh hơn so với các kim loại trung bình (Fe, Ni, Pb,...)?
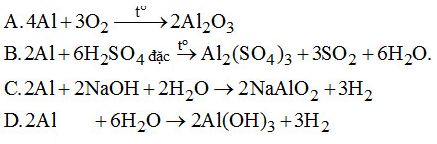
Câu 3. Phản ứng điều chế nhôm trong công nghiệp là

Câu 4. Criolit \(N{a_3}Al{F_6}\) được thêm vào \(A{l_2}{O_3}\) trong quá trình điện phân \(A{l_2}{O_3}\) nóng chảy, để sản xuất nhôm. Lí do nào sau đây không liên quan đến vai trò của criolit?
A. Làm giảm nhiệt độ nóng chảy \(A{l_2}{O_3}\), cho phép điện phân ở nhiệt độ thấp nhằm tiết kiệm năng lượng.
B. Làm tăng độ dẫn điện của \(A{l_2}{O_3}\) nóng chảy.
C. Tạo một lớp ngăn cách để bảo vệ nhôm nóng chảy khỏi bị oxi hóa.
D. Giúp loại bỏ tạp chất trong nhôm.
Câu 5. Để điều chế \(Al{(OH)_3}\) trong phòng thí nghiệm, dùng cách nào sau đây hiệu quả nhất?
A. Đổ từ từ dung dịch NaOH vào dung dịch \(AlC{l_3}\) cho tới dư.
B. Đổ từ dung dịch \(NaAl{O_2}\) vào dung dịch NaOH cho tới dư.
C. Nhỏ dung dịch HCl tới dư vào dung dịch \(NaAl{O_2}\).
D. Rót từ từ dung dịch \(N{H_3}\) vào dung dịch \(AlC{l_3}\) tới dư.
Câu 6. Sục khí \(C{O_2}\) từ từ đến dư vào dung dịch \(NaAl{O_2}\). Hiện tượng quan sát được là
A. ban đầu có kết tủa, sau đó kết tủa tan tạo dung dịch trong suốt.
B. có kết tủa trắng tạo thành, kết tủa không tan khi \(C{O_2}\) dư,
C. dung dịch vẫn trong suốt, không có hiện tượng gì xảy ra.
D. lúc đầu dung dịch vẫn trong suốt, sau đó khi \(C{O_2}\) dư mới có kết tủa trắng.
Câu 7. Hóa chất thích hợp để trực tiếp phân biệt ba chất rắn Al, Mg, \(A{l_2}{O_3}\) là
A. dung dịch HCl.
B. dung dịch \(CuC{l_2}\)
C. dung dịch NaOH.
D. dung dịch \(HN{O_3}\) loãng.
Câu 8. Chất X có đặc điểm:
+ Tan trong dung dịch HCl và NaOH.
+ Không tan trong dung dịch \(F{e_2}{(S{O_4})_3}.\)
+ Khôn bị nhiệt phân.
X là chất nào dưới đây?
\(\begin{array}{l}A.\,Al.\\B.\,Al{(OH)_3}.\end{array}\) \(\begin{array}{l}B.\,A{l_2}{O_3}.\\D.\,Al{(N{O_3})_3}.\end{array}\)
Câu 9. Một hỗn hợp gồm Na, Al có tỷ lệ số mol là 1:2. Cho hỗn hợp này vào nước. Sau khi kết thúc phản ứng thu được 8,96 lít khí \({H_2}\) (đktc) và còn lại chất rắn. Khối lượng chất rắn còn lại là
A. 5,6 gam.
B. 2,7 gam.
C. 5,4 gam.
D. 10,8 gam.
Câu 10. Thực hiện phản ứng nhiệt nhôm trong điều kiện không có không khí hỗn hợp gồm 8,1 gam Al và 16 gam \(F{e_2}{O_3}\). Nghiền nhỏ sản phẩm rồi cho tác dụng với dung dịch HCl dư thì thu được thể tích khí (đktc) là
A. 4,48 lít.
B. 7,84 lít.
C. 6,72 lít.
D. 10,08 lít.
Lời giải chi tiết
Câu 1. Chọn B.
Làm dụng cụ đun nấu vì dẫn nhiệt tốt và ít bị gỉ.
Câu 2. Chọn D.
Phản ứng cho thấy Al phản ứng với \({H_2}O\) ở nhiệt độ thường.
C sai: các kim loại trung bình tạo hiđroxit lưỡng tính cũng có thể tan trong dung dịch kiềm (Pb, Sn,... ).
Câu 3. Chọn D.
Al chỉ được điều chế bằng phương pháp điện phân nóng chảy oxit:
\(\begin{array}{l}A{l_2}{O_3} \to 2Al + \dfrac{3}{2}{O_2}\\2C + {O_2} \to 2CO\end{array}\)
Câu 4. Chọn D.
\(A{l_2}{O_3}\) đã được tinh chế kỹ trước khi điện phân.
Câu 5. Chọn D.
A, C sai: \(Al{(OH)_3}\) mới sinh ra tan trong HCl hoặc NaOH dư.
B sai: Không tạo ra \(Al{(OH)_3}\).
Câu 6. Chọn B.
\(NaAl{O_2} + C{O_2} + {H_2}O \to NaHC{O_3} + Al{(OH)_3} \downarrow \)
Câu 7. Chọn C.
Al: tan, cho bọt khí
\(2Al + 2NaOH + 2{H_2}O \to 2NaAl{O_2} + 3{H_2}\)
Mg: không tan
\(A{l_2}{O_3}\) tan, không cho khí. \(A{l_2}{O_3} + 2NaOH \to 2NaAl{O_2} + {H_2}O\)
Câu 8. Chọn B.
Al tan trong dung dịch \(F{e_2}{(S{O_4})_3}\)
\(Al{(N{O_3})_3}\,\tan trong\,{H_2}O\, \to \) tan trong mọi dung dịch dung môi nước; bị nhiệt phân sinh ra \(A{l_2}{O_3},N{O_2},{O_2}.\)
\(Al{(OH)_3}\) bị nhiệt phân tạo ra \(A{l_2}{O_3}.\)
Câu 9. Chọn C.
\(\begin{array}{l}2Na + 2{H_2}O \to 2NaOH + {H_2}\\\,\,a\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,a\,\,\,\,\,\,\,\,\,\,\,\,\;\;\;\;\;\;\;\;\dfrac{a}{2}\,\,\,\,mol\\2NaOH + 2Al + 2{H_2}O \to 2NaAl{O_2} + 3{H_2}\\\,\,\,\,\,\,\,a\,\,\,\,\,\,\,\,\,\,\,\,\,\,a\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\;\;\;\;\;\;\;\;\;\;1,5a\,\,\,\,\,mol\end{array}\)
Nhôm dư a mol; tổng \({H_2}\) sinh ra 2a mol
\( \to a = 0,4:2 = 0,2mol \to \) khối lượng chất rắn: 5,4 gam.
Câu 10. Chọn B
\(2Al + F{e_2}{O_3} \to A{l_2}{O_3} + 2Fe\)
0,3 0,1 mol
\(F{e_2}{O_3}\) dư 0,1 mol
\(\begin{array}{l}2Al + 6HCl \to 2AlC{l_3} + 3{H_2}\\0,1\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,0,15\,\,\,mol\\Fe + 2HCl \to FeC{l_2} + {H_2}\\0,2\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,0,2\,\,mol\\ \to {n_{{H_2}}} = 0,35mol(7,84\,lit).\end{array}\)

