Khi phân hủy bằng nhiệt 14,2 gam CaCO3 và MgCO3 ta thu được 3,36 lít CO2 ở đktc. Thành phần phần trăm về khối lượng các chất trong hỗn hợp đầu lần lượt là:
${n_{C{O_2}}} = \frac{{3,36}}{{22,4}} = 0,15\,\,mol$
Gọi số mol của CaCO3 và MgCO3 lần lượt là x và y mol
=> mhỗn hợp = 100x + 84y = 14,2 (1)
Phương trình hóa học:
CaCO3 $\xrightarrow{{{t^o}}}$ CaO + CO2
x mol → x mol
MgCO3 $\xrightarrow{{{t^o}}}$ MgO + CO2
y mol → y mol
$ = > {n_{C{O_2}}} = x + y = 0,15\,\,mol\,\,(2)$
Từ (1) và (2) => x = 0,1 mol; y = 0,05 mol
$ = > \% {m_{CaC{{\text{O}}_3}}} = \frac{{100.0,1}}{{14,2}}.100\% = 70,42\% ;\,\,\% {m_{MgC{O_3}}} = 29,58\% $
Cho các muối A, B, C, D là các muối (không theo tự) CaCO3, CaSO4, Pb(NO3)2, NaCl. Biết
rằng A không được phép có trong nước ăn vì tính độc hại của nó, B không độc nhưng cũng không được có trong nước ăn vì vị mặn của nó; C không tan trong nước nhưng bị phân hủy ở nhiệt ; D rất ít tan trong nước và khó bị phân hủy ở nhiệt độ cao. A, B, C và D lần lượt là
A là Pb(NO3)2 vì kim loại Pb rất độc
B là NaCl vì NaCl là muối ăn, nên có vị mặn
C là CaCO3. CaCO3 là muối không tan và dễ bị nhiệt phân hủy
CaCO3 \(\buildrel {{t^0}} \over\longrightarrow \) CaO + CO2↑
D là CaSO4. Muối CaSO4 ít tan trong nước và không bị nhiệt phân hủy.
Cho dãy các dung dịch: MgCl2, NaOH, H2SO4, CuSO4, Fe(NO3)3. Khi cho dung dịch trên tác dụng với nhau từng đôi một thì số phản ứng không xảy ra là
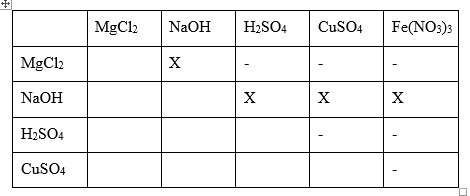
Dấu X là có phản ứng xảy ra
Dấu – là không có phản ứng xảy ra
\( \to\) có 6 cặp chất đổ vào nhau không có phản ứng xảy ra.
Trong các dung dịch sau, chất nào phản ứng được với dung dịch BaCl2 ?
Điều kiện để muối phản ứng được với dd axit hay muối khác là: sản phẩm tạo thành có chất kết tủa hoặc bay hơi ; hoặc axit tạo thành yếu hơn axit tham gia phản ứng.
BaCl2 + 2AgNO3 → Ba(NO3)2 + 2AgCl↓
Cho 1,84g hỗn hợp 2 muối ACO3 và BCO3 tác dụng hết với dung dịch HCl thu được 0,672 lít CO2 ở đktc và dung dịch X. Khối lượng muối trong dung dịch X là:
nCO2 = VCO2 : 22,4 = 0,672 : 22,4 = 0,03 mol
Gọi số mol của ACO3 và BCO3 lần lượt là x và y
ACO3 + 2HCl→ ACl2 + H2O + CO2↑ (1)
x →2x → x → x
BCO3 + 2HCl→ BCl2 + H2O + CO2↑ (2)
y →2y → y → y
Từ pt dễ dàng thấy nH2O (1) + nH2O (2) = nCO2 (1) + n CO2 (2) = x + y = nCO2 = 0,03 mol
nHCl (1) + nHCl (2) = 2nCO2 (1) + 2n CO2 (2) = 2 (x + y) = 2nCO2 = 0,06 mol
Áp dụng định luật bảo toàn khối lượng ta có
m ACO3 + mBCO3 + mHCl = mACl2 + mBCl2 + mH2O + mCO2
=> mACl2 + mBCl2 = m ACO3 + mBCO3 + mHCl – (mH2O + mCO2)
= 1,84 + 0,06 . 36,5 – (0,03 . 18 + 0,03 . 44) = 2,17g
Cho dãy chuyển hóa sau: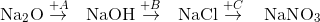 . Các chất A, B, C trong dãy trên lần lượt là:
. Các chất A, B, C trong dãy trên lần lượt là:
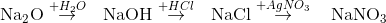
Cho dung dịch chứa 0,3 mol NaOH vào lượng dư dung dịch MgCl2, sau khi phản ứng hoàn toàn thu được a gam kết tủa. Giá trị của a là
PTHH: 2NaOH + MgCl2 → Mg(OH)2↓ + 2NaCl
Kết tủa thu được là Mg(OH)2
Theo PTHH: nMg(OH)2 = 1/2 nNaOH = 1/2 .0,3 = 0,15 (mol)
⟹ mMg(OH)2 = nMg(OH)2×MMg(OH)2 = 0,15×(24+17.2)= 8,7 (g)
Nhiệt phân một lượng MgCO3 sau một thời gian thu được chất rắn A và khí B. Hấp thụ hết khí B bằng dung dịch NaOH thu được dung dịch C. Dung dịch C vừa tác dụng được với BaCl2, vừa tác dụng với KOH. Hòa tan chất rắn A bằng dung dịch H2SO4 loãng dư thu được khí B và dung dịch D.
Xác định thành phần của D
A: MgCO3 và MgO
B: CO2
C: NaHCO3 và Na2CO3
D: MgSO4, H2SO4 dư
PTHH:
MgCO3 \(\mathrel{\mathop{\kern0pt\longrightarrow}\limits_{}^{{t^0}}} \) MgO + CO2
CO2 + 2NaOH → Na2CO3 + H2O
CO2 + NaOH → NaHCO3
BaCl2 + Na2CO3 → BaCO3↓ + 2NaCl
2NaHCO3 + 2KOH → Na2CO3 +2H2O + K2CO3
MgCO3 + H2SO4 → MgSO4 + H2O + CO2↑
MgO + H2SO4 → MgSO4 + H2O
Cô cạn từ từ 200ml dung dịch CuSO4 0,2M thu được 10 gam tinh thể CuSO4.xH2O. Tìm x ?
200 ml = 0,2 (lít)
nCuSO4 = CM. V = 0,2. 0,2 = 0,04 (mol)
Vì cô cạn chỉ là quá trình làm bay hơi nước, khối lượng CuSO4 trước và sau khi cô cạn không thay đổi.
Số mol CuSO4 trước và sau cô cạn bằng nhau.
nCuSO4.xH2O = nCuSO4 = 0,04 (mol)
=> khối lượng phân tử của CuSO4.xH2O là: \({M_{CuSO4.xH2O}} = \frac{{10}}{{0,04}} = 250\,(g/mol)\)
Ta có: 160 + 18x = 250
=> 18x = 90
=> x = 90: 18
=> x = 5
Cho từ từ đến hết 100 ml dung dịch FeCl2 0,5M vào 100 ml dung dịch AgNO3 1,2M. Sau phản ứng hoàn toàn được m gam kết tủa và dung dịch chứa các muối. Gía trị của m là?
FeCl2 + 3AgNO3 → 2AgCl↓ + Ag↓ + Fe(NO3)3
0,04 ←0,12 → 0,08 0,04 0,04
Vậy: m(kết tủa) = mAgCl + mAg = 143,5 . 0,08 + 108 . 0,04 → m = 15,8(g)
Trộn dung dịch có chứa 0,1mol CuSO4 và một dung dịch chứa 0,3 mol NaOH, lọc kết tủa, rửa sạch rồi đem nung đến khối lượng không đổi thu được m g chất rắn. Giá trị m là:
Phương trình hóa học
CuSO4 + 2NaOH → Cu(OH)2 + Na2SO4
0,1 0,2 0,1 (mol)
Cu(OH)2 → CuO + H2O
0,1 0,1 (mol)
m = mCuO = 0,1 . 80 = 8g
Hòa tan 25,9g hỗn hợp hai muối khan gồm NaCl và Na2SO4 vào nước thì thu được 200g dung dịch A. Cho dung dịch A vào dung dịch Ba(OH)2 20% vừa đủ, thấy xuất hiện 23,3g kết tủa, lọc bỏ kết tủa thu được dung dịch B. Tính khối lượng muối khan trong hỗn hợp ban đầu.
Khi cho hh muối khan gồm NaCl và Na2SO4 vào nước ta thu được dd A chứa chất tan là NaCl và Na2SO4.
Cho dd A tác dụng với dd Ba(OH)2 chỉ có dd Na2SO4 pư còn dd NaCl không phản ứng.
PTHH: Na2SO4 + Ba(OH)2 → BaSO4↓ + 2NaOH (1)
Ta có: Kết tủa thu được là BaSO4 có khối lượng 23,3 gam
\({n_{BaS{O_4}}} = \frac{{{m_{BaS{O_4}}}}}{{{M_{BaS{O_4}}}}} = \frac{{23,3}}{{137 + 32 + 16.4}} = 0,1\,(mol)\)
Theo PTHH (1): nNa2SO4 = nBaSO4 = 0,1 (mol)
→ mNa2SO4 = nNa2SO4×MNa2SO4 = 0,1×142 = 14,2 (g)
→ mNaCl = mhh – mNa2SO4 = 25,9 – 14,2 = 11,7 (g)
=> Khối lượng muối thu được sau phản ứng là: 14,2 + 11,7 = 25,9 gam.
Để hòa tan hết 5,1 g M2O3 phải dùng 43,8 g dung dịch HCl 25%. Phân tử khối của M2O3 là:
\(\eqalign{
& {m_{HCl}} = {{{m_{ddHCl}}} \over {100\% }}.C\% = {{43,8} \over {100\% }}.25\% = 10,95\,(g) \cr
& \Rightarrow {n_{HCl}} = {{{m_{HCl}}} \over {{M_{HCl}}}} = {{10,95} \over {36,5}} = 0,3\,(mol) \cr} \)
PTHH: M2O3 + 6HCl → 2MCl3 + 3H2O
0,05 ← 0,3 (mol)
Theo PTHH: nM2O3 = 1/6. nHCl = 0,3/6 = 0,05 (mol)
\( \Rightarrow {M_{{M_2}O}}_{_3} = {{{m_{{M_2}O}}_{_3}} \over {{n_{{M_2}O}}_{_3}}} = {{5,1} \over {0,05}} = 102\,(g/mol)\)
Công thức hóa học của muối natri hidrosunfat là:
Công thức hóa học của muối natri hidrosunfat là: NaHSO4
Cho Na2O vào dung dịch muối X, thu được kết tủa màu trắng. Muối X là chất nào sau đây?
Khi cho Na2O vào nước có phản ứng sau: Na2O + H2O → NaOH
A. NaCl không phản ứng với NaOH
B. FeCl3 tác dụng với NaOH sinh ta kết tủa màu nâu đỏ: FeCl3 + 3NaOH → Fe(OH)3↓ + 3NaCl
C. CuCl2 tác dụng với NaOH sinh ra kết tủa màu xanh lam: CuCl2 + 2NaOH → Cu(OH)2↓ + 2NaCl
D. MgCl2 tác dụng với NaOH sinh ra kết tủa màu trắng: MgCl2 + 2NaOH → Mg(OH)2↓ + 2NaCl
Muối nào sau đây không bị nhiệt phân hủy?
Muối cacbonat của kim loại kiềm bền nên không bị nhiệt phân hủy. Do đó, Na2CO3 không bị nhiệt phân.
Dãy muối cacbonat bị nhiệt phân ở nhiệt độ cao
Ghi nhớ: Na2CO3 và K2CO3 không bị nhiệt phân hủy
=> loại A, B, D => Chọn C
CaCO3 \(\xrightarrow{{{t^0}}}\) CaO + CO2↑
Ca(HCO3)2 \(\xrightarrow{{{t^0}}}\) CaCO3 + CO2 + H2O

