Tiết 18 .Bài 11 - AXIT PHOTPHORIC VÀ MUỐI PHOTPHAT
I. MỤC TIÊU BÀI HỌC
1. Kiến thức:
* Biết được:
- Cấu tạo phân tử, tính chất vật lí (trạng thái, màu, tính tan), ứng dụng, cách điều chế H3PO4 trong phòng thí nghiệm và trong công nghiệp.
- Tính chất của muối photphat (tính tan, tác dụng với axit, phản ứng với dung dịch muối khác), ứng dụng.
* Hiểu được H3PO4 là axit trung bình, axit ba nấc.
2. Kĩ năng:
- Viết các PTHH dạng phân tử hoặc ion rút gọn minh hoạ tính chất của axit H3PO4 và muối photphat.
- Nhận biết được axit H3PO4 và muối photphat bằng phương pháp hoá học.
- Tính khối lượng H3PO4 sản xuất được,% muối photphat trong hỗn hợp
3. Tư tưởng:
Phát huy khả năng tư duy, tinh thần học tập tích cực của học sinh.
4. Năng lực cần hướng tới :
- Năng lực chung : tự học ; giao tiếp ;hợp tác ; tư duy logic, so sánh và tổng hợp ; vận dụng kiến thức hóa học vào thực tiễn
- Năng lực riêng : tư duy hóa học ;sử dụng ngôn ngữ hóa học ;tính toán hóa học ; thực hành hóa học
II. CHUẨN BỊ CỦA GIÁO VIÊN VÀ HỌC SINH
1. Giáo Viên:
- Hóa chất : nước cất, dd Na3PO4, AgNO3, NaCl, Ca3(PO4)2, H3PO4, NaOH.
- Dụng cụ : ống nghiệm, ống hút, ống nhỏ giọt.
2. Học Sinh: Học bài cũ và đọc trước bài mới.
IV. TIẾN TRÌNH BÀI GIẢNG
1, Ổn định tổ chức : Kiểm tra sĩ số, đồng phục...
|
Lớp dạy |
|
|
Ngày dạy |
|
|
Sĩ số |
2, Kiểm tra bài cũ :
- Nêu các dạng thù hình của P và tính chất hóa học của P ? Cho ví dụ ?
- Tính chất hóa học của HNO3 ? PTHH minh họa ?
3. Bài mới:
3.1- Khởi động : Dựa vào nội dung kiểm tra bài cũ về HNO3 , GV đưa ra tình huống học tập : bài hôm nay chúng ta sẽ cùng tìm hiểu xem tính chất của H3PO4 có gì giống & khác với HNO3 ?
Hoạt động hình thành kiến thức
Hoạt động 1: Cấu tạo phân tử và tính chất vật lý
+ Bước 1: Chuyển giao nhiệm vụ học tập:
Từ kiến thức đã chuẩn bị, HS cho biết cấu tạo phân tử và tính chất vật lý của axit photphoric
+ Bước 2: Học sinh thực hiện nhiệm vụ học tập: Nhóm thực hiện.
+ Bước 3: Báo cáo kết quả và thảo luận:
HS trình bày kết quả.
Nhóm khác nghe, đánh giá, nhận xét.
+ Bước 4: Đánh giá kết quả thực hiện nhiệm vụ học tập.
GV chuẩn xác kiến thức
A. AXIT PHOTPHORIC:
I. Cấu tạo phân tử:
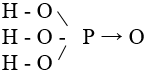
* P có : hóa trị 5 , số oxi hóa +5.
II. Tính chất vật lí:
-Tinh thể trong suốt, tnchảy → 42,50C.
- Háo nước, dễ chảy rữa, tan tốt trong nước.
- Dung dịch thường dùng đặc, sánh, không màu, C% → 85%.
Hoạt động 2: Tính chất hóa học
+ Bước 1: Chuyển giao nhiệm vụ học tập:
-Từ CTCT nêu tính chất hóa học cơ bản của H3PO4?
-Viết phương trình điện li của axit photphoric để chứng minh đó là axit ba nấc và là axit trung bình.
+ Bước 2: Học sinh thực hiện nhiệm vụ học tập: Nhóm thực hiện.
+ Bước 3: Báo cáo kết quả và thảo luận:
HS trình bày kết quả.
Nhóm khác nghe, đánh giá, nhận xét.
+ Bước 4: Đánh giá kết quả thực hiện nhiệm vụ học tập.
GV chuẩn xác kiến thức
III. Tính chất hóa học :
1. Là axit 3 nấc:
Là axit trung bình, trong nước phân li theo 3 nấc :
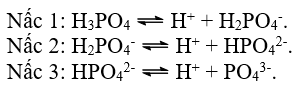
Sự phân li giảm dần từ nấc 1 đến 3.
2. Tác dụng với dd kiềm:
* Tùy theo tỷ lệ phản ứng mà thu được các sản phẩm khác nhau. VD:
H3PO4 + NaOH → NaH2PO4 + H2O.
H3PO4 + 2NaOH→ NaHPO4 + 2H2O.
H3PO4 + 3NaOH → Na3PO4 + 3H2O.
3. H3PO4 không có tính oxi hóa.
Hoạt động 3: Điều chế và ứng dụng
HS nghiên cứu sgk và tài liệu rồi tự hoàn thiện
IV. Điều chế trong CN:
Từ quặng apatit hoặc photphorit.
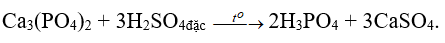
* Để được axit tinh khiết và nồng độ cao:
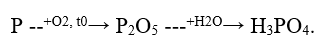
V. Ứng dụng:
- Điều chế muối photphat , sản xuất phân lân. Sản xuất thuốc trừ sâu.
- Dùng trong CN dược phẩm.
Hoạt động 4: Muối photphat
B. MUỐI PHOTPHAT
+ Bước 1: Chuyển giao nhiệm vụ học tập:
HS dựa vào bảng tính tan và SGK cho biết về các đặc điểm:
+ Tính tan.
+ Phản ứng thủy phân.
HS: Viết phản ứng xảy ra khi cho dd AgNO3 vào dd Na3PO4 ?
+ Bước 2: Học sinh thực hiện nhiệm vụ học tập: Nhóm thực hiện.
+ Bước 3: Báo cáo kết quả và thảo luận:
HS trình bày kết quả.
Nhóm khác nghe, đánh giá, nhận xét.
+ Bước 4: Đánh giá kết quả thực hiện nhiệm vụ học tập.
GV chuẩn xác kiến thức I. Khái niệm và phân loại:
* Muối photphat là muối của axit photphoric.
* VD : NaH2PO4 , NaHPO4 , Na3PO4...
* Có 3 loại : - đihdrophotphat H2PO4-.
- hidrôphtphat HPO42-.
- photphat PO43-.
II. Tính tan :
- Muối trung hòa và muối axit của Na, K, NH4+ tan tốt trong nước.
- Với các KL còn lại chỉ có muối đihdrophotphat là tan.
III. Nhận biết ion PO43-:
Thuốc thử là dd AgNO3.
PƯ: 3Ag+ + PO43- → Ag3PO4 ↓vàng
3.4,Luyện tập :
Câu 1:Nhóm nào sau đây bao gồm các muối tan ?
a.Na3PO4 , BaHPO4 , Ca3(PO4)2
b.K3PO4 , Ca(H2PO4)2 , (NH4)2HPO4
c.NaH2PO4 , Mg3(PO4)2 , K2HPO4
d.(NH4)3PO4 , Ba(H2PO4)2 , MgHPO4 .
Câu 2 : Viết PT ion rút gọn của các phản ứng sau đây (nếu có)
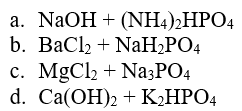
HD :
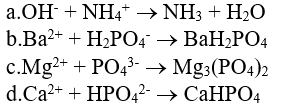
4. Củng cố bài giảng: Nội dung trọng tâm của bài :
- Viết được phương trình phân li theo từng nấc của axit H3PO4 là axit ba nấc.
- Viết được các PTHH minh họa tính chất hóa học của axit H3PO4 : tính axit, tác dụng với dd kiềm tạo ra 3 loại muối tùy theo lượng chất tác dụng.
- Tính chất của muối photphat. Nhận biết ion photphat.
5.Hướng dẫn về nhà:
- Học bài, làm bài tập SGK, chuẩn bị bài “Phân bón hoá học”; một số mẫu phân bónhoá học
- BTVN: Đổ dung dịch có chứa 11,76 g H3PO4 vào dd có chứa 16,8 g KOH. Tính khối lượng các muối thu được khi làm bay hơi dung dịch?

