I. NỘI DUNG CỦA THUYẾT CẤU TẠO HOÁ HỌC
1. Trong phân tử hợp chất hữu cơ, các nguyên tử liên kết với nhau theo đúng hoá trị và theo một thứ tự nhất định. Thứ tự liên kết đó được gọi là cấu tạo hoá học. Sự thay đổi thứ tự liên kết đó, tức là thay đổi cấu tạo hoá học, sẽ tạo ra hợp chất khác.
Ví dụ: Công thức phân tử C2H6O có hai thứ tự liên kết (2 công thức cấu tạo) ứng với 2 hợp chất sau :
H3C-O-CH3 : đimetyl ete, chất khí, không tác dụng với Na.
H3C-CH2-OH : ancol etylic, chất lỏng, tác dụng với Na giải phóng hiđro.
2. Trong phân tử hợp chất hữu cơ, cacbon có hoá trị 4. Nguyên tử cacbon không những có thể liên kết với nguyên tử của các nguyên tố khác mà còn liên kết với nhau thành mạch cacbon.
Ví dụ:
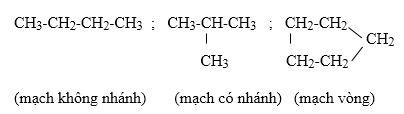
3. Tính chất của các chất phụ thuộc vào thành phần phân tử (bản chất, số lượng các nguyên tử) và cấu tạo hoá học (thứ tự liên kết các nguyên tử).
Ví dụ :
- Phụ thuộc thành phần phân tử : CH4 là chất khí dễ cháy, CCl4 là chất lỏng không cháy; CH3Cl là chất khí không có tác dụng gây mê, còn CHCl3 là chất lỏng có tác dụng gây mê.
- Phụ thuộc cấu tạo hoá học : CH3CH2OH và CH3OCH3 khác nhau cả về tính chất vật lí và tính chất hoá học.
II. HIỆN TƯỢNG ĐỒNG ĐẲNG, ĐỒNG PHÂN
1. Đồng đẳng: Những hợp chất có thành phần phân tử hơn kém nhau một hay nhiều nhóm CH2 nhưng có tính chất hoá học tương tự nhau là những chất đồng đẳng, chúng hợp thành dãy đồng đẳng.
Giải thích : Mặc dù các chất trong cùng dãy đồng đẳng có công thức phân tử khác nhau những nhóm CH2 nhưng do chúng có cấu tạo hoá học tương tự nhau nên có tính chất hoá học tương tự nhau.
Ví dụ: Các hiđrocacbon trong dãy : CH4, C2H6, C3H8, C4H10, C5H12, ..., CnH2n+2, chất sau hơn chất trước 1 nhóm CH2 nhưng đều có tính chất hoá học tương tự nhau.
2. Đồng phân: Những hợp chất khác nhau nhưng có cùng công thức phân tử là những chất đồng phân.
Giải thích : Những chất đồng phân tuy có cùng công thức phân tử nhưng có cấu tạo hoá học khác nhau, chẳng hạn etanol có cấu tạo H3C-CH2-O-H, còn đimetyl ete có cấu tạo H3C-O-CH3, vì vậy chúng là những chất khác nhau, có tính chất khác nhau.
Etanol (C2H5OH) và đimetyl ete (CH3OCH3) là 2 chất khác nhau (có tính chất khác nhau) nhưng lại có cùng công thức phân tử là C2H6O.
3. Liên kết trong phân tử hợp chất hữu cơ
a. Các loại liên kết trong phân tử hợp chất hữu cơ
- Liên kết tạo bởi 1 cặp electron dùng chung là liên kết đơn. Liên kết đơn thuộc loại liên kết s. Liên kết đơn được biểu diễn bởi 2 dấu chấm hay 1 gạch nối giữa 2 nguyên tử.
- Liên kết tạo bởi 2 cặp electron dùng chung là liên kết đôi. Liên kết đôi gồm 1 liên kết s và 1 liên kết p, biểu diễn bởi 4 dấu chấm hay 2 gạch nối.
- Liên kết tạo bởi 3 cặp electron dùng chung là liên kết ba. Liên kết ba gồm 1 liên kết s và 2 liên kết p, biểu diễn bởi 6 dấu chấm hay 3 gạch nối.
- Liên kết đôi và liên kết ba gọi chung là liên kết bội.
b. Các loại công thức cấu tạo
Công thức cấu tạo biểu diễn thứ tự và cách thức liên kết của các nguyên tử trong phân tử. Có cách viết khai triển, thu gọn và thu gọn nhất.
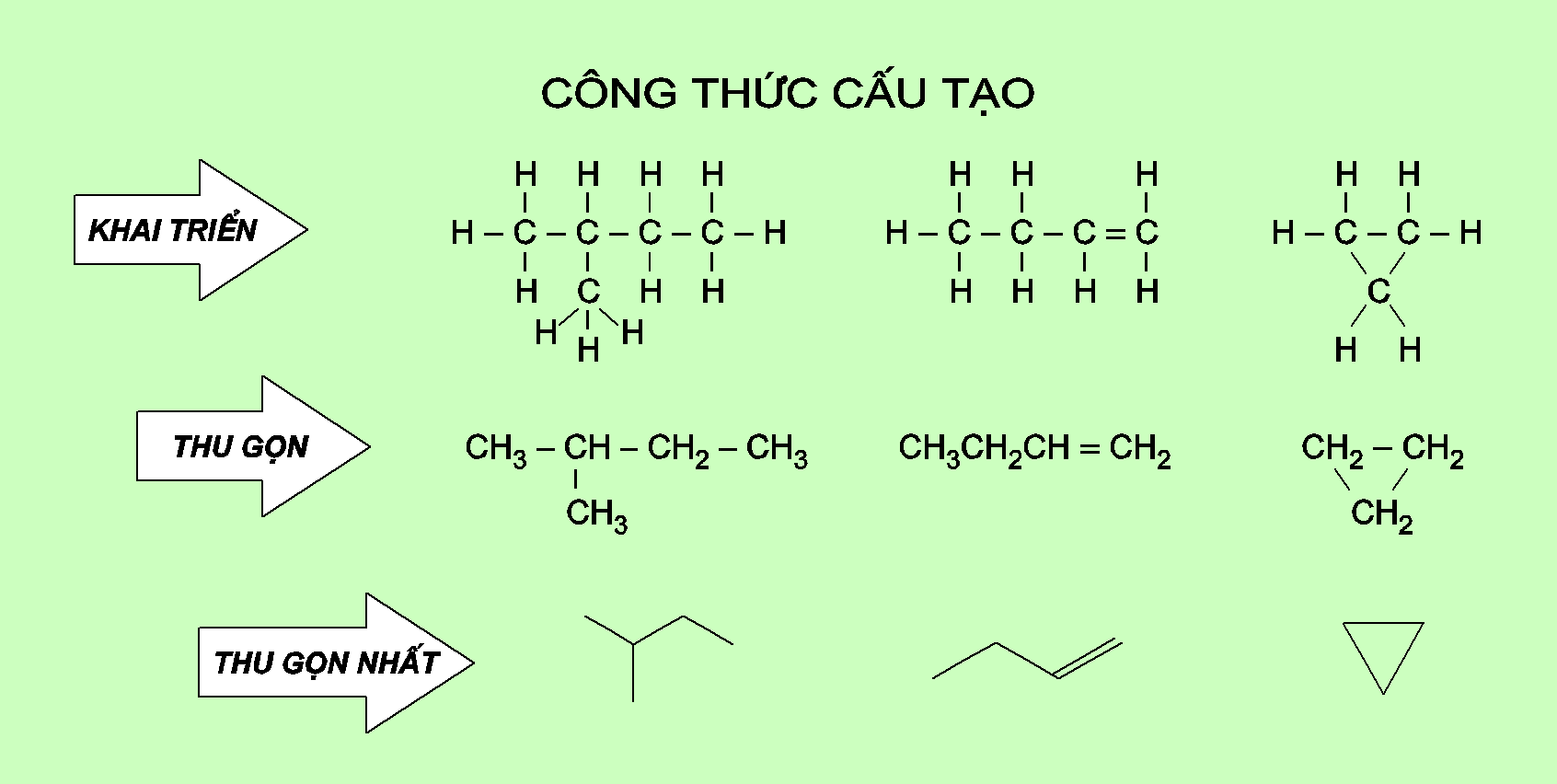
Công thức cấu tạo khai triển : Viết tất cả các nguyên tử và các liên kết giữa chúng.
Công thức cấu tạo thu gọn : Viết gộp nguyên tử cacbon và các nguyên tử khác liên kết với nó thành từng nhóm.
Công thức cấu tạo thu gọn nhất : Chỉ viết các liên kết và nhóm chức, đầu mút của các liên kết chính là các nhóm CHx với x đảm bảo hoá trị 4 ở C.
4. Đồng phân cấu tạo
a. Khái niệm : Những hợp chất có cùng công thức phân tử nhưng có cấu tạo hoá học khác nhau gọi là những đồng phân cấu tạo.
b. Phân loại đồng phân cấu tạo
- Đồng phân cấu tạo chia làm ba loại :
+ Đồng phân mạch cacbon : khác nhau về sự phân nhánh mạch cacbon
+ Đồng phân nhóm chức : khác nhau về bản chất nhóm chức
+ Đồng phân vị trí nhóm chức : khác nhau về vị trí của nhóm chức
5. Đồng phân hình học
Phân tử dạng
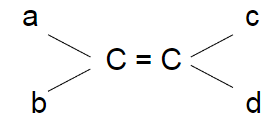
- Điều kiện để có đồng phân hình học là a ≠ b và c ≠ d
Ví dụ: CHCl=CHCl có hai cách sắp xếp không gian khác nhau dẫn tới hai chất đồng phân hình học

