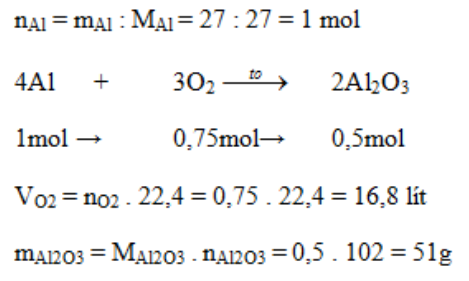Hòa tan hoàn toàn 11,2 gam sắt (Fe) trong axit clohiđric (HCl) thu được muối sắt clorua (FeCl2) và khí hiđro (H2).
a. Viết phương trình hóa học xảy ra.
b. Tính thể tích khí hiđro (H2) thu được ở điều kiện tiêu chuẩn.
c. Tính khối lượng axit clohiđric (HCl) đã tham gia phản ứng.
a. Fe + 2 HCl →FeCl2 + H2↑
b. \({n_{Fe}} = {{{m_{Fe}}} \over {{M_{Fe}}}} = {{11,2} \over {56}} = 0,2\,(mol)\)
Theo phương trình hóa học: \({n_{{H_2}}} = {n_{Fe}} = 0,2\,(mol)\)
\({V_{{H_2}(dktc)}} = {n_{{H_2}}} \times 22,4 = 0,2 \times 22,4 = 4,48\,(l)\)
c. Theo phương trình hóa học: \({n_{HCl}} = 2{n_{Fe}} = 2 \times 0,2 = 0,4\,(mol)\)
mHCl = nHCl × MHCl = 0,4 × 36,5 = 14,6 (g)
Magie tác dụng với axit clohiđric:
Mg + 2HCl → MgCl2 + H2↑
Nếu có 12g Mg tham gia phản ứng, em hãy tìm:
a) Thể tích khí hiđro thu được ở đktc.
b) Khối lượng axit clohiđric cần dùng.
Số mol của 12 g Mg là: \({n_{Mg}} = {{{m_{Mg}}} \over {{M_{Mg}}}} = {{12} \over {24}} = 0,5\,(mol)\)
PTPƯ: Mg + 2HCl → MgCl2 + H2↑
Theo PTP Ư: 1 2 1 (mol)
Theo đề bài: 0,5 x=? y = ? (mol)
a) số mol H2 sinh ra là: y = nH2 = \({{0,5 \times 1} \over 1} = 0,5\,(mol)\)
=> Thể tích của H2 thu được ở đktc là: VH2(ĐKTC) =nH2×22,4 = 0,5×22,4 = 11,2 (lít)
b) Số mol HCl phản ứng là: x = nHCl = \({{0,5 \times 2} \over 1} = 1\,(mol)\)
Khối lượng HCl tham gia phản ứng là: mHCl = nHCl×MHCl = 1. 36,5 = 36,5 (g)
Đốt cháy hoàn toàn 27 gam Al trong oxi thu được Al2O3. Tính khối lượng Al2O3 thu được và thể tích oxi (đktc) đã dùng.