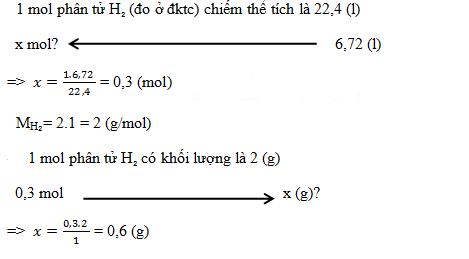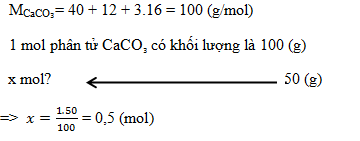Hỗn hợp X gồm 4 gam metan (CH4) và 7 gam etilen (C2H4) có thể tích là
MCH4 = MC + 4MH = 12 + 4.1 = 16 (g/mol) \( \Rightarrow {n_{C{H_4}}} = \frac{{{m_{C{H_4}}}}}{{{M_{C{H_4}}}}} = \frac{4}{{16}} = 0,25\,(mol)\)
MC2H4 = 2MC + 4MH = 2.12 + 4.1 = 28 (g/mol) \( \Rightarrow {n_{{C_2}{H_4}}} = \frac{{{m_{{C_2}{H_4}}}}}{{{M_{{C_2}{H_4}}}}} = \frac{7}{{28}} = 0,25\,(mol)\)
⟹ ∑nCH4+C2H4 = 0,25 + 0,25 = 0,5 (mol)
Thể tích của hỗn hợp X là: Vx (đktc) = ∑nCH4+C2H4 ×2,24 = 0,5×2,24 =11,2 (lít)
3,36 lít khí axetilen (C2H2) ở điều kiện tiêu chuẩn có khối lượng là
Bước 1: Tính số mol: \(n = \frac{V}{{22,4}} = \frac{{3,36}}{{22,4}} = 0,15\,(mol)\)
Bước 2: Tính phân tử khối C2H2: MC2H2 = 2MC + 6M2= 2.12 + 2.1 = 26 (g/mol)
Bước 3: Tính: mC2H2 = nC2H2×MC2H2 = 0,15×26 = 3,9 (g)
0,2 mol C2H5CHO có khối lượng là
Xét C2H5CHO = 3C + 6H + 1O = 3.12 + 6.1 + 1.16 = 58 (g/mol)
⟹ mC2H5CHO = n×M = 0,2×58 = 11,6 (g).
4,48 lít khí X ở điều kiện tiêu chuẩn chiếm số mol là
áp dụng công thức: \(n = \frac{V}{{22,4}} = \frac{{4,48}}{{22,4}} = 0,2\,(mol)\)
Biết 0,125 mol X có khối lượng 20 gam. Khối lượng mol phân tử của chất X là
áp dụng công thức: \(M = \frac{m}{n}\,\, = \frac{{20}}{{0,125}} = 160\,\,(g/mol)\)
Ở cùng điều kiện nhiệt độ và áp suất, so sánh thể tích của 4 gam CH4 và 1 gam H2 ta có:
nCH4 = 4 : 16 =0,25 mol
nH2 =0,5 mol
Vì nH2 > nCH4 nên VH2 > VCH4
1 mol khí SO2 ở điều kiện tiêu chuẩn có thể tích là:
Ở điều kiện tiêu chuẩn 1 mol khí bất kì có thể tích là 22,4 lít
Trong 16g CuSO4 có chứa bao nhiêu gam đồng?
nCuSO4 = mCuSO4 : MCuSO4 = 16 : 160 = 0,1 mol
Trong 1mol CuSO4 có 1 mol Cu
=> 0,1 mol CuSO4 có 0,1 mol Cu
=> mCu = nCu . MCu = 0,1 . 64 = 6,4g
Tính khối lượng khí H2 có trong 6,72 lít khí H₂(đo ở đktc)?

Tính số mol phân tử có trong 50 gam CaCO₃?
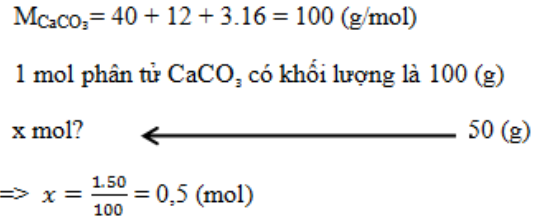
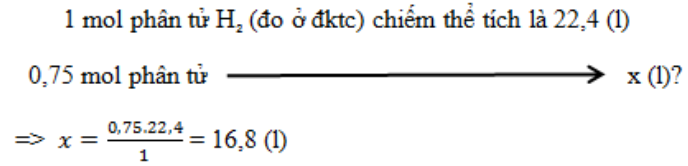
0,75 mol phân tử hyđro(đo ở đktc) chiếm thể tích bao nhiêu lít?