Lưu huỳnh đioxit có CTHH là SO2. Ta nói thành phần phân tử của lưu huỳnh đioxit gồm:
Thành phần phân tử của lưu huỳnh đioxit gồm: 1 nguyên tử lưu huỳnh và 2 nguyên tử oxi
Viết công thức hóa học của
Axit nitric (phân tử gồm 1H, 1N, 3O)
Axit nitric: HNO3
Viết công thức hóa học của
Khí gas (phân tử gồm 3C, 8H)
Khí gas: C3H8
Viết công thức hóa học của
Đá vôi (phân tử gồm 1Ca, 1C, 3O)
Đá vôi: CaCO3
Tính phân tử khối của các chất sau:
Giấm ăn (phân tử gồm 2C, 4H, 2O)
Giấm ăn C2H4O2:
MC2H4O2=2.MC+4.MH+2.MO=2.12+4.1+2.16=60 (đvC)
Tính phân tử khối của các chất sau:
Đường saccarozơ (phân tử gồm 12C, 22H, 11O)
Đường saccarozơ C12H22O11:
MC12H22O11=12.12+22.1+11.16=342 (đvC)
Tính phân tử khối của các chất sau:
Phân ure (phân tử gồm 1C, 4H, 1O, 1N)
Phân ure CH4ON:
MCH4ON=12.1+4.1+16+14=46 (đvC)
Phân tử A có phân tử khối là 64 (đvC) và được tạo bởi từ 2 nguyên tố S và O. Xác định công thức hóa học của A.
Gọi công thức hóa học của A là: SxOy
MA=x.MS+y.MO⇔64=32x+16y
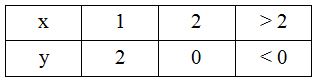
⇒x=1;y=2
⇒ công thức hóa học của A là: SO2
Phân tử X có phân tử khối là 80 (đvC) và được tạo bởi từ 2 nguyên tố Cu và O. Xác định công thức hóa học của X.
Gọi công thức hóa học của X là: CuxOy
MX=x.MCu+y.MO⇔80=64x+16y
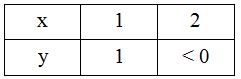
⇒x=1;y=1
⇒ công thức hóa học của X là: CuO
Hợp chất A trong phân tử gồm có 1X, 1S, 4O liên kết với nhau (X là nguyên tố chưa biết), biết nguyên tử X có khối lượng bằng 5/4 lần phân tử khí oxi. Tìm CTHH của A
Gọi công thức hóa học của A là: XSO4
Phân tử khí oxi có MO2=16.2=32 đvC
⇒MX=54.32=40 đvC => X là nguyên tố Ca
=> Công thức hóa học của hợp chất A là: CaSO4
Phân tử hợp chất A gồm 1 nguyên tử X và 3 nguyên tử H. A nặng gấp 8,5 lần khí H2. Xác định công thức hóa học của A.
Gọi công thức hóa học của A là: XH3
MA=8,5.MH2=8,5.2=17(đvC)
MA=MX+3.MH⇔17=MX+3.1
⇔MX=14(đvC) ⇒X là N
⇒ công thức hóa học của A là: NH3
Hợp chất A phân tử gồm 1 nguyên tử X và 2 nguyên tử O, phân tử A nặng gấp 22 lần khí H2. Công thức hóa học của A là
Gọi công thức hóa học của A là: XO2
MA=22.MH2=22.2=44(đvC)
MA=MX+2.MO⇔44=MX+2.16
⇔MX=12(đvC) ⇒X là C
⇒ công thức hóa học của A là: CO2
Hợp chất của nguyên tố X hóa trị II với oxi, có phân tử khối nặng gấp 1,75 lần khí oxi. Xác định công thức hóa học của hợp chất đó
Gọi công thức hóa học của hợp chất cần tìm là: IIXaIIOb
Theo quy tắc hóa trị ta có: II.a=II.b ⇔a=b=1
Công thức hóa học của hợp chất có dạng: XO
MA=1,75.MO2=1,75.32=56 (đvC)
MA=MX+MO⇔56=MX+16
⇔MX=40(đvC) ⇒ X là Ca
⇒ công thức hóa học của A là: CaO
Phân tử khối của hợp chất tạo ra từ 3 nguyên tử oxi và 2 nguyên tử R là 102 đvC. Nguyên tử khối của R là
Đặt công thức hợp chất tạo bởi 3 nguyên tử oxi và 2 nguyên tử R là R2O3
Theo bài ta có:
MR2O3=102⇒2×MR+3×16=102⇒2×MR+48=102⇒2×MR=102−48⇒2×MR=54⇒MR=542⇒MR=27(dvC)
Hợp chất Alx(NO3)3 có phân tử khối là 213. Giá trị của x là:
Theo bài ta có phương trình:
MAlx(NO3)3=213⇒x.27+(14+3.16).3=213⇒27x+62.3=213⇒27x+186=213⇒27x=27⇒x=2727⇒x=1
Hợp chất của kim loại M với nhóm PO4 có công thức là M3(PO4)2. PTK = 262. M có tên gọi và kí hiệu hóa học là:
Phân tử khối của hợp chất là 262 nên ta có phương trình
MM3(PO4)2=262⇒3×MM+(31+4×16)×2=262⇒3×MM+190=262⇒3×MM=262−190⇒3×MM=72⇒MM=723⇒MM=24(dvC)
Vậy M là Magie có kí hiệu hóa học là Mg
Hợp chất của nguyên tố X hóa trị II với oxi, có phân tử khối nặng gấp 1,75 lần khí oxi. Xác định công thức hóa học của hợp chất đó
Gọi công thức hóa học của hợp chất cần tìm là: IIXaIIOb
Theo quy tắc hóa trị ta có: II.a=II.b ⇔a=b=1
Công thức hóa học của hợp chất có dạng: XO
MA=1,75.MO2=1,75.32=56 (đvC)
MA=MX+MO⇔56=MX+16
⇔MX=40(đvC) => X là Ca
=> công thức hóa học của A là: CaO
Một hợp chất B phân tử tạo bởi một nguyên tử X kết hợp với 3 nguyên tử oxi. Phân tử khối của B gấp 2,5 lần phân tử khối của khí oxi. Phân tử khối của X và kí hiệu hóa học của X là:
Gọi công thức phân tử B là: XO3
MXO3=MX+3×MO
Mặt khác, theo bài ra MXO3=2,5×MO2=2,5×2×16=80
⇒MX+3×MO=80⇒MX=80−3×16⇒MX=32⇔MX=64−2⋅16
⇔MX=32
→ X là lưu huỳnh, có kí hiệu hóa học là S.
Công thức hóa học hợp chất của nguyên tố X với nhóm SO4 có hóa trị II là X2(SO4)3. Công thức hóa học hợp chất của nguyên tố Y với hiđro là H3Y. Công thức hóa học hợp chất của nguyên tố X và nguyên tố Y là:
Áp dụng quy tắc hóa trị cho X2 (SO4)3 ta có hóa trị của X : II.3 : 2=III
Áp dụng quy tắc hóa trị cho H3Y có hóa trị của Y : I.3 :2= III
Hợp chất tạo bới X và Y có dạng XaYb thì a.III =b.III → a : b = III : III =1:1
→ hợp chất XY
Công thức hóa học của hợp chất gồm 2 nguyên tố: Na ( I) và nhóm PO4 (III) là:
Công thức hóa học của hợp chất gồm 2 nguyên tố: Na ( I) và nhóm PO4 (III) là: Nax(PO4)y
Ta có I.x = III. y → x : y = 3: 1→ x = 3 và y =1
→ hợp chất là Na3PO4

