Kết quả:
0/29
Thời gian làm bài: 00:00:00
Cho FeS tác dụng với dung dịch H2SO4 loãng, thu được khí A; nếu dùng dung dịch H2SO4 đặc, nóng thì thu được khí B. Dẫn khí B vào dung dịch A thu được rắn C. Các chất A, B, C lần lượt là:
Để nhận biết dung dịch H2SO4 và dung dịch HCl người ta dùng
Vị trí của nguyên tố oxi trong bảng tuần hoàn hóa học là
Dung dịch NaCl bị lẫn NaI. Để làm sạch dung dịch NaCl có thể dùng:
Hệ số của O2 trong phương trình: H2S + O2 → H2O + SO2 là bao nhiêu?
Trong nhóm halogen, sự biến đổi tính chất nào sau đây của đơn chất đi từ flo đến iot là đúng ?
Chất có khả năng ăn mòn thủy tinh SiO2 là
Cho các chất rắn sau: Cr2O3, Fe(NO3)2, Al(OH)3, Mg. Số chất tan được trong dung dịch HCl loãng nguội (dư) là
Clorua vôi có công thức là:
Ion X2- có cấu hình electron lớp ngoài cùng là 2s22p6. X là nguyên tố nào sau đây?
Đơn chất vừa có tính oxi hóa vừa có tính khử là
Sục Cl2 vào nước, thu được nước clo màu vàng nhạt. Trong nước clo có chứa các chất là
Cho các chất sau: Cl2, H2, Fe(OH)2, CO2, SO2, Ag, Fe, Na. Oxi không thể phản ứng được với
Đốt cháy đơn chất X trong oxi thu được khí Y. Mặt khác, X phản ứng với H2 (khi đun nóng) thu được khí Z. Trộn hai khí Y và Z thu được chất rắn màu vàng. Đơn chất X là:
Cho các phản ứng hóa học sau:
(a) S + O2 $\xrightarrow{{{t^ \circ }}}$ SO2
(b) S + 3F2 $\xrightarrow{{{t^ \circ }}}$ SF6
(c) S + Hg $\xrightarrow{{}}$ HgS
(d) S + 6HNO3 (đặc) $\xrightarrow{{{t^ \circ }}}$ H2SO4 + 6NO2 + 2H2O
Số phản ứng trong đó S thể hiện tính khử là :
SO2 luôn thể hiện tính khử trong các phản ứng với
Thực hiện thí nghiệm điều chế clo theo sơ đồ sau:
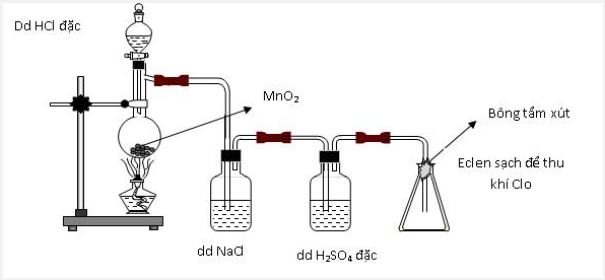
Cho các nhận định sau:
(a) Bình chứa dung dịch NaCl dùng để giữ khí HCl.
(b) Bình chứa dung dịch H2SO4 đặc để giữ hơi nước.
(c) Bông tẩm dung dịch xút có thể thay bằng tẩm nước.
(d) Có thể thay chất rắn trong bình cầu thành thuốc tím.
Số nhận định chính xác là:
Cho axit H2SO4 đặc, dư tác dụng vừa đủ với 29,25 gam NaCl đun nóng. Khí thu được hòa tan vào 73 gam H2O. Nồng độ phần trăm của HCl trong dung dịch thu được là
Nung m gam hỗn hợp KClO3 một thời gian thu được hỗn hợp chất rắn trong đó phần trăm khối lượng của oxi là 9,6%, của KCl là 74,5%. Phần trăm KClO3 bị phân hủy là:
Cho V lít khí Cl2 (đktc) vào dung dịch chứa 30gam NaI và 30,9 gam NaBr. Sau khi phản ứng xảy ra hoàn toàn thu được dung dịch Y. Cô cạn dung dịch Y thu được 33,7 gam muối khan Z. Giá trị của V và phần trăm khối lượng các muối trong Z là:
Đốt 13 gam bột một kim loại hóa trị II trong oxi dư đến khối lượng không đổi thu được chất rắn X có khối lượng 16,2 gam (giả sử hiệu suất phản ứng là 100%). Kim loại đó là
Hấp thụ hoàn toàn 6,4 gam SO2 vào dung dịch NaOH 1M, sau phản ứng thu được 11,5 gam muối. Thể tích dung dịch NaOH cần là
Nhúng thanh sắt dư vào 200 ml dung dịch chứa HCl 0,2M và mol H2SO4 0,1M đến khi phản ứng hoàn toàn thu được V lít khí. Giá trị của V là
Để khử hoàn toàn 3,04 gam hỗn hợp X gồm FeO, Fe3O4, Fe2O3, cần 0,05 mol H2. Mặt khác hoà tan hoàn toàn 3,04 gam hỗn hợp X trong dung dịch H2SO4 đặc nóng thì thu được thể tích V ml SO2 (đktc). Giá trị V(ml) là:
Hãy xác định công thức của oleum A, biết rằng khi hoà tan 3,38 gam A vào nước người ta phải dung 800 ml dung dịch KOH 0,1M để trung hòa dung dịch A
Khi nhiệt phân hoàn toàn 100 gam mỗi chất sau: KClO3 (xúc tác MnO2), KMnO4, KNO3 và AgNO3. Chất tạo ra lượng O2 lớn nhất là
Hoà tan hoàn toàn 4,0 gam hỗn hợp Mg, Fe, Cu bằng dung dịch H2SO4 đặc, nóng, dư thu được 2,24 lít khí SO2 duy nhất (đktc) và dung dịch chứa m gam muối. Giá trị của m là
Hỗn hợp a gồm Cu và CuO Hòa tan hoàn toàn 20,8 gam hỗn hợp a vào 73,5 gam dung dịch H2SO4 80% chỉ thu được dung dịch x và khí SO2 là sản phẩm khử duy nhất cho x tác dụng hoàn toàn với 900 ml dung dịch NaOH 1M sau đó lọc bỏ kết tủa được dung dịch y cô cạn y thu được chất rắn z nặng 60,8 g nồng độ phần trăm của CuSO4 trong x.
Dẫn V lít khí SO2 (đktc) vào 100 ml dung dịch Ba(OH)2 0,5 M thu được dung dịch A chỉ chứa một chất tan duy nhất và không có khí thoát ra. Thêm tiếp NaOH dư vào dung dịch A thu được m gam kết tủa. Tìm giá trị của V và m.

