Kết quả:
0/30
Thời gian làm bài: 00:00:00
Cho các phản ứng sau:
(1) NaOH + HCl → NaCl + H2O.
(2) K2CO3 + HCl → KCl + CO2 + H2O.
(3) MnO2 + HCl → MnCl2 + Cl2 + H2O.
(4) KMnO4 + HCl → KCl + MnCl2 + Cl2 + H2O.
(5) Fe + HCl→ FeCl2 + H2.
(6) HCl + CuO →CuCl2 + H2O.
Số phản ứng HCl chỉ thể hiện tính oxi hoá là:
Những hiđro halogenua có thể thu được khi cho H2SO4 đặc lần lượt tác dụng với các muối NaF, NaCl, NaBr, NaI là
Thuốc thử đặc trưng để nhận biết hợp chất halogenua trong dung dịch là
Chất nào sau đây là chất rắn ở điều kiện thường ?
Brom đơn chất được điều chế trong phòng thí nghiệm và được bảo quản trong bình kín. Trạng thái của brom đơn chất ở điều kiện thường là
Thể tích khí Cl2 (đktc) cần dùng để phản ứng hết với 7,8 gam Crom
Liên kết trong phân tử X2 (X: F, Cl, Br, I) là
Phản ứng nào sau đây chứng minh Cl2 có tính oxi hóa mạnh hơn Br2?
Cho các phản ứng sau:
\(KCl + {H_2}S{O_4} \to KHS{O_4} + HCl \uparrow \) (1)
$CaC{l_2}\xrightarrow{{dpnc}}Ca + C{l_2} \uparrow $ (2)
\(2HI + N{a_2}O \to 2NaI + {H_2}O\) (3)
\(2HBr + {H_2}S{O_4} \to B{r_2} + S{O_2} + 2{H_2}O\) (4)
\(6KI + 4{H_2}S{O_4} \to 3{I_2} + S + 3{K_2}S{O_4} + 4{H_2}O\) (5)
Số phương trình thể hiện tính khử của các ion halogen là
Chất nào sau đây là chất lỏng có màu nâu đỏ ?
Trong phòng thí nghiệm, người ta thường bảo quản dung dịch HF trong bình làm bằng
Phản ứng nào sau đây viết sai?
Nguyên tử của nguyên tố nhóm VIIA có cấu hình electron lớp ngoài cùng là
Cho dãy axit HF, HCl, HBr, HI. Theo chiều từ trái sang phải, tính chất axit biến đổi như sau:
Cho các phát biểu sau:
(1) Từ HF đến HI, tính acid tăng dần.
(2) Acid HCl thường được dùng để đánh sạch lớp oxide, hydroxide, muối carbonate bám trên bề mặt kim loại trước khi sơn, hàn, mạ điện dựa trên tính acid của HCl.
(3) Trong công nghiệp, hỗn hợp gồm KF và HF (có tỉ lệ mol tương ứng 3:1) được dùng để điện phân nóng chảy sản xuất fluorine.
(4) Acid HF phân li hoàn toàn trong nước, còn các acid HCl, HBr, HI phân li một phần trong nước.
Số phát biểu sai là
Dung dịch NaCl bị lẫn NaI. Để làm sạch dung dịch NaCl có thể dùng:
Trong các tính chất kể dưới đây, những tính chất nào chung nhất cho các đơn chất halogen
(1) Phân tử gồm 2 nguyên tử
(2) Tác dụng mạnh với nước
(3) Có tính oxi hóa
(4) Trạng thái rắn ở nhiệt độ thường
Cho các phản ứng sau:
(1) Cl2 + 2NaBr → 2NaCl + Br2
(2) Br2 + 2NaI → 2NaBr + I2
(3) Cl2 + 2NaF → 2NaCl + F2
(4) Br2 + 5Cl2 + 6H2O → 2HBrO3 + 10HCl
(5) F2 (khô) + 2NaCl(nóng chảy) → 2NaF + Cl2
(6) HF + AgNO3 → AgF + HNO3
(7) HCl + AgNO3 → AgCl + HNO3
(8) PBr3 + 3H2O → H3PO3 + 3HBr
Số phương trình hóa học viết đúng là
Trong muối NaCl có lẫn NaBr và NaI. Để loại 2 muối này ra khỏi NaCl, người ta có thể
Tính chất hóa học đặc trưng của halogen là
Cho 1,12 gam một kim loại X tác dụng với khí clorine dư thu được 3,25 gam muối. Kim loại đó là
Đốt cháy hoàn toàn 7,2 gam kim loại M (có hóa trị không đổi) trong hỗn hợp khí Cl2 và O2. Sau phản ứng thu được 23 gam chất rắn và thể tích khí đã phản ứng là 5,6 lít (đktc). Kim loại M là
Cho các giá trị nhiệt độ nóng chảy của các đơn chất halogen (không theo thứ tự) là
-7,3oC, -219,6oC, 113,6oC và -101,0oC. Dãy sắp xếp phù hợp là
Sục khí clo (Cl2) dư vào dung dịch chứa muối NaBr và KBr thu được muối NaCl và KCl, đồng thời thấy khối lượng muối giảm 4,45 gam so với ban đầu. Lượng clo (Cl2) đã tham gia phản ứng là:
Cho dung dịch chứa 6,03 gam hỗn hợp gồm hai muối NaX và NaY (X, Y là hai nguyên tố có trong tự nhiên, ở hai chu kì liên tiếp thuộc nhóm VIIA, số hiệu nguyên tử ZX < ZY) vào dung dịch AgNO3 (dư), thu được 8,61 gam kết tủa. Phần trăm khối lượng của NaY trong hỗn hợp ban đầu là
Có một hỗn hợp gồm NaCl và NaBr. Cho hỗn hợp đó tác dụng với AgNO3 dư thì tạo ra kết tủa 25,975 gam kết tủa. Mặt khác, cho hỗn hợp đó tác dụng vừa đủ với 1,12 lít khí Cl2 (ở đktc). Phần trăm về số mol của NaBr trong hỗn hợp đầu là
Thêm 78 ml dung dịch AgNO3 10% (D=1,09 g/ml) vào dung dịch có chứa 3,88 g hỗn hợp KBr và NaI. Lọc bỏ kết tủa. Nước lọc phản ứng vừa đủ với 13,3 ml dung dịch HCl 1,5 M. Phần trăm khối lượng KBr trong hỗn hợp muối ban đầu là
Cho 14,25 gam hỗn hợp NaX, NaY (X, Y là hai halogen ở hai chu kì liên tiếp) vào dung dịch AgNO3 có dư thu được 14,35 gam kết tủa. X và Y là
Cho các dung dịch sau: NaCl, KI, Mg(NO3)2, AgNO3. Chỉ dùng thuốc thử duy nhất là dung dịch HCl thì nhận biết được bao nhiêu dung dịch trên?
Cho các phản ứng sau:
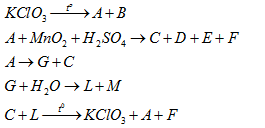
Cho các phát biểu sau:
(1) B là khí không màu, nặng hơn không khí, ít tan trong nước và duy trì sự cháy.
(2) Cả 5 phản ứng trên đều thuộc phản ứng oxi hóa – khử.
(3) 1 mol G tác dụng với nước tạo 0,5 mol khí H2.
(4) L làm quỳ ẩm chuyển màu xanh.
Số phát biểu đúng là

