I. Hiện tượng điện li
1. Thí nghiệm
Chuẩn bị ba cốc: Cốc 1 đựng nước cất, cốc 2 đựng dung dịch sacchaose C12H22O11 (nước đường), cốc 3 đựng dung dịch sodium chloride NaCl (nước muối) rồi lắp vào bộ dụng cụ như hình dưới đây.
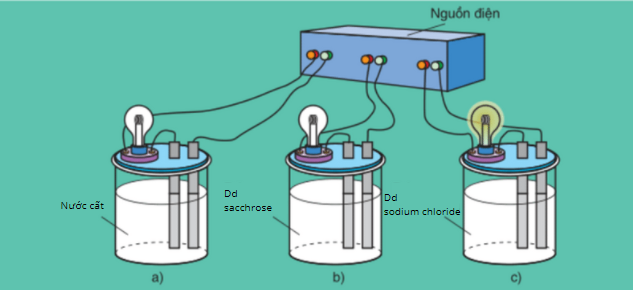
Khi nối các đầu dây dẫn điện với cùng một nguồn điện, ta chỉ thấy bóng đèn ở cốc đựng dung dịch NaCl bật sáng. Vậy dung dịch NaCl dẫn điện, còn nước cất vào dung dịch sacchaose thì không dẫn điện.
Nếu làm các thí nghiệm tương tự, người ta thấy các dung dịch acid, base và muối đều dẫn điện.
2. Nguyên nhân tính dẫn điện của dung dịch acid, base trong muối và nước
Tính dẫn điện của dung dịch acid, base và muối là do trong dung dịch của chúng có các tiểu phân mang điện tích chuyển động tự do được gọi là các ion.
Bài tập áp dụng: Dung dịch các chất điện li dẫn được điện là vì trong dung dịch có
A. các ion. B. các proton.
C. các electron. D. các đơn chất.
Lời giải: Tính dẫn điện của dung dịch acid, base và muối là do trong dung dịch của chúng có các tiểu phân mang điện tích chuyển động tự do được gọi là các ion.
=> Đáp án: A
II. Khái niệm sự điện li
- Chất dẫn điện: các acid, base, muối trong dung dịch hoặc trong trạng thái nóng chảy.
- Chất không dẫn điện: các chất rắn khan (NaCl, NaOH khan) và các dung dịch ethyl alcohol, glucose, nước cất, …
Khái niệm sự điện li và chất điện li:
- Sự điện li là quá trình phân li các chất trong nước ra ion
- Chất điện li: Những chất tan trong nước phân li thành các ion
Vậy acid, base, muối là các chất điện li.
Bài tập áp dụng:
Bài 1: Sự điện li là
A. quá trình các chất phân li trong nước sinh ra hợp chất.
B. quá trình các chất phân li trong nước sinh ra muối.
C. quá trình các chất phân li trong nước sinh ra ion.
D. quá trình các chất phân li trong nước sinh ra đơn chất.
Lời giải: Sự điện li là quá trình phân li các chất trong nước ra ion
Đáp án: C
Bài 2: Chất nào sau đây không dẫn điện được?
A. KCl rắn, khan; ethyl alcohol
B. dd muối ăn, acetic acid
C. NaOH nóng chảy, CaCl2 nóng chảy
D. HBr hòa tan trong nước, dd nước vôi trong
Lời giải: - Chất dẫn điện: các acid, base, muối trong dung dịch hoặc trong trạng thái nóng chảy.
- Chất không dẫn điện: các chất rắn khan (NaCl, NaOH khan) và các dung dịch ethyl alcohol, glucose, nước cất, …
Vậy KCl rắn, khan và ethyl alcohol không dẫn điện được.
Đáp án: A
III. Phân loại các chất điện li
1. Chất điện li mạnh
- Chất điện li mạnh là các chất khi tan trong nước phân li hoàn toàn ra ion.
Ví dụ: NaCl là chất điện li mạnh. Nếu trong dung dịch có 100 phân tử NaCl hòa tan, thì cả 100 phân tử đều phân li ra ion.
- Các chất điện li mạnh:
+ acid mạnh (HCl, H2SO4, HNO3,..)
+ base mạnh (NaOH, KOH, Ba(OH)2, Ca(OH)2,...)
+ hầu hết các muối

- Trong phương trình điện li của chất điện li mạnh, người ta dùng một mũi tên chỉ chiều của quá trình điện li:
+ với acid: HCl → H+ + Cl-
+ Với base: NaOH → Na+ + OH-
+ Với muối: Na2SO4 → 2Na+ + SO42-
2. Chất điện li yếu
- Chất điện li yếu là chất khi tan trong nước, chỉ có 1 phần số phân tử hòa tan phân li ra ion, phần còn lại vẫn tồn tại dưới dạng phân tử trong dung dịch.
- Chất điện li yếu:
+ acid yếu (H2S, CH3COOH, HF,...)
+ base yếu (Mg(OH)2,....)
+ muối HgCl2, Hg(CN)2,...

- Trong phương trình điện li của chất điện li yếu, người ta dùng hai mũi tên ngược chiều nhau.
CH3COOH ⇄
- Chất không điện li: C6H12O6, C12H22O11, C6H6, C2H5OH,...
Bài tập áp dụng:
Bài 1. Dãy chất nào sau đây, trong nước đều là chất điện li mạnh?
A. H2SO4, Cu(NO3)2, CaCl2, H2S
B. HCl, H3PO4, Fe(NO3)3, NaOH
C. HNO3, CH3COOH, BaCl2, KOH
D. H2SO4, MgCl2, Al2(SO4)3, Ba(OH)2
Lời giải: A sai vì H2S là chất điện li yếu
B sai vì H3PO4 là chất điện li yếu
C sai vì CH3COOH là chất điện li yếu
=> Đáp án: D
Bài 2. Phương trình điện li nào sau đây viết sai?
A. CH3COOH → CH3COO- + H+
B. NaCl → Na+ + Cl-
C. KOH → K+ + OH-
D. HNO3 → H+ + NO3-
Lời giải:
- A sai vì CH3COOH là chất điện li yếu nên phương trình điện li là:
C{H_3}COOH\;{\text{ }}\; \rightleftarrows \;{\text{ }}\;C{H_3}CO{O^ - }\;{\text{ }}\; + \;{\text{ }}\;{H^ + }
- B, C và D đúng vì H3PO4 là chất điện li mạnh.
=> Đáp án: A
Lưu ý: Các chất AgCl, BaSO4, Fe(OH)2,... thường được coi là không tan trong nước. Tuy nhiên thực tế vẫn có sự hòa tan một lượng rất nhỏ, phần bị hòa tan có thể phân li nên chúng vẫn được xếp vào các chất điện li.

