Cho 200 ml dung dịch H3PO4 0,3M vào 500 ml dung dịch Ba(OH)2 0,16M. Sau khi phản ứng xảy ra hoàn toàn. Khối lượng muối có phân tử khối bé hơn là
Trả lời bởi giáo viên
${n_{{H_3}P{O_4}}}$= 0,06 mol
${n_{Ba{{(OH)}_2}}}$= 0,08 mol $ \Rightarrow {n_{O{H^ - }}}$= 0,16 mol
\(\frac{{{n_{O{H^ - }}}}}{{{n_{{H_3}P{O_4}}}}} = \frac{{0,16}}{{0,06}} = 2,67\)
Ta thấy 2 < 2,67 <3 $ \Rightarrow $ Tạo 2 muối $HPO_4^{2 - }$ (x mol) và $PO_4^{3 - }$(y mol)
BT nguyên tố P: ${n_{{H_3}P{O_4}}} = {n_{HPO_4^{2 - }}} + {n_{PO_4^{3 - }}}$ => x + y = 0,06 (1)
BT điện tích: ${n_{O{H^ - }}} = 2.{n_{HPO_4^{2 - }}} + 3.{n_{PO_4^{3 - }}}$ => 2x + 3y = 0,16 (2)
Từ (1) và (2) => x = 0,02 mol; y = 0,04 mol
Ta có:
${n_{BaHP{O_4}}} = {n_{HPO_4^{2 - }}}$= 0,02 mol $ \Rightarrow $${m_{BaHP{O_4}}}$= 0,02.233 = 4,66 gam
${n_{B{a_3}{{(P{O_4})}_2}}} = \dfrac{1}{2}{n_{PO_4^{3 - }}}$= 0,02 mol $ \Rightarrow $${m_{B{a_3}{{(P{O_4})}_2}}} = $0,02.601 = 12,02 gam
Hướng dẫn giải:
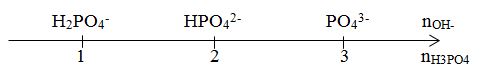
+) tỉ lệ \(\frac{{{n_{O{H^ - }}}}}{{{n_{{H_3}P{O_4}}}}}\)
+) Đối chiếu với sơ đổ quy kết muối
+) Viết PTHH, đặt ẩn giải hệ

