I. Sự tạo thành ion
- Ion dương (cation): Khi cho electron, nguyên tử trở thành ion dương
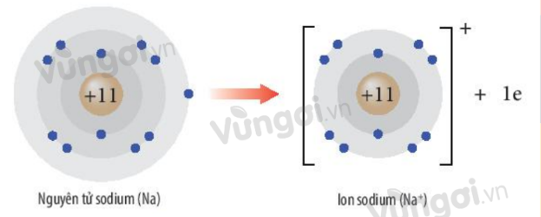
- Ion âm (anion): Khi nhận electron, nguyên tử trở thành ion âm
.png)
- Giá trị điện tích trên cation hoặc anion bằng số electron mà nguyên tử đã nhường hoặc nhận
- Ion đơn nguyên tử và ion đa nguyên tử
+ Ion đơn nguyên tử: là ion tạo nên từ 1 nguyên tử (VD: Na+, Mg2+, Cl-,…)
+ Ion đa nguyên tử: là những nhóm nguyên tử mang điện tích dương hay âm (VD: NH4+, OH-, SO42-,…)
II. Sự tạo thành liên kết ion
- Khái niệm liên kết ion: Là liên kết được hình thành bởi lực hút tĩnh điện giữa các ion mang điện tích trái dấu
- Liên kết ion thường được hình thành khi kim loại điển hình tác dụng với phi kim điển hình
Ví dụ: Khi kim loại sodium kết hợp với phi kim chlorine tạo thành các ion Na+ và Cl-, các ion này tích điện trái dấu sẽ hút nhau tạo thành liên kết ion
.png)
PTHH: \(2Na + C{l_2} \to 2NaCl\)
III. Tinh thể ion
- Cấu trúc của tinh thể ion: Các ion được sắp xếp theo một trật tự nhất định trong không gian theo kiểu mạng lưới, trong đó các nút của mạng lưới là những ion dương và ion âm được sắp xếp luân phiên, liên kết chặt chẽ với nhau do sự cân bằng giữa lực hút và lực đẩy.
.png)
- Đặc điểm của hợp chất ion:
+ Trong điều kiện thường tồn tại ở trạng thái rắn, khó nóng chảy, khó bay hơi và không dẫn điện ở trạng thái rắn
+ Thường dễ tan trong nước, tạo dung dịch có khả năng dẫn điện

