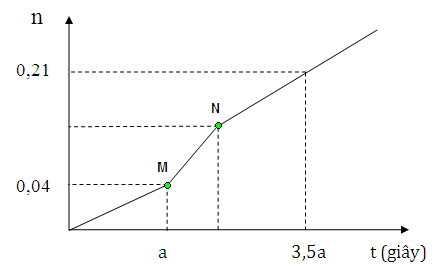
Hòa tan hoàn toàn m gam hỗn hợp CuSO4 và NaCl vào nước thu được dung dịch X. Tiến hành điện phân X với các điện cực trơ, màng ngăn xốp, dòng điện có cường độ không đổi. Tổng số mol khí thu được trên cả hai điện cực (n) phụ thuộc vào thời gian điện phân (t) được mô tả như đồ thị bên (đồ thị gấp khúc tại các điểm M, N). Giả sử hiệu suất điện phân là 100%, bỏ qua sự bay hơi của nước. Giá trị của m là
Trả lời bởi giáo viên
Đoạn 1: nCl2 = 0,04 mol
→Trong a giây mỗi điện cực đã trao đổi 0,04.2 = 0,08 mol electron.
Đoạn 2: Có độ dốc lớn hơn đoạn 1 nên tốc độ thoát khí nhanh hơn → thoát Cl2 và H2
Bảo toàn electron → nCl2 = nH2 = u
Đoạn 3: Thoát H2 và O2. Đặt nO2 = v → nH2 = 2v
Ta có hệ:
\(\left\{ \matrix{
\sum {{n_{khi}} = {n_{C{l_2}}} + {n_{{H_2}}} + {n_{{O_2}}}} \hfill \cr
\sum {n{\,_{e\,\,anot}} = 2{n_{C{l_2}}} + 4{n_{{O_2}}} = } \hfill \cr} \right. \Leftrightarrow \left\{ \matrix{
0,04 + 2u + 3v = 0,21 \hfill \cr
2(u + 0,04) + 4v = 3,5.0,08 \hfill \cr} \right. \Rightarrow \left\{ \matrix{
u = 0,04 \hfill \cr
v = 0,03 \hfill \cr} \right.\)
nCuSO4 = nCu = nCl2 đoạn 1 = 0,04 (mol)
nNaCl = 2nCl2 tổng = 2(0,04 + 0,04) = 0,16(mol)
→ m = 0,04.160 + 0,16.58,5 = 15,76 (g)
Hướng dẫn giải:
Chia đồ thị ra 3 giai đoạn
Đoạn 1: chỉ có Cl2 thoát ra ở anot
Đoạn 2: Có Cl2 và H2 bên catot thoát ra
Đoạn 3: Có H2 và O2 bên anot thoát ra
Lập phương trình với số mol khí thoát ra và số mol e trao đổi sẽ tìm ra được số mol mỗi khí Cl2, H2, O2
Từ đó suy ngược lại tìm được m =?

