Cho từ từ đến dư dung dịch KOH vào dung dịch hỗn hợp x mol HNO3 và y mol Al(NO3)3, kết quả thí nghiệm được biểu diễn trên đồ thị sau
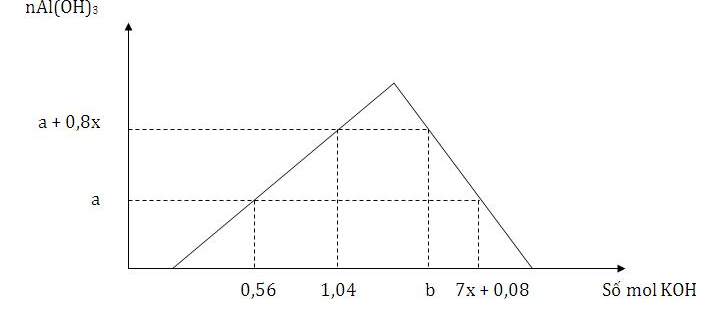
Tỉ lệ của b : a có giá trị là
Trả lời bởi giáo viên
KOH + HNO3 → KNO3 + H2O
3KOH + Al(NO3)3 → 3KNO3 + Al(OH)3
KOH + Al(OH)3 → KAlO2 + 2H2O
Xét tại các thời điểm
+) có 0,56 mol KOH thì chỉ xảy ra 2 phản ứng đầu
→ nKOH = nHNO3 + 3nAl(OH)3 = x + 3a = 0,56 mol
+) có 1,04 mol KOH thì chỉ có 2 phản ứng đầu xảy ra
→ nKOH = nHNO3 + 3nAl(OH)3 = x + 3(a + 0,8x ) =1,04
→ x = 0,2 mol và a = 0,12 mol
+) tại thời điểm b mol KOH thì xảy ra cả 3 phản ứng và thu được
nAl(OH)3 = a + 0,8x = 0,28 mol
→ nKOH = nHNO3 + 3nAl(NO3)3 + nAl(OH)3 bị hòa tan = x + 3y + (y – 0,28) =0,2 + 4y – 0,28 = 4y – 0,08 (mol) = b(1)
+) tại thời điểm (7x + 0,08) mol KOH hay 1,48 mol KOH thì nAl(OH)3 = 0,12 mol và cả 3 phản ứng xảy ra
→ nKOH = nHNO3 + 3nAl(NO3)3 + nAl(OH)3 bị hòa tan
= x + 3y + (y – 0,12) = 4y + 0,08 = 1,48 → y = 0,35 (2)
Từ (1) và (2) suy ra b = 1,32 mol
→ b : a = 1,32 : 0,12 = 11
Hướng dẫn giải:
Thứ tự xảy ra phản ứng
KOH + HNO3 → KNO3 + H2O
3KOH + Al(NO3)3 → 3KNO3 + Al(OH)3
KOH + Al(OH)3 → KAlO2 + 2H2O
Xét số mol KOH tại các thời điểm

