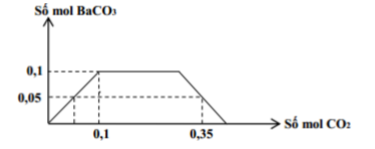
Cho m gam hỗn hợp K và Ba vào một lượng nước dư thu được dung dịch X và V lít khí (đktc). Sục từ từ đến dư khí CO2 vào dung dịch X, kết quả thí nghiệm được biểu diễn trên đồ thị như sau:
Khối lượng của K có trong m gam hỗn hợp là
Trả lời bởi giáo viên
Gọi nBa = x mol; nK = y mol
Ba + 2H2O → Ba(OH)2 + H2
x x x
2K + 2H2O → 2KOH + H2
y y 0,5y
=> nOH- = 2x + y
PT tạo kết tủa: Ba2+ + CO32- → BaCO3 ↓
Nhìn vào đồ thị ta thấy nkết tủa max = nBa2+ = x = 0,1 mol (1)
Xét \({{n}_{C{{O}_{2}}}}\) = 0,35 mol, khi đó nkết tủa = 0,05 mol = \({{n}_{CO_{3}^{2-}}}\)
Khi đó:
CO2 + 2OH- → CO32- + H2O
0,05 ← 0,1 ← 0,05
nCO2 còn lại = 0,35 – 0,05 = 0,3 mol sẽ có phản ứng:
CO2 + OH- → HCO3-
0,3 → 0,3
=> nOH- = 0,4 = 2x + y (2)
Từ (1) và (2) => x = 0,1 và y = 0,2
=> mK = 7,8
Hướng dẫn giải:
Gọi nBa = x mol; nK = y mol
+) Tính nOH- theo x và y
+) Nhìn vào đồ thị ta thấy nkết tủa max = nBa2+ => x
+) nkết tủa = \({{n}_{CO_{3}^{2-}}}\)
+) Từ số mol CO2 phản ứng => tính số mol OH-
=> x, y