Nhỏ từ từ dung dịch Ba(OH)2 vào ống nghiệm chứa dung dịch gồm HCl và Al2(SO4)3. Đồ thị biểu diễn sự phụ thuộc của khối lượng kết tủa theo thể tích dung dịch Ba(OH)2 như sau:
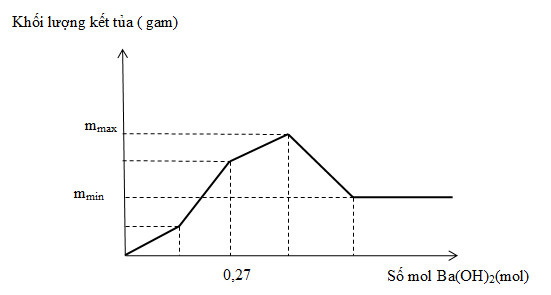
Giá trị của ( mmax – mmin) là
Trả lời bởi giáo viên
Gọi số mol của HCl là a (mol) và số mol của Al2(SO4)3 là b (mol)
=> \({{n}_{{{H}^{+}}}}=a\text{ (mol)};\text{ }{{n}_{A{{l}^{3+}}}}=2b\,(mol);\text{ }{{n}_{SO_{4}^{2-}}}=3b\text{ (mol)}\)
Khi cho Ba(OH)2 từ từ vào dung dịch hỗn hợp, trong khi Ba2+ tạo kết tủa ngay khi xuất phát thì OH- lại phải trung hòa H+ trước rồi mới tạo kết tủa sau. Do đó Ba2+ sẽ đến đích trước OH-
=> BaSO4 đạt max khi kết thúc giai đoạn thứ 2 và nBaSO4 max = 3b (mol). Lúc này Al(OH)3 mới tạo được một lượng là:
\({{n}_{Al{{(OH)}_{3}}}}=\frac{1}{3}{{n}_{O{{H}^{-}}}}=\frac{6b-a}{3}(mol)\)
=> nBa(OH)2 = 3b = 0,27
=> b = 0,09 (mol)
Kết tủa max bao gồm : \({{m}_{max}}~={{m}_{BaSO}}_{_{4}max}~+\text{ }{{m}_{Al{{\left( OH \right)}_{3}}}}_{max}\)
Kết tủa không thay đổi (đường đồ thị nằm ngang) chính là khi chỉ có kết tủa BaSO4, còn kết tủa Al(OH)3 bị hòa tan hoàn toàn.
=> mmax – mmin = mAl(OH)3 max = 2b.78 = 2.0,09.78 = 14,04 (gam)
Hướng dẫn giải:
Gọi số mol của HCl là a (mol) và số mol của Al2(SO4)3 là b (mol)
=> \({{n}_{{{H}^{+}}}}=a\text{ (mol)};\text{ }{{n}_{A{{l}^{3+}}}}=2b\,(mol);\text{ }{{n}_{SO_{4}^{2-}}}=3b\text{ (mol)}\)
Tại giá trị nBa(OH)2 = 0,27 (mol) => nBaSO4 max = 2b => b = ? (mol)
Kết tủa max bao gồm: \({{m}_{max}}~={{m}_{BaSO}}_{_{4}max}~+\text{ }{{m}_{Al{{\left( OH \right)}_{3}}}}_{max}\)
Kết tủa không thay đổi (đường đồ thị nằm ngang) chính là khi chỉ có kết tủa BaSO4, còn kết tủa Al(OH)3 bị hòa tan hoàn toàn.
=> mmax – mmin = mAl(OH)3max