Hỗn hợp X gồm FeO, Fe2O3 và Fe3O4. Cho khí CO qua m gam X nung nóng, sau một thời gian thu được hỗn hợp chất rắn Y và hỗn hợp khí Z. Cho toàn bộ Z vào dung dịch Ca(OH)2 dư, đến phản ứng hoàn toàn, thu được 4 gam kết tủa. Mặt khác, hòa tan hoàn toàn Y trong dung dịch H2SO4 đặc, nóng (dư), thu được 1,008 lít khí SO2 (đktc, sản phẩm khử duy nhất) và dung dịch chứa 18 gam muối. Giá trị của m là
Trả lời bởi giáo viên
Quy đổi hỗn hợp X ban đầu gồm Fe và O
$m\,(g)\,hh\,X\left\{ \begin{gathered}F{\text{e}}:x\,\,mol \hfill \\O:\,y\,\,mol \hfill \\ \end{gathered} \right.\xrightarrow{{CO}}$ hh rắn Y + hh khí Z $\left\{ \begin{gathered}C{O_2} \hfill \\CO \hfill \\ \end{gathered} \right.\xrightarrow{{Ca{{(OH)}_2}}}4\,\,g\,CaC{{\text{O}}_3} \downarrow $
→ ${n_{C{O_2}}} = {n_{CaC{{\text{O}}_3}}} = 0,04\,mol$ → nCO pứ = 0,04 mol
Hỗn hợp rắn Y + H2SO4 tạo muối Fe2(SO4)3
→${n_{F{{\text{e}}_2}{{(S{O_4})}_3}}} = \dfrac{{18}}{{400}} = 0,045\,mol \to {n_{F{\text{e}}}} = x = 0,09\,mol$
${n_{S{O_2}}} = \dfrac{{1,008}}{{22,4}} = 0,045\,\,mol$
Quá trình cho-nhận e:
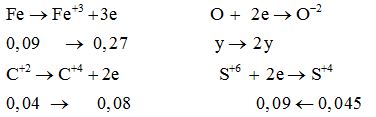
Bảo toàn e: 0,27 + 0,08 = 2y + 0,09 → y = 0,13 mol
→ mX = 56.0,09 + 16.0,13 = 7,12 g
Hướng dẫn giải:
Quy đổi hỗn hợp X ban đầu gồm Fe và O
+) ${n_{C{O_2}}} = {n_{CaC{{\text{O}}_3}}}$ → nCO pứ
Hỗn hợp rắn Y + H2SO4 tạo muối Fe2(SO4)3
→ ${n_{F{{\text{e}}_2}{{(S{O_4})}_3}}} \to {n_{F{\text{e}}}}$
+) Bảo toàn e → y
→ mX

