Hỗn hợp X gồm Al, Fe3O4 và CuO, trong đó oxi chiếm 25% khối lượng hỗn hợp. Cho 1,344 lít khí CO (đktc) đi qua m gam X nung nóng, sau một thời gian thu được chất rắn Y và hỗn hợp khí Z có tỉ khối so với H2 bằng 18. Hòa tan hoàn toàn Y trong dung dịch HNO3 loãng (dư), thu được dung dịch chứa 3,08m gam muối và 0,896 lít khí NO (ở đktc, là sản phẩm khử duy nhất). Giá trị m gần giá trị nào nhất sau đây?
Trả lời bởi giáo viên
${n_{CO}} = 0,06\,mol$; ${n_{NO}} = 0,04\,mol$
Coi hỗn hợp X gồm Al, Fe, Cu và O → m kim loại = 0,75m và mO = 0,25m
Hỗn hợp khí Z gồm CO2 và CO dư. $\overline {{M_Z}} = 36$
$ \to \% {n_{CO}} = \dfrac{{44 - 36}}{{44 - 28}} = 50\% \to {n_{CO}} = {n_{C{O_2}}} = 0,03\,\,mol$
Quá trình cho – nhận e:
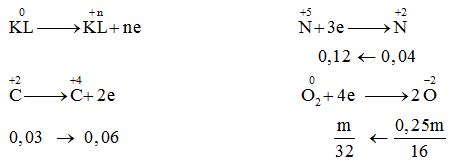
mmuối = ${m_{KL}} + {m_{N{O_3}^ - }}$ $ = 0,75m + {m_{NO_3^ - }} = 3,08m$
$ \to {m_{N{O_3}^ - }} = 2,33m$
${n_{NO_3^ - }} = 4{n_{{O_2}}} + 3{n_{NO}} - 2{n_{C{O_2}}} \to (\dfrac{m}{{32}} + 0,12 - 0,06).62 = 2,33m\,\, \to \,\,m \approx 9,48\,$
Hướng dẫn giải:
+) Coi hỗn hợp X gồm Al, Fe, Cu và O
+) Tính m kim loại và mO theo m
+) Tính số mol CO2 và CO dư
+) mmuối = ${m_{KL}} + {m_{N{O_3}^ - }}$ $ \to {m_{N{O_3}^ - }}$
+) ${n_{NO_3^ - }} = 4{n_{{O_2}}} + 3{n_{NO}} - 2{n_{C{O_2}}}$

