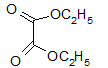
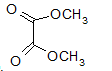
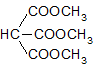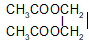Khi thủy phân hoàn toàn 0,1 mol este X tiêu tốn hết 8g NaOH. Mặt khác, khi thủy phân5,9 g este đó thì tiêu tốn hết 4g NaOH và thu được 6,8g muối. Vậy CTCT este là:
Trả lời bởi giáo viên
+ nNaOH = 0,2mol => \(\frac{{{n_{KOH}}}}{{{{\rm{n}}_{{\rm{es}}te}}}} = 2\)nKOH = 2n este => X là este 2 chức
=> CTTQ: R(COOR’)2 hoặc( RCOO)2R’
+ nNaOH = 0,1 mol
Lượng NaOH ở lần 2 giảm 1 nửa => nX (lần 2) = 0,05 mol
=> MX = 118
BTKL: meste + mKOH = mancol + m muối => mancol = 3,1g
TH1: CTTQ của X là R(COOR’)2 => nancol = 2 nX = 0,1 => Mancol = 31 loại
TH2: CTTQ của X là ( RCOO)2R’ => nancol = nX = 0,2 => Mancol = 62 => Ancol là C2H4(OH)2
=> R’ là C2H4 và R là H
=> X: (HCOO)2C2H4
Hướng dẫn giải:
Bước 1: Tính tỉ số \(\frac{{{n_{KOH}}}}{{{{\rm{n}}_{{\rm{es}}te}}}}\)=> Dạng TQ của este.
Bước 2: BTKL: meste + mKOH = m ancol + mmuối => m ancol
Bước 3: Xác định gốc hidrocacbon dựa vào khối lượng muối và ancol