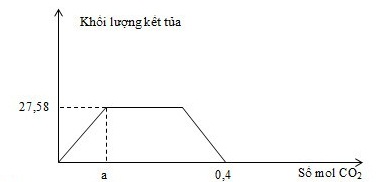
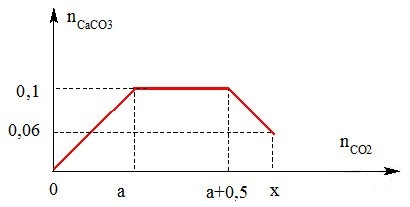
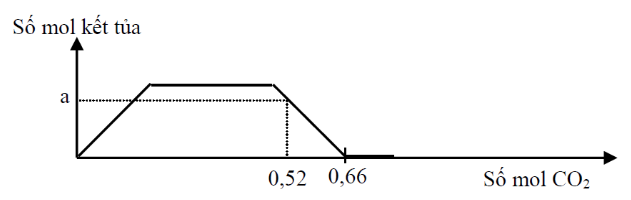
Hòa tan hết 34,6 gam hỗn hợp gồm Na, Na2O, Ba, BaO vào nước dư, thu được dung dịch X và a mol khí H2. Sục khí CO2 dư vào dung dịch X, phản ứng được biểu diễn theo sơ đồ sau:
Nếu cho 34,6 gam X tác dụng với 300 ml dung dịch H2SO4 0,4M và HCl 0,6M. Kết thúc phản ứng, thu được dung dịch Y có khối lượng tăng x gam so với dung dịch ban đầu. Giá trị của x là
Trả lời bởi giáo viên
Hỗn hợp ban đầu chứa Na (x mol); Ba (y mol) và O (z mol)
=> 23x + 137y + 16z = 34,6 (1)
Bảo toàn electron: x + 2y = 2z + 2a (2)
Trên đồ thị, khi CO2 = 0,66 thì kết tủa bị hòa tan hết => ${{n}_{HCO_{3}^{-}}}=0,66$
Bảo toàn điện tích => x + 2y = 0,66 (3)
Tại nCO2 = 0,53 thì kết tủa bị hòa tan 1 phần
${{n}_{BaC{{O}_{3}}}}=a\Rightarrow {{n}_{Ba{{\left( HC{{O}_{3}} \right)}_{2}}}}=y-a$ và ${{n}_{NaHC{{O}_{3}}}}=x$
Bảo toàn C => a + 2.(y – a) + x = 0,52 (4)
Từ (1), (2), (3), (4) => x = 0,3; y = 0,18; z = 0,19; a = 0,14
${{n}_{{{H}_{2}}S{{O}_{4}}}}=0,12\Rightarrow {{n}_{BaS{{O}_{4}}}}=0,12$
$\Delta m=34,6{-{m}_{BaS{{O}_{4}}}}-{{m}_{{{H}_{2}}}}=6,36$ => tăng 6,36 gam
Hướng dẫn giải:
Hỗn hợp ban đầu chứa Na (x mol); Ba (y mol) và O (z mol)
+) Khối lượng hỗn hợp => PT (1)
+) Bảo toàn electron => PT (2)
Trên đồ thị, khi CO2 = 0,66 thì kết tủa bị hòa tan hết => ${{n}_{HCO_{3}^{-}}}$
+) Bảo toàn điện tích => Pt (3)
Tại nCO2 = 0,53 thì kết tủa bị hòa tan 1 phần
${{n}_{BaC{{O}_{3}}}}=a\Rightarrow {{n}_{Ba{{\left( HC{{O}_{3}} \right)}_{2}}}}=y-a$ và ${{n}_{NaHC{{O}_{3}}}}=x$
+) Bảo toàn C => Pt (4)
Từ (1), (2), (3), (4) => x; y; z; a
+) $\Delta m=34,6{-{m}_{BaS{{O}_{4}}}}-{{m}_{{{H}_{2}}}}$