Hấp thụ hết 4,48 lít khí CO2 (đktc) vào dung dịch chứa x mol KOH và y mol K2CO3 thu được 200 ml dung dịch X. Cho từ từ đến hết 100 ml dung dịch X vào 300 ml dung dịch HCl 0,5M, thu được 2,688 lít khí (đktc). Mặt khác, cho 100 ml dung dịch X tác dụng với đung dịch Ba(OH)2 dư, thu được 39,4 gam kết tủa. Giá trị của x là
Trả lời bởi giáo viên
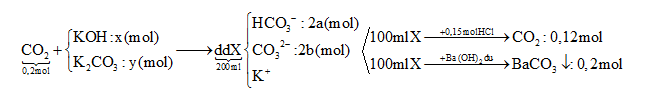
TH1: Nếu trong dd X có OH- dư => dd X chứa OH- dư, CO32-, K+
Khi cho từ từ 100 ml dd X vào 0,15 mol HCl
OH- + H+ → H2O
CO32- + 2H+ → CO2 ↑+ H2O
=> ${{n}_{{{H}^{+}}}}~={{n}_{O{{H}^{-}}}}+2{{n}_{C{{O}_{2}}}}~>0,12.2=0,24\text{ }\left( mol \right)$
=> loại vì ${{n}_{{{H}^{+}}}}=0,15\left( mol \right)$
Vậy dd X không chứa OH- dư
TH2: dd X không chứa OH- dư ta có sơ đồ bài toán như trên
Khi cho từ từ 100ml dd X vào 0,15 mol HCl có phản ứng:
HCO3- + H+ → CO2 + H2O
x → x → x (mol)
CO32- + 2H+ → CO2 + H2O
y → 2y → y (mol)
Gọi x và y là số mol khi tham gia phản ứng với HCl với tỉ lệ $\frac{x}{y}=\frac{a}{b}$
Ta có:
$\left\{ {\begin{array}{*{20}{l}}{\sum {{n_{C{O_2}}} = x + y = 0,12} }\\{\sum {{n_{HCl}} = x + 2y = 0,15} }\end{array}} \right. \Rightarrow \left\{ {\begin{array}{*{20}{l}}{x = 0,09\left( {mol} \right)}\\{y = 0,03\left( {mol} \right)}\end{array}} \right. \Rightarrow \frac{a}{b} = \frac{x}{y} = \frac{3}{1} = > a = 3b{\mkern 1mu} {\mkern 1mu} (1)$
BTNT C: ${{n}_{BaC{{O}_{3}}}}$ = a + b = 0,2 (2)
Từ (1) và (2) => a = 0,15 và b = 0,05 (mol)
Trong 200 ml dd X: ${{n}_{HCO_{3}^{-}}}~=0,3\left( mol \right);\,{{n}_{CO_{3}^{2-}}}~=0,1\left( mol \right)$
Bảo toàn điện tích đối với dd X : nK+ = 0,3 + 0,1.2 = 0,5 (mol)
BTNT C: ${{n}_{CO2(b)}}+{{n}_{{{K}_{2}}C{{O}_{3}}}}={{n}_{HCO_{3}^{-}}}+{{n}_{CO_{3}^{2-}}}~$=> 0,2 + y = 0,3 + 0,1 => y = 0,2 (mol)
BTNT K: ${{n}_{K+}}={{n}_{KOH}}+2{{n}_{{{K}_{2}}C{{O}_{3}}}}=>{{n}_{KOH}}=0,52.0,2=0,1\left( mol \right)$
=> x = 0,1 (mol)
Hướng dẫn giải:
Khi cho từ từ dd chứa HCO3- và CO32- vào dd HCl sẽ xảy ra phản ứng:
HCO3- + H+ → CO2 + H2O
CO32- + 2H+ → CO2 + H2O
Gọi x và y là số mol khi tham gia phản ứng với HCl với tỉ lệ này trùng với tỉ lệ HCO3- và CO32- ban đầu.
Bảo toàn nguyên tố C
Bảo toàn điện tích
Bảo toàn nguyên tố K