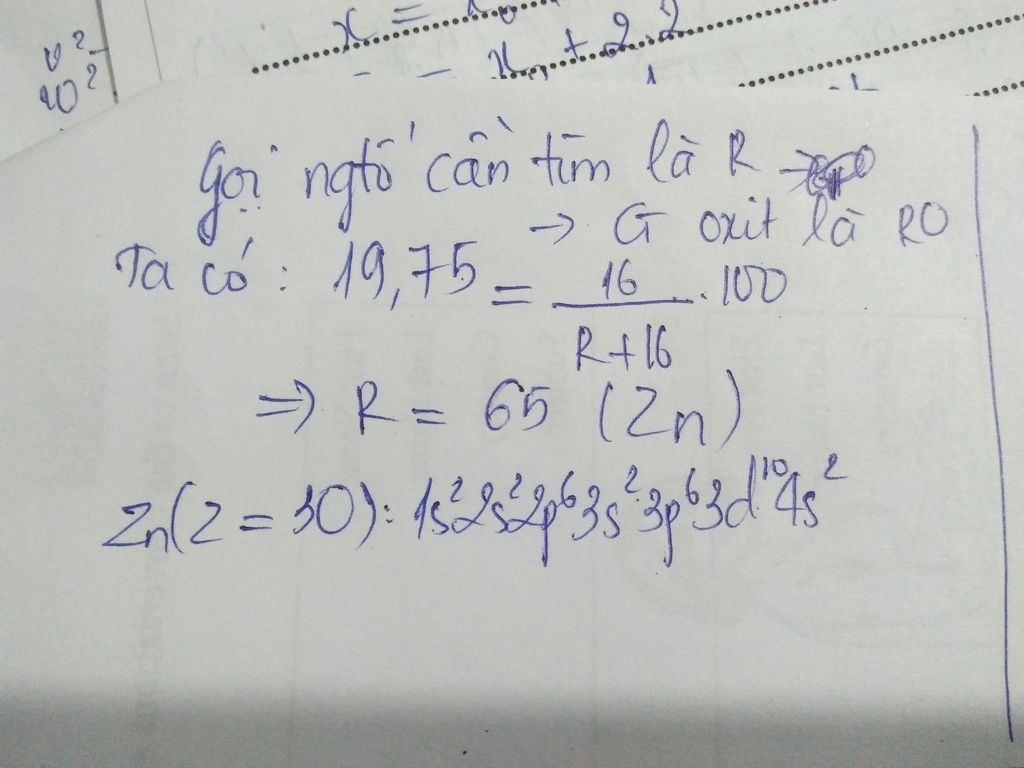Oxit của một nguyên tố nhóm 2A chứa 19,75% Oxi và khối lượng Hãy xác định nguyên tố và viết cấu hình electron của nguyên tố đó
2 câu trả lời
Đáp án:
X là Kẽm (Zn)
Zn(Z=30) có cấu hình e: 1s2 2s2 2p6 3s2 3p6 3d10 4s2
hay [Ar] 3d10 4s2
Giải thích các bước giải:
Đặt nguyên tố là X
Nguyên tố thuộc nhóm IIA => có hóa trị II trog hợp chất với oxi
=> CT oxit có dạng X2O2 rút gọn là XO
Trong công thức Oxi chiếm 19,75% về khối lượng nên ta có phương trình:
\(\eqalign{
& \% mO = {{16} \over {X + 16}}.100\% = 19,75\% \cr
& \Rightarrow 1600 = 19,75X + 316 \cr
& \Rightarrow 19,75X = 1284 \cr
& \Rightarrow X = 65 \cr} \)
X là Kẽm (Zn)
Zn(Z=30) có cấu hình e: 1s2 2s2 2p6 3s2 3p6 3d10 4s2
hay [Ar] 3d10 4s2
Chú ý: Zn thuộc nhóm IIB chứ không phải IIA nhé, chắc bạn chép nhầm