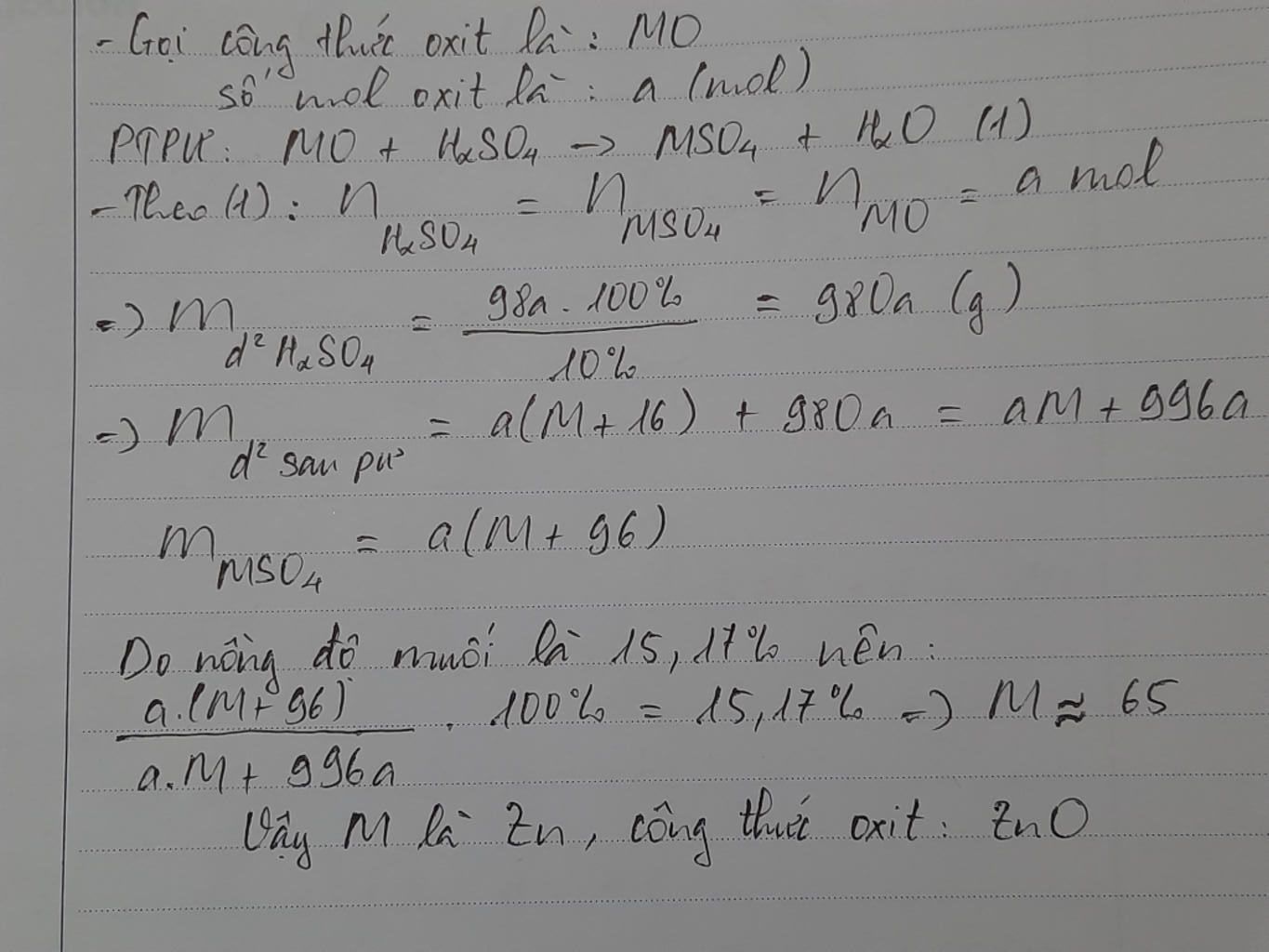Hòa tan một oxit kim loại hóa trị 2 bằng một lượng vừa đủ dung dịch H2 SO4 10% thu được dung dịch muối có nồng độ 15,17% Tìm công thức của oxit kim loại đó.
2 câu trả lời
Đáp án:Công thức oxit là ZnO
Giải thích các bước giải:
Đặt công thức oxit là AO: x (mol)
Đặt mdd H2SO4 = 100 (g) => mH2SO4 = mdd H2SO4.C%:100% = 100.10%:100% = 10 (g)
=> nH2SO4 = 10/98 (mol)
PTHH: AO + H2SO4 ---> ASO4 + H2O
\({{10} \over {98}}\) <--\({{10} \over {98}}\) ---> \({{10} \over {98}}\) (mol)
Theo PTHH: nAO = nASO4 = nH2SO4 = \({{10} \over {98}}\) (mol)
=> mAO = nAO. M AO = \({{10} \over {98}}\) (A+ 16) (g)
mASO4 = \({{10} \over {98}}\)(A + 96) (g)
Khối lượng dd sau pư là:
mdd sau = mAO + mdd H2SO4 = \({{10} \over {98}}\)(A+16) +100 (g)
Theo bài có C% ASO4 = 15,17% nên ta có:
\(\eqalign{
& C\% AS{O_4} = {{{m_{AS{O_4}}}} \over {m{\,_{dd\,AS{O_4}}}}}.100\% \cr
& \Rightarrow {{{{10} \over {98}}.(A + 96)} \over {{{10} \over {98}}.(A + 16) + 100}}.100\% = 15,17\% \cr
& \Rightarrow {{1000A + 96000} \over {10A + 160 + 9800}} = 15,17 \cr
& \Rightarrow 1000A + 96000 = 151,7A + 151093,2 \cr
& \Rightarrow 848,3A = 55093,2 \cr
& \Rightarrow A = 64,945 \approx 65 \cr} \)
=> A là kẽm (Zn)
=> Công thức oxit là ZnO