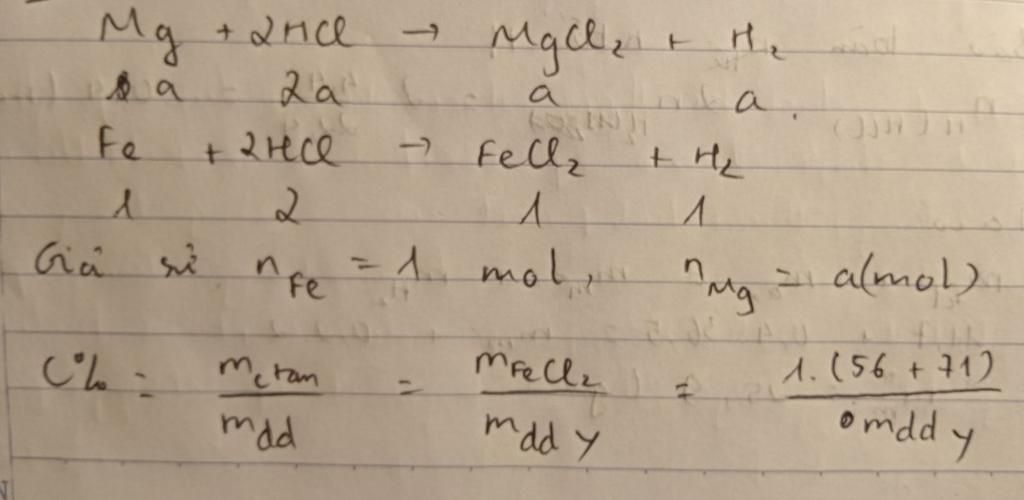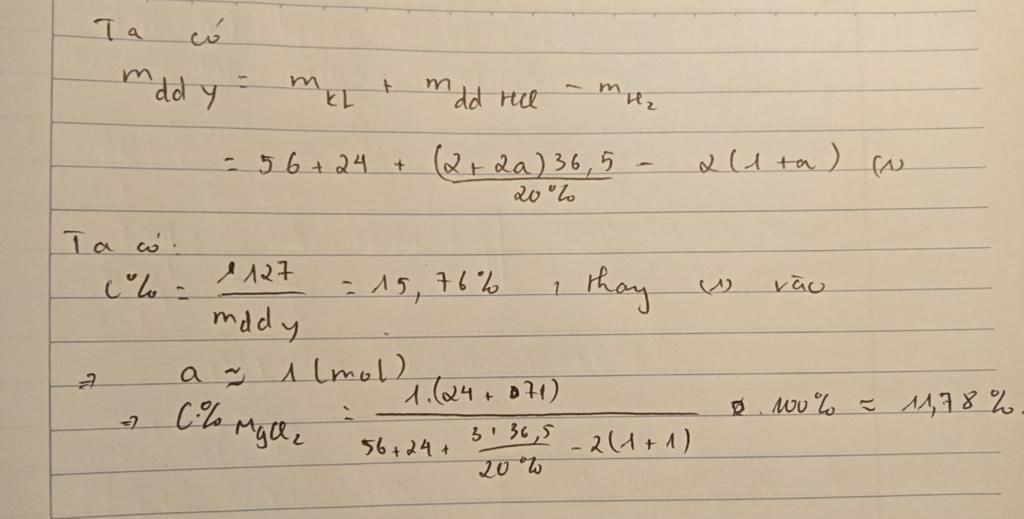Hòa tan hoàn toàn hỗn hợp X gồm Fe và Mg bằng một lượng vừa đủ dung dịch HCl 20%, thu được dung dịch Y. Nồng độ phần trăm của FeCl2 trong dung dịch Y là 15,76%. Nồng độ phần trăm của MgCl2 trong dung dịch Y là bao nhiêu phần trăm
2 câu trả lời
Đáp án:
$C\%_{MgCl_2} = 11,79\%$
Giải thích các bước giải:
Gọi số mol của $Fe,\ Mg$ lần lượt là a, b mol
PTHH:
$Fe + 2HCl \to FeCl_2 + H_2 \\ \hspace{0,2cm}a\to\hspace{0,3cm}2a\hspace{1,5cm}a\hspace{1,3cm}a\ (mol)$
$Mg + 2HCl \to MgCl_2 + H_2\\ \hspace{0,2cm}b\to\hspace{0,5cm}2b\hspace{1,7cm}b\hspace{1,4cm}b\ (mol)$
$\Rightarrow m_{\text{chất rắn X}} = 56a + 24b;\ n_{HCl} = 2a + 2b\ (mol)$
+) $m_{dd\ HCl} = \dfrac{36,5(2a+2b)}{20\%} = 365(a+b)$
Mà: $m_{FeCl_2}=127a;\ m_{MgCl_2} = 95b;\ m_{H_2} = 2a+2b\ (g)$
$\Rightarrow m_{dd\ spư} = 56a+24b+365(a+b) - 2a-2b = 419a+387b$
Theo đề bài: $C\%_{FeCl_2} = 15,76\%$
$\Rightarrow \dfrac{127a}{419a+387b}.100=15,76$
$\Rightarrow a= b$
Vậy: $C\%_{MgCl_2} = \dfrac{95}{419+387}.100=11,79\%$