Bài 6: Xu hướng biến đổi tính chất của đơn chất, biến đổi thành phần và tính chất của hợp chất trong một chu kì và trong một nhóm
Sách cánh diều
Phosphorus (P) là nguyên tố thuộc nhóm VA, chu kì 3 của bảng tuần hoàn. Cho các phát biểu sau:
(1) Nguyên tử P có 5 electron hóa trị và 8 electron p.
(2) Nguyên tử P có 3 lớp electron và có 2 electron độc thân.
(3) Công thức oxide cao nhất của P có dạng P2O5 và là acidic oxide.
(4) Hydroxide cao nhất của P có dạng H3PO4 và có tính acid.
(5) Nguyên tố P có độ âm điện thấp hơn nguyên tố có số hiệu nguyên tử là 9.
Số phát biểu đúng là
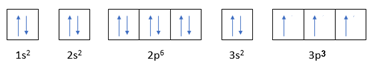
1s22s22p63s23p3
(1) sai vì có 9 electron p
(2) sai vì có 3 electron độc thân
Số hiệu nguyên tử là 9 => Nguyên tố F (F có giá trị độ âm điện lớn nhất trong các nguyên tố trong bảng tuần hoàn)
(3), (4), (5) đúng
T, Q là hai nguyên tố thuộc cùng nhóm và ở hai chu kì liên tiếp. Tổng số điện tích hạt nhân của T và Q là 58. Phát biểu nào sau đây không đúng?
Theo đề bài:
ZT +ZQ = 58 (1)
- Nếu T, Q hơn nhau 8 nguyên tố, ta có:
ZQ = ZT +8 (2)
(1) và (2) ⇒ ZT= 25, ZQ = 33.
Cấu hình electron của T: 1s2 2s2 2p6 3s2 3p6 4s2 3d5 (chu kì 4, nhóm VIIB)
Cấu hình electron của Q: 1s2 2s2 2p6 3s2 3p6 4s2 3d10 4p3 (chu kì 4, nhóm VA) (trái với giả thiết).
– Nếu T, Q hơn nhau 18 nguyên tố, ta có:
ZQ = ZT +18 (2’)
(1) và (2’) ⇒ ZT = 20, ZQ = 38.
Cấu hình electron của T: 1s2 2s2 2p6 3s2 3p64s2 (chu kì 4, nhóm IIA)
Cấu hình electron của Q: 1s2 2s2 2p6 3s2 3p6 4s2 3d10 4p6 5s2 (chu kì 5, nhóm IIA)
T, Q phù hợp.
- Nếu ZQ =ZT +32. Lí luận tương tự và kết luận không phù hợp
Nhận thấy T, Q cùng thuộc nhóm IIA nhưng khác chu kì
Trong một nhóm A theo chiều điện tích hạt nhân tăng dần tính kim loại tăng dần ⇒ T có tính kim loại nhỏ hơn Q
Oxide cao nhất của một nguyên tố R thuộc nhóm IVA, có tỉ lệ khối lượng các nguyên tố mR:mO = 3:8. Xác định nguyên tố R?
Oxide cao nhất của một nguyên tố R thuộc nhóm IVA ⇒ RO2
mR:mO = 3:8 \( \Rightarrow \dfrac{R}{{2.16}} = \dfrac{3}{8} \Rightarrow R = 12\)(C)
Cho mô hình cấu tạo của một số nguyên tố:
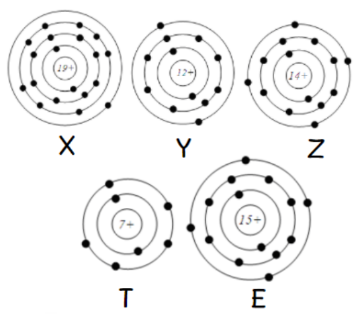
Phát biểu nào sau đây không đúng?
A đúng. Z, E có cùng 4 electron lớp ngoài cùng
B đúng vì Y, Z, E có cùng số lớp electron
C sai. Nguyên tố có 1, 2 hoặc 3 electron lớp ngoài cùng thì là kim loại => Nguyên tố X, Y
D đúng. Nguyên tố có 5, 6 hoặc 7 electron lớp ngoài cùng thì là phi kim => Nguyên tố T

