Tại sao Flo chỉ có một số oxi hóa là -1, còn các nguyên tố khác có thêm +1, +3, +5, +7?
2 câu trả lời
Đáp án:
Vì flo không có phân lớp d, nhưng clo , brom , iot lại có
Giải thích các bước giải:
-Lí do flo chỉ có số oxi hóa -1 , còn các nguyên tố halogen khác có thêm số oxi hóa +1,+3,+5,+7 là vì :
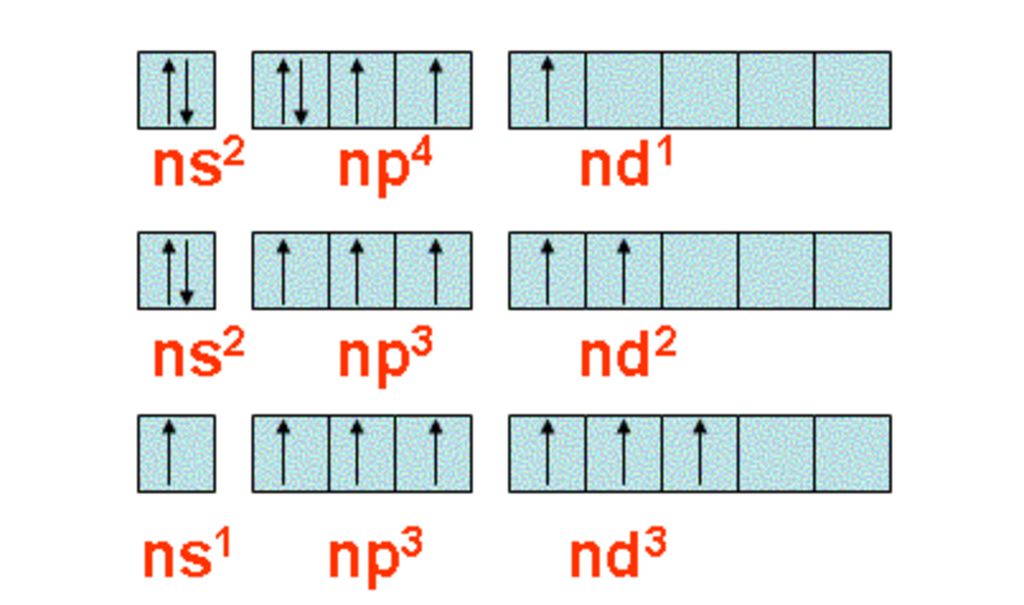
Ở trạng thái kích thích : Cl,Br,I có phân lớp d , trống nên khi được kich thích (trong phản ứng) , 1 2 hoặc 3 e có thể chuyển đến obital trống để lấp đủ các obital
Từ cấu hình e lớp ngoài cùng của các halogen là : ns$^{2}$np$^{5}$
Phân lớp tiếp theo của flo là 3s , khó có sự phân bố electron lên phân lớp này
Còn lại clo , brom , iot gần với phân lớp d dễ dàng kích thích e sang phân lớp d
Giải thích các bước giải:
* $F$ chỉ có số oxi hóa là $-1$ trong các hợp chất do $F$ là phi kim mạnh nhất nên trong phản ứng hóa học $F$ luôn nhận thêm $1e$ để trở thành $F^-$
$F+1e→F^{-1}$
* Còn các nguyên tố $Halogen$ khác ngoài số oxi hóa là $-1$ còn có các số oxi hóa: $+1;+3;+5:+7$ trong các hợp chất vì các $Halogen$ có thể nhận $e$ hay nhường $e$ trong phản ứng hóa học
$Cl+1e→Cl^{-1}$
$Cl_2^0+2NaOH→NaCl^{-1}+NaCl^{+1}O+H_2O$

