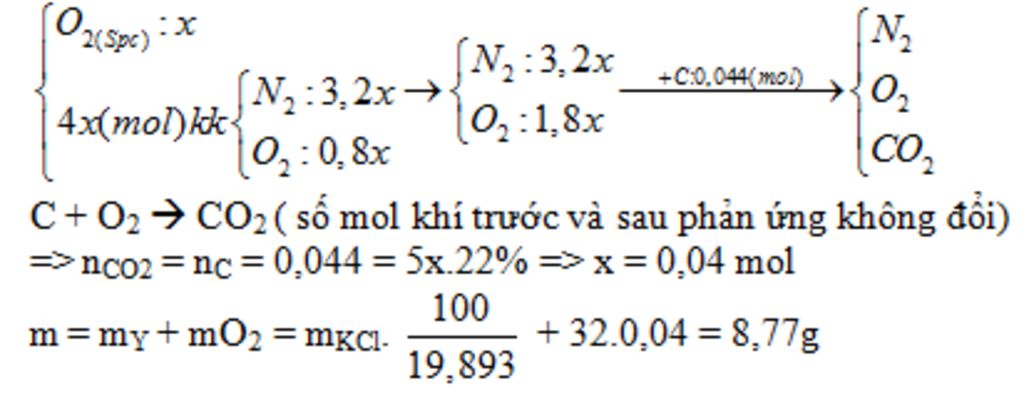Nung m gam hỗn hợp X gồm KClO3 và KMnO4 thu được chất rắn Y (KCl, K2MnO4, MnO2, KMnO4) và O2. Trong Y có 1,49 gam KCl chiếm 19,893% theo khối lượng. Trộn lượng O2 ở trên với không khí theo tỉ lệ thể tích tương ứng là 1:4 thu được hỗn hợp khí Z. Đốt cháy hết 0,528 gam cacbon bằng hỗn hợp Z thu được hỗn hợp khí T gồm 3 khí O2, N2, CO2, trong đó CO2 chiếm 22% về thể tích. Biết trong không khí có 80% N2 và 20% O2 theo thể tích. Giá trị của m là A. 8,70. B. 8,77. C. 8,91. D. 8,53.
2 câu trả lời
chọn câu b
giải thích các bước giải
ta có
X=Y+$0_2$
KCL=1,49⇒$M_Y=7,49
$N_C$=$N_CO_2$=0,044
⇒$N_T$=0,2
C+$O_2$
NÊN SỐ MOD SẼ KO THAY ĐỖI
⇒$N_T$=$N_Z$=0,2(MOD)
→$N_O2$=$\dfrac{0,2}{5}$
=0,4 MOD
⇒M=7,49+0,04.32
=8,77(GAM)
Câu hỏi trong lớp
Xem thêm