Nguyên tử của nguyên tố X có tổng các hạt cơ bản là 46 hạt, trong đó các hạt mang điện nhiều hơn các hạt không mang điện là 14 hạt. a. Tính số khối của nguyên tử X,viết kí hiệu nguyên tử của X. b. Viết cấu hình e nguyên tử của X. Cho biết X thuộc nguyên tố s, p, d, f. Giải thích?
1 câu trả lời
`a)` Ta có : số `e =` số `p=Z`
Nguyên tử của nguyên tố `X` có tổng các hạt cơ bản là `46` hạt .
`=> 2Z + N = 46` `(1)`
Các hạt mang điện nhiều hơn các hạt không mang điện là `14` hạt.
`=> 2Z - N = 14` `(2)`
Từ `(1)` và `(2)` ta có hệ phương trình :
$\begin{cases} 2Z + N = 46\\ 2 Z - N = 14 \end{cases}$
`<=>` $\begin{cases} Z = 15 \\ N = 16 \end{cases}$
`=> A = Z + N = 15 + 16 = 31`
Ký hiệu nguyên tử : ( hình ảnh )
`b)` `Z = 15`
- Cấu hình e nguyên tử của `X:` `1s^2 2s^2 2p^6 3s^2 3p^3`
- `X` thuộc nguyên tố `p` , do electron cuối cùng đặt vào phân lớp `p`
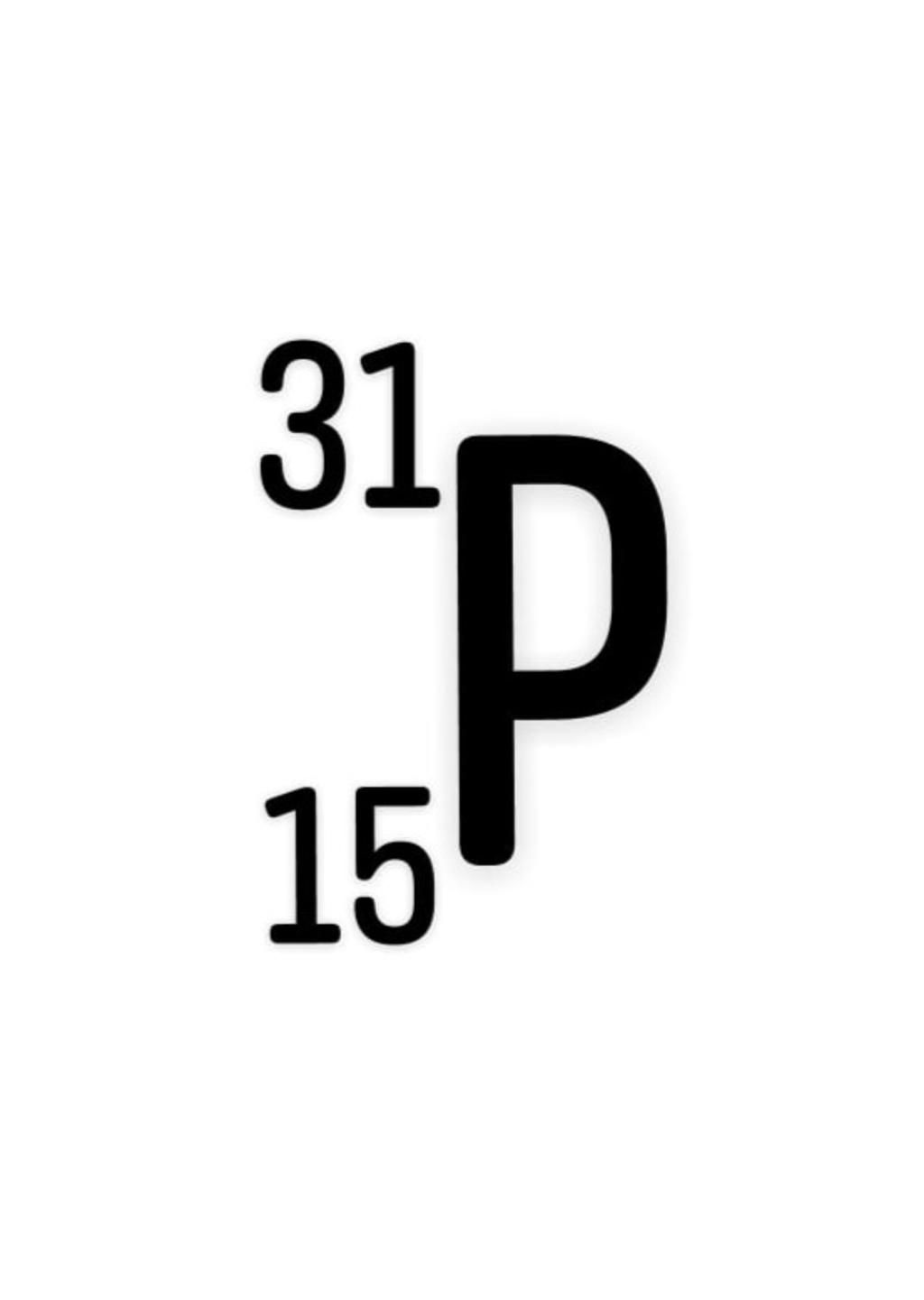
Câu hỏi trong lớp
Xem thêm

