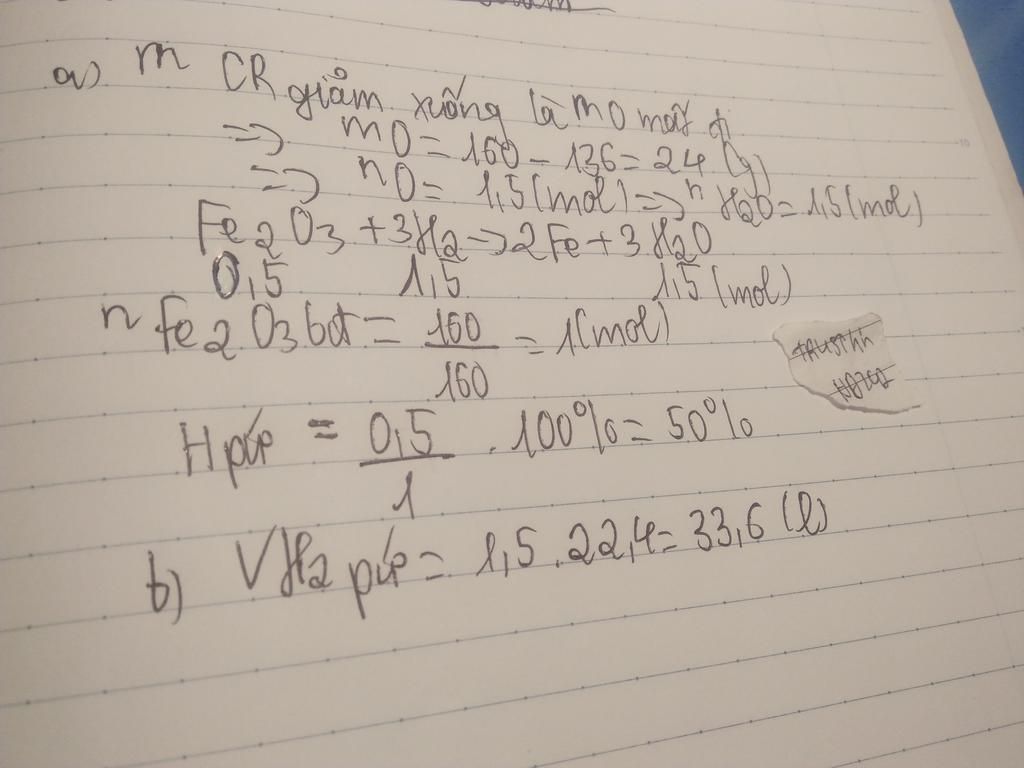mong mọi người giúp ạ dùng 4mol h2 khử 160g fe2o3 ở nhiệt độ cao thu được 136g chất rắn.tính a) tính hiệu suất b)tính Vh2 tham gia phản ứng
2 câu trả lời
Đáp án:
$a)H\%=50\%$
$b)V_{H_2(p/ứ)}=33,6(l)$
Giải thích các bước giải:
$a)PTHH:Fe_2O_3+3H_2\xrightarrow{t^o}2Fe+3H_2O$
$n_{Fe_2O_3}=\dfrac{160}{160}=1(mol)$
Đặt $n_{Fe_2O_3(p/ứ)}=x(mol)$
Theo PT: $n_{Fe}=2n_{Fe_2O_3(p/ứ)}=2x(mol)$
$\Rightarrow 160x+56.2x=136$
$\Rightarrow x=0,5(mol)$
$\Rightarrow H\%=\dfrac{n_{Fe_2O_3(p/ứ)}}{n_{Fe_2O_3}}.100\%=\dfrac{0,5}{1}.100\%=50\%$
$b)$ Theo PT: $n_{H_2(p/ứ)}=3n_{Fe_2O_3}=1,5(mol)$
$\Rightarrow V_{H_2(p/ứ)}=1,5.22,4=33,6(l)$
Câu hỏi trong lớp
Xem thêm