Đốt cháy hoàn toàn 33,6 gam fe trong 11,2 l o2 (đktc), sau phản ứng thu được chất rắn x. Tính mx
2 câu trả lời
Chúc bạn học tốt ạ
Cho mình xin ctlhn mang về cho nhóm nhé
Cảm ơn bạn
Ko hiểu đâu thì hỏi mình nhé
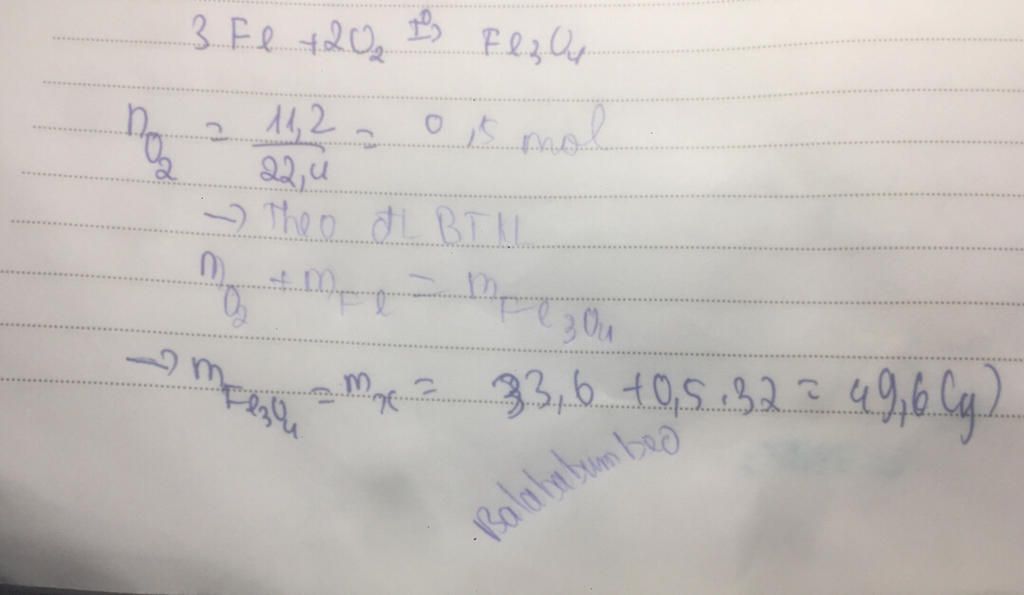
`flower`
Đáp án + Giải thích các bước giải:
Phương trình hóa học :
`3Fe+2O_2→Fe_3O_4`
Số mol `Fe` tham gia :
`n_{Fe}=m_{Fe}/M_{Fe}=(33,6)/56=0,6(mol)`
Số mol `O_2` tham gia :
`n_{O_2}=V_{O_2}/(22,4)=(11,2)/(22,4)=0,5(mol)`
Xét : `(0,6)/3<(0,5)/2`
Tính theo `Fe`
Chất rắn `x` : `Fe_3O_4`
Theo phương trình trên : `n_{Fe_3O_4}=1/3n_{Fe}=1/3 .0,6=0,2(mol)`
Số gam khối lượng chất rắn thu được :
`m_x=M_{Fe_3O_4}×n_{Fe_3O_4}=232×0,2=46,4(g)`

