Câu 1: Hòa tan hoàn toàn hỗn hợp X gồm Fe và Mg bằng một lượng vừa đủ dung dịch HCL 20% thu được dung dịch Y. Nồng độ của FeCl2 trong dung dịch Y 15,76% . Xác định nồng độ % của MgCl2 trong dung dịch Y Câu 2: Cho 3.87g hỗn hợp gồm Mg và Al tác dụng với 500ml dung dịch HCL 1M , sau khi phản ứng xảy ra hoàn toàn thu được 4,368 lít khí (đktc) a. tính % khối lượng mỗi kim loại trong hỗn hợp b. Tính nồng độ mol các chất có trong dung dịch sau phản ứng, biết thể tích dung dịch không đổi trong quá trình phản ứng c. Tính khối lượng NaCl( có 5% tạp chất) cần dùng để điều chế đủ lượng axit ở trên biết hiệu suất phản ứng điều chế là 75% Câu 3: Hòa tan hoàn toàn 9g hỗn hợp Fe và Mg vào dung dịch HCL thu được 4,48 lít khí (đktc) và dung dịch A a. Tính % khối lượng mỗi kim loại trong hỗn hợp b. Dẫn khí Clo dư vào dung dịch A, sau đó cô cạn dung dịch thì thu được bao nhiêu g chất rắn c. Dung dịch HCL ở trên có nồng độ mol là 1M (d= 0,98g g/ml) và dùng dư 30% so với lí thuyết .Tính khối lượng HCL đã dùng
1 câu trả lời
b3
a. nH2=4,48/22,4=0,2
Fe+2HCl->FeCL2+H2
Mg+2HCl->MgCl2+H2
Gọi số mol Fe và Mg là a và b
Ta có 56a+24b=9
Lại có a+b=0,2
->a=21/160; b=11/160
->%mFe=21/160.56/9=81,67%
->%mMg=100%-81,67%=18,33%
b. 2FeCL2+CL2->2FeCl3
21/160 21/160
Cô cạn dung dịch thu được FeCl3 và MgCl2
Ta có m=21/160.162,5+11/160.95=27,859375
c. nHCl phản ứng=2nH2=2.0,2=0,4mol
->nHCl ban đầu=0,4+0,4.30%=0,52mol
->VddHCl=0,52l=520ml
->Khối lượng ddHCl=520.0,98=509,6g
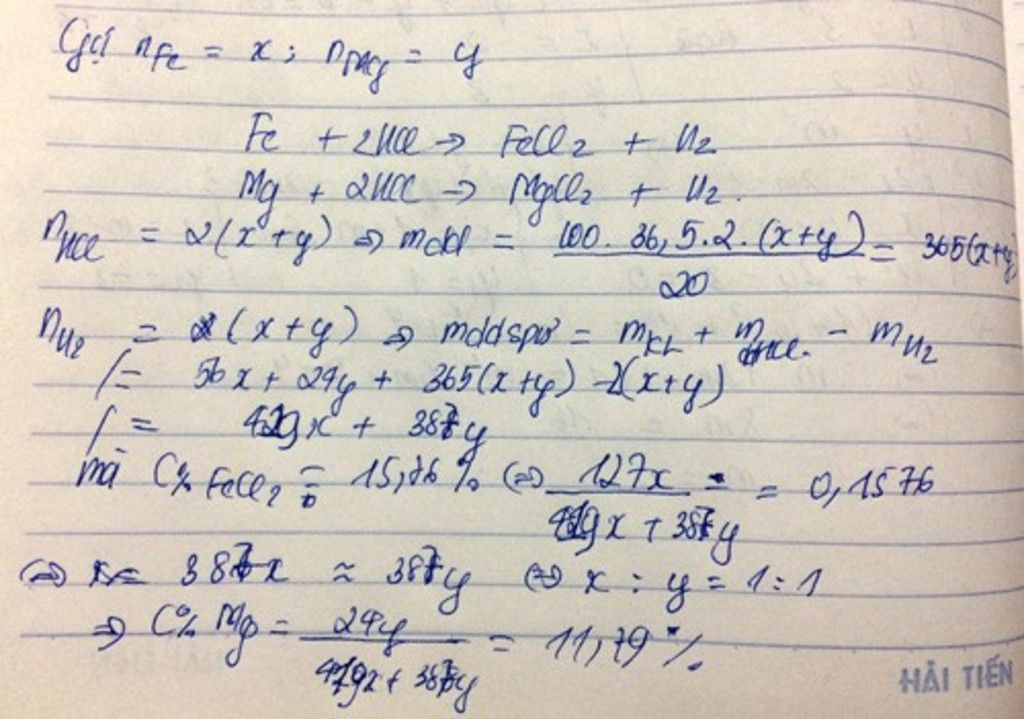
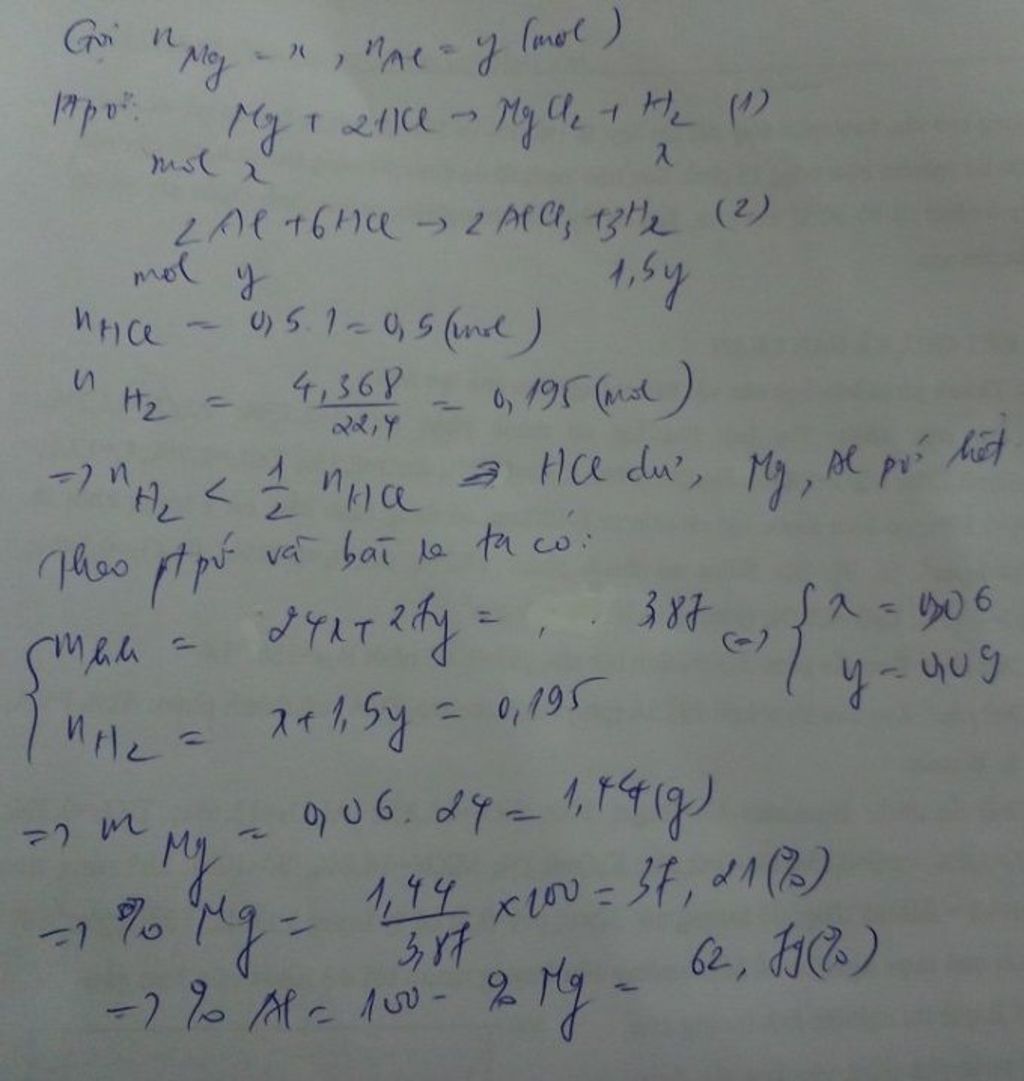
Câu hỏi trong lớp
Xem thêm

