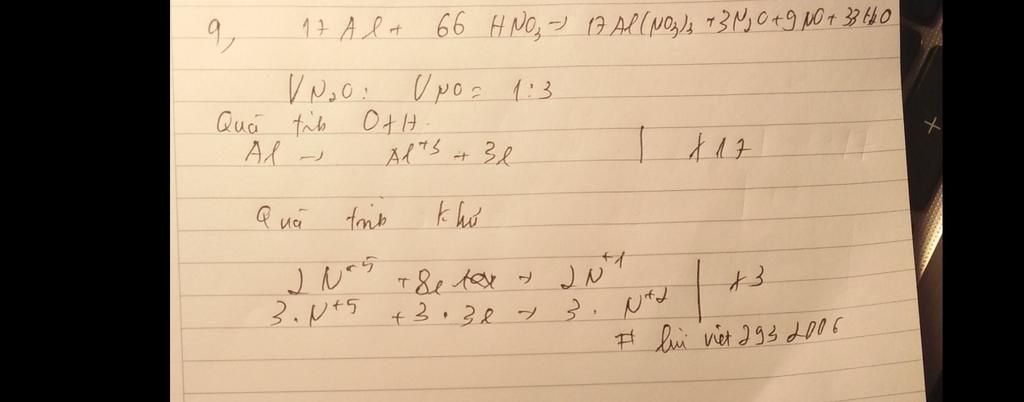Cân bằng phản ứng oxi hóa – khử bằng phương pháp thăng bằng electron g) Al + HNO3 → Al(NO3)3 + N2O + NO + H2O (Biết hỗn hợp khí tạo thành chứa 25% V N2O) h) Mg + HNO3 → Mg(NO3)2 + NO + N2 + H2O (Biết tỉ khối của hỗn hợp khí so với H2 là 14,8)
2 câu trả lời
Đáp án:
Giải thích các bước giải:
Tỉ lệ $\frac{N_2O}{NO} = \frac{25}{100-25} = \frac{1}{3}$
=> $ 3N_2O = NO$
x3 |$5N^{+5} +17e \to N^{+}_2 + 3N^{+2}$
x17|$Al^o \to Al^{+3} +3e$
$17Al + 66HNO_3 \to 17Al(NO_3)_3 + 3N_2O + 9NO + 33H_2O$
h, Giả sử hỗn hợp khí là 1 mol
Gọi số mol các chất là $n_{NO} = a $, $n_{N_2} = b $
Ta có hpt
$\begin{cases} a + b = 1 \\30a + 28b = 14,8.2 \end{cases}$
$\begin{cases} a = 0,8 \\b = 0,2 \end{cases}$
$\frac{NO}{N_2} = \frac{0,8}{0,2} = 4 $
=> $ 4N_2 = NO$
x1 |$6N^{+5} +22e \to N^{o}_2 + 4N^{+2}$
x11|$Mg^o \to Mg^{+2} +2e$
$11Mg + 28HNO_3 \to 11Mg(NO_3)_2 + N_2 + 4NO + 14H_2O$
Câu hỏi trong lớp
Xem thêm