bài 1:cho 11,2 gam Fe phản ứng với lượng dư khí Cl2 sau phản ứng thu được 19,5 gam FeCl3. tính hiệu suất của phản ứng. bài 2: nung 12,87 gam NaCl với H2SO4 đặc dư thu được bao nhiêu lít khí và bao nhiêu gam muối Na2SO4 biết hiệu suất phản ứng là 90%
2 câu trả lời
Đáp án:
1/
H=60%
2/
V HCl=4,4352lit
mNa2SO4=14,058g
Trong ảnh nha bạn
Giải thích các bước giải:
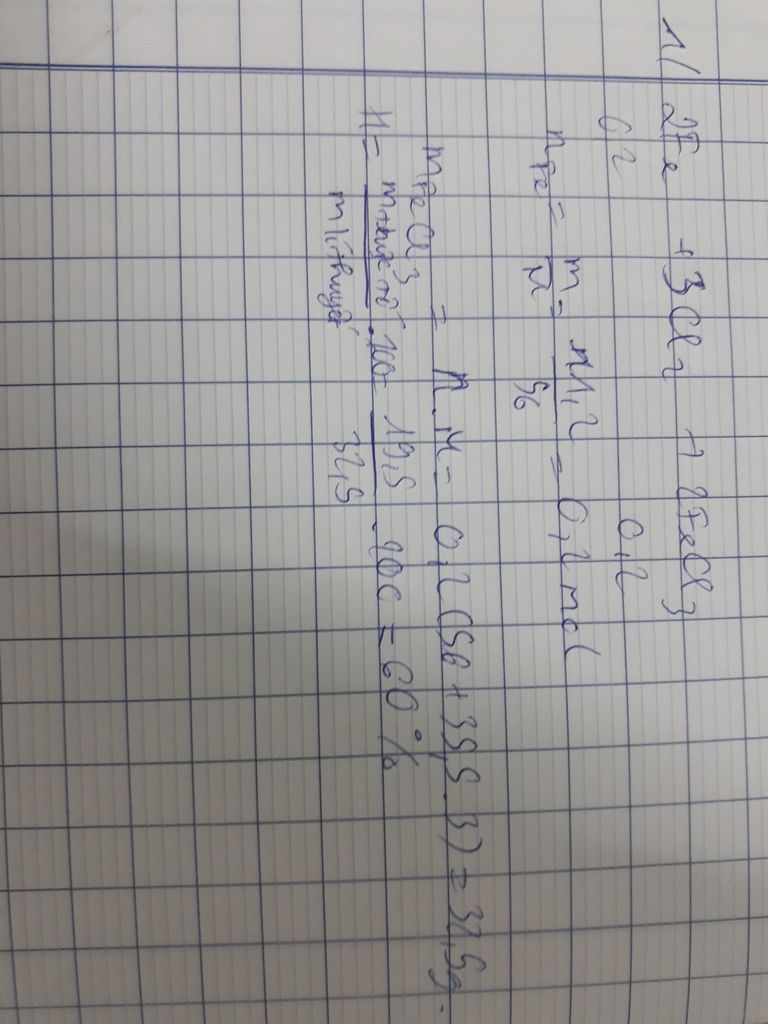

Đáp án:
1) $H\% =60\%$
2) $V_{HCl} = 4,4352\ l;\ m_{Na_2SO_4} = 14,058\ g$
Giải thích các bước giải:
Câu 1:
Ta có: $n_{Fe} = \dfrac{11,2}{56} = 0,2\ mol;\ n_{FeCl_3} = n_{Fe\ \text{pư}} = \dfrac{19,5}{162,5}=0,12\ mol$
Khi đó: $H\% = \dfrac{n_{Fe\ \text{pư}}}{n_{Fe\ \text{bđ}}}.100\%$
$\to H\% = \dfrac{0,12}{0,2}.100\%=60\%$
Câu 2:
Ta có: $n_{NaCl} = \dfrac{12,87}{58,5}=0,22\ mol$
Sơ đồ: $2NaCl \xrightarrow{H\%=90\%} Na_2SO_4\\ \hspace{0,2cm}0,22 \to \hspace{1,6cm}\dfrac{0,22}{2}.90\%=0,099(mol) $
$NaCl \xrightarrow{H\%=90\%} HCl\\ \hspace{0,2cm}0,22 \to \hspace{1,2cm}0,22.90\%=0,198(mol)$
Vậy: $V_{HCl} = 0,198.22,4 = 4,4352\ l$
$m_{Na_2SO_4} = 0,099.142 = 14,058\ g$

