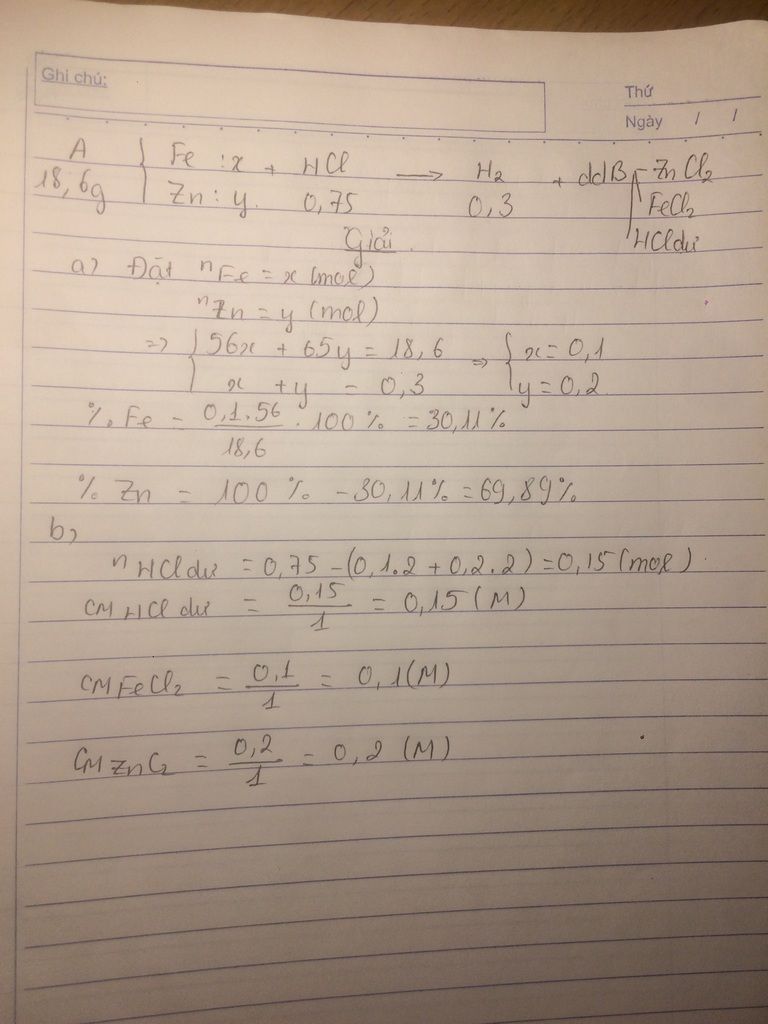4/ Cho 18,6g hỗn hợp A gồm Fe và Zn tan hoàn toàn trong 1000ml ddHCl 0,75M (lấy dư) thì thấy có 6,72 lít khí đktc bay ra và thu được dd B a/ tính % khối lượng mỗi kim loại trong hỗn hợp A b/ Tính nồng độ mol các chất trong dd B xem thể tích dd ko thay đổi sau phản ứng
2 câu trả lời
Đáp án:
a) $\eqalign{
& \% {m_{Fe}} = 30,11\% \cr
& \% {m_{Zn}} = 69,89\% \cr} $
b) CM (FeCl2) = 0,1 (M)
CM (ZnCl2) = 0,2 (M)
CM (HCl dư) = 0,15 (M)
Giải thích các bước giải:
a) nHCl = 0,75 . 1 = 0,75 mol
nH2 = 6,72 : 22,4 = 0,3 mol
HCl dư nên hỗn hợp A tan hết
Gọi số mol Fe, Zn trong A là x, y
mA = mFe + mZn
→ 56x + 65y = 18,6 (1)
Fe + 2HCl → FeCl2 + H2↑
x → 2x → x → x
Zn + 2HCl → ZnCl2 + H2↑
y → 2y → y → y
nH2 = x + y = 0,3 mol (2)
Từ (1) và (2) → x = 0,1; y = 0,2
$\eqalign{
& \% {m_{Fe}} = {{0,1.56} \over {18,6}}.100\% = 30,11\% \cr
& \% {m_{Zn}} = 100\% - 30,11\% = 69,89\% \cr} $
b) Dung dịch B gồm: FeCl2 (0,1 mol)
ZnCl2 (0,2 mol)
HCl (0,75 - 0,1 . 2 - 0,2 . 2 = 0,15 mol)
CM (FeCl2) = 0,1 : 1 = 0,1 (M)
CM (ZnCl2) = 0,2 : 1 = 0,2 (M)
CM (HCl dư) = 0,15 : 1 = 0,15 (M)