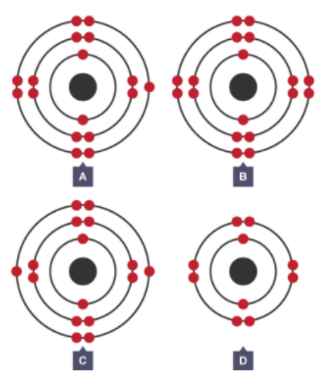
Mô hình dưới dây biểu diễn sự sắp xếp electron của nguyên tử nguyên tố X đến nguyên tố T ở trạng thái cơ bản

Cho các phát biểu sau:
(a) Cả 4 nguyên tố đều thuộc cùng một chu kì trong bảng tuần hoàn.
(b) Nguyên tử của nguyên tố Y có 5 orbital chứa electron.
(c) Nguyên tố Y có bán kính nguyên tử nhỏ hơn nguyên tố T.
(d) Bán kính anion T- lớn hơn cation X+.
Số phát biểu đúng là
Trả lời bởi giáo viên
(a) đúng vì cả 4 nguyên tố đều có cùng số lớp electron
(b) sai. Cấu hình electron nguyên tử của Y là 1s22s22p2
Biểu diễn bằng cấu hình orbital nguyên tử:
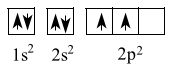
=> Nguyên tố Y có 4 orbital nguyên tử chứa electron
(c) sai
Có 4 nguyên tố trên đều cùng thuộc một chu kì. Thứ tự sắp xếp theo chiều tăng dần số đơn vị điện tích hạt nhân là Y, Z, X, T
Trong một chu kì theo chiều tăng dần số đơn vị điện tích hạt nhân, bán kính nguyên tử giảm dần
=> Thứ tự giảm dần về bán kính nguyên tử là Y>Z>X>T
=> Y có bán kính nguyên tử lớn hơn T
(d) đúng
Có các bán phản ứng sau:
\(X \to {X^ + } + 1e\) => Để tạo thành X+ thì X mất đi 1 electron => X+ có 2 lớp electron
\(T + 1e \to {T^ - }\) => Để tạo thành T- thì T thêm 1 electron => T- có 3 lớp electron
=> T- có bán kính nguyên tử lớn hơn X+
=> Số phát biểu đúng là 2